Chargement de l'article...
Écriture : Élodie Billard
Relecture scientifique : Éléonore Bellot
Relecture de forme : Sylvain Le Grill et Eléonore Pérès
Temps de lecture : environ 11 minutes.
Thématiques : Microbiologie (Biologie) et Écologie
Publication originale : Morono Y., et al., Aerobic microbial life persists in oxic marine sediment as old as 101.5 million years. Nature Communications, 2020. DOI : 10.1038/s41467-020-17330-1
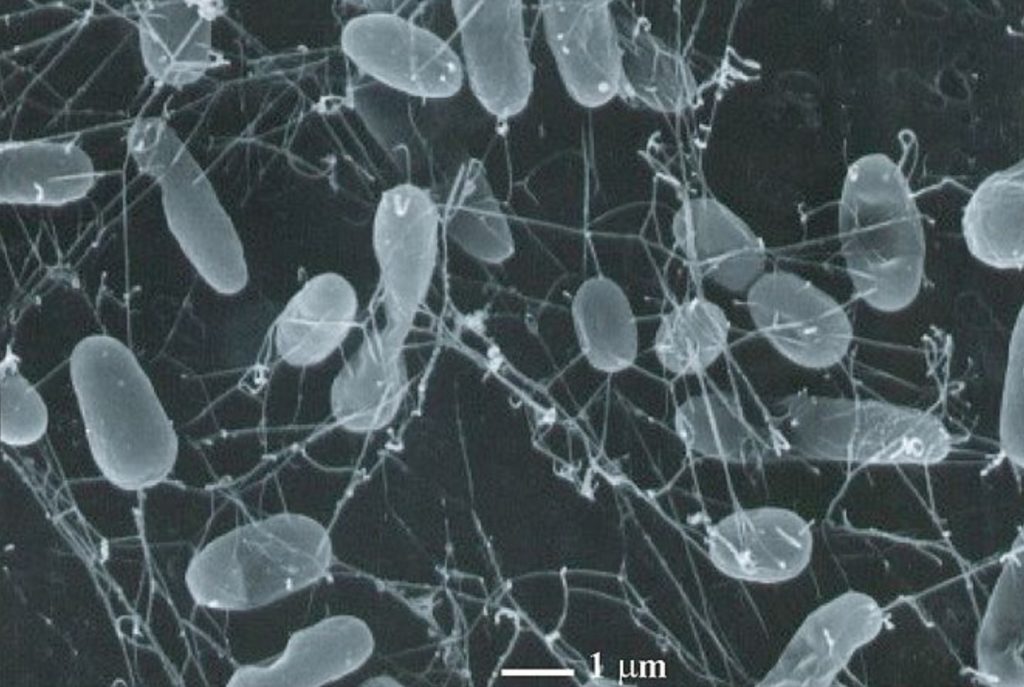
Si on vous dit qu’une équipe de recherche a réussi à faire revivre des organismes vivants il y a 100 millions d’années, vous imaginez probablement une bande de T-rex semant la panique en ville (merci Jurassic Park !). Exit les dinosaures, bonjour les bactéries. Ici nous allons expliquer comment une équipe de chercheurs japonais et américains a réussi à faire revivre et se multiplier, sur une période de 18 mois, des microorganismes vivants dans des sédiments marins datés d’il y a 101,5 millions d’années.
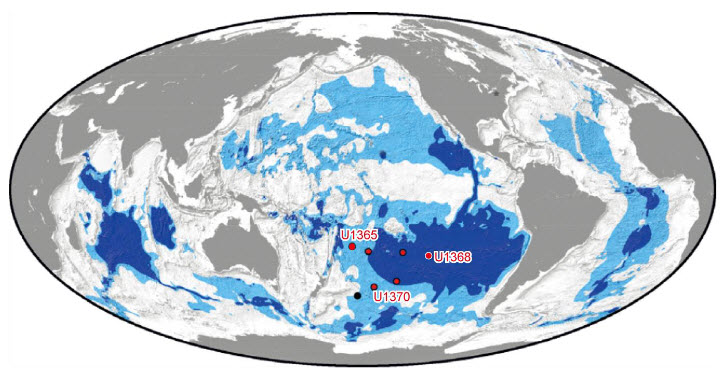
La Terre est souvent appelée « la planète bleue » à cause des océans qui recouvrent environ 70 % de sa surface. Pourtant les profondeurs océaniques sont l’un des lieux les moins connus de notre planète. Elles sont recouvertes de sédiments, c’est-à-dire de particules en suspension dans l’eau qui se sont déposées en couches successives sur le fond. Ces sédiments sont caractérisés par leur nature, leur origine, leur taille et les espèces qui y vivent. Parmi ces dernières vit un grand nombre de microorganismes dont la diversité et les modes de vie sont encore largement mal compris. C’est donc pour tenter de percer les mystères qui entourent cette vie microbienne des fonds marins que l’équipe emmenée par le chercheur Yuki Morono a travaillé sur des sédiments d’un lieu bien particulier sur Terre. Ce lieu, c’est le gyre subtropical du Pacifique Sud (Figure 1). Les gyres, venant de rotation en grec, sont des tourbillons d’eau océanique formés par un ensemble de courants marins. Ils sont provoqués par un mouvement de rotation qui tourne dans le sens des aiguilles d’une montre dans l’hémisphère Nord et en sens inverse dans l’hémisphère Sud.
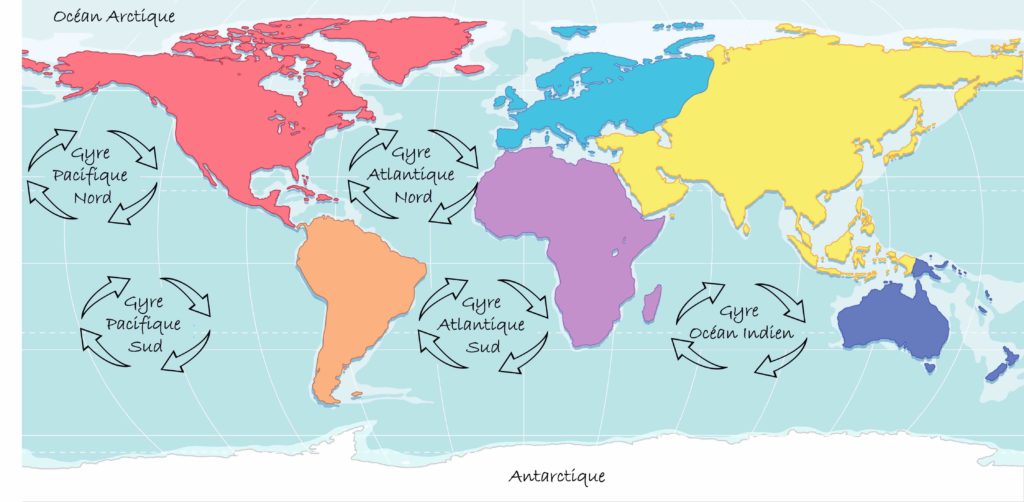
Le gyre subtropical du Pacifique Sud (abréviation SPG) est situé entre l’Amérique du Sud et l’Australie. C’est le plus grand gyre océanique sur Terre et son centre est plus éloigné des continents que tous les autres gyres existants. La particularité de cette zone est qu’elle est très pauvre en vie marine. Elle est considérée comme la région du monde où la productivité (c’est-à-dire la quantité de matière organique produite dans un volume d’eau, pendant un temps donné) est la plus faible sur Terre.
Cela s’explique par plusieurs raisons. Comme dit précédemment, les sédiments sont caractérisés par leur nature et leur taille. Ici, ils sont de nature argileuse et calcaire donc très fins (autour de 0,02 micron, soit la même taille que les plus petits virus), avec pour conséquence une très faible perméabilité : on ne s’infiltre pas facilement entre les particules ! Cette propriété du milieu limite la mobilité des microorganismes qui y vivent et rend difficile les déplacements. Pas facile de trouver de quoi se nourrir dans ces conditions, d’autant plus que cette zone est particulièrement pauvre en éléments nutritifs. Enfin, pour en rajouter une couche, les sédiments dans le SPG s’accumulent à un taux extrêmement faible d’un à deux mètres par million d’années. Qu’est-ce que tout cela veut dire ? Que ce n’est pas facile de faire ses courses quand les rayons sont approvisionnés au compte-goutte. En résumé, ils n’ont « pas grand-chose à se mettre sous la dent » et n’ont qu’une très faible zone de déplacement pour trouver le peu de nourriture à disposition. Ceci limite donc fortement leur multiplication. Les microorganismes présents dans ces sédiments y ont été piégés peu de temps après leur dépôt. Leur étude permet donc de savoir si la vie peut subsister dans un environnement aussi limité en nutriments. Et si oui, pendant combien de temps elle peut s’y maintenir dans de telles conditions.
À la recherche de vie cachée
Pour cette étude, les sédiments du SPG ont été prélevés lors d’une campagne menée en 2010 [*]. Les différentes caractéristiques de ceux-ci sont résumées dans le Tableau 1.
| Nom de l’échantillon | Caractéristiques des sédiments | Âge (en Million d’années) | Profondeur sous l’eau (en mètre) | Profondeur dans les sédiments (en mètre) |
| E1 | Argile | 95,4 Ma | 5 697 m | 68,9 m |
| E2 | Argile | 101,5 Ma | 5 697 m | 74,5 m |
| E3 | Calcaire | 4,3 Ma | 3 739 m | 1,6 m |
| E4 | Calcaire | 13 Ma | 3 739 m | 14,7 m |
Afin de ne pas perdre en qualité au niveau des échantillons prélevés, les scientifiques ont commencé l’expérimentation directement pendant l’expédition. Les échantillons ont été placés dans des flacons (Figure 2) en présence d’oxygène et avec des éléments nutritifs à base de carbone (bicarbonate, acétate, glucose, pyruvate) et d’azote (ammonium) contenant un marquage permettant de suivre l’évolution de la consommation de ces éléments tout au long de l’expérience. Ils ont ensuite réalisé une série de prélèvements à différents temps (T) :
- T0 : au début de l’expérimentation (point de référence) ;
- T1 : 21 jours après le début de l’expérience ;
- T2 : à 68 jours (6 semaines) ;
- T3 : à 557 jours (18 mois).

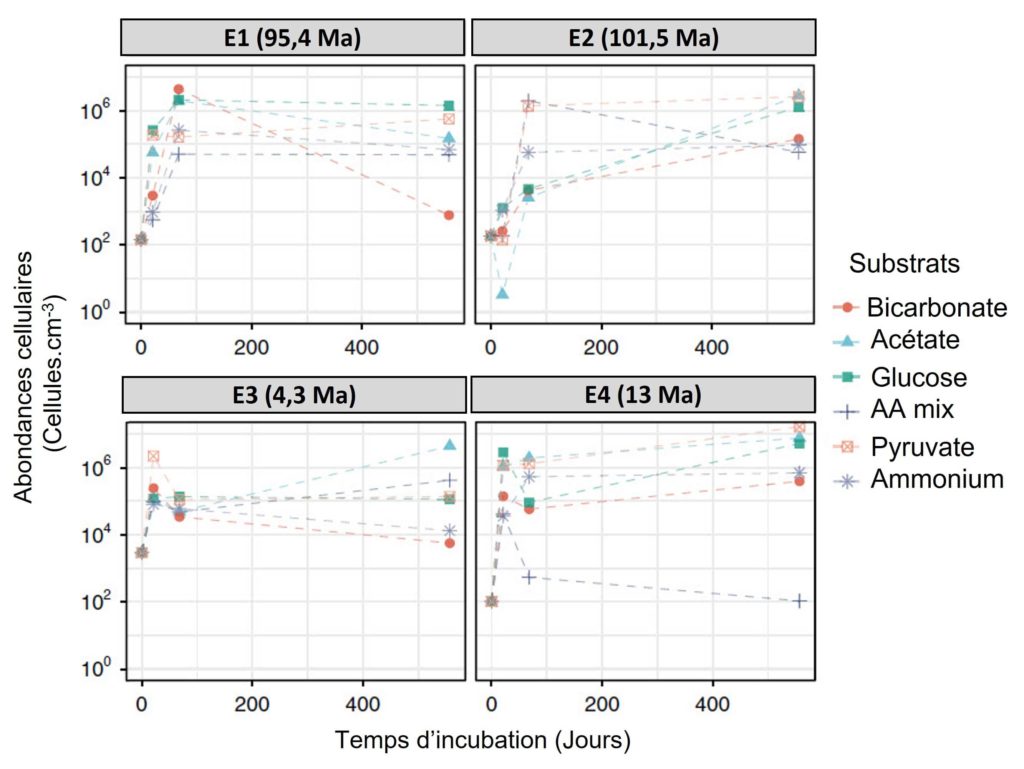
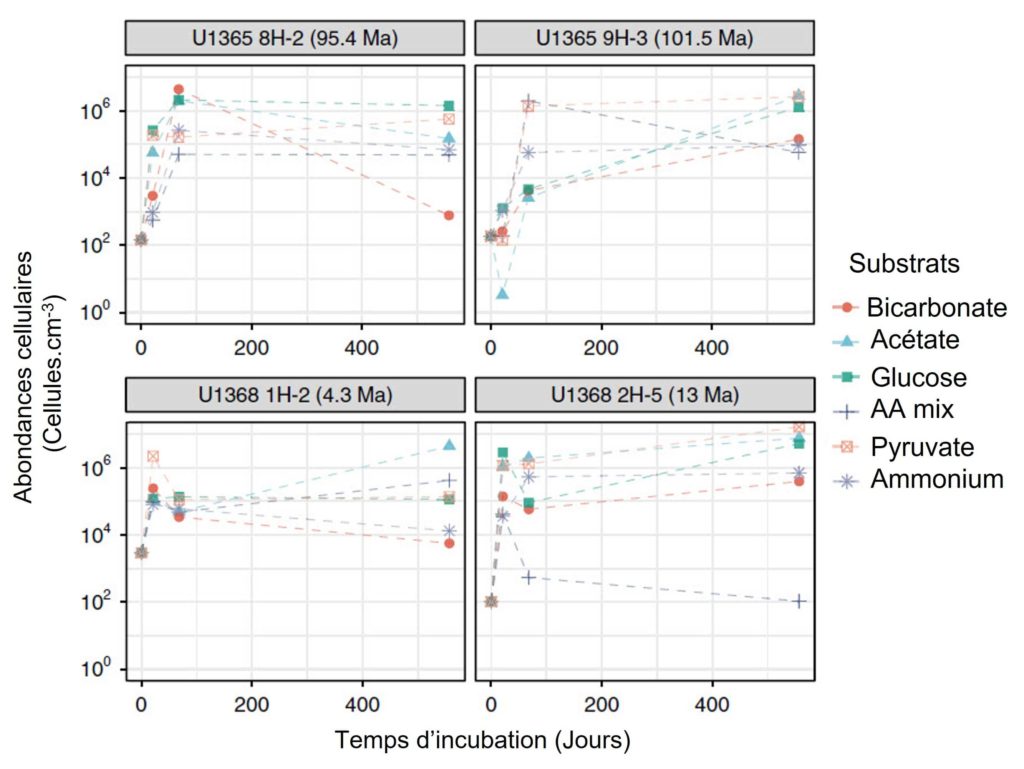
L’équipe de recherche a commencé par mesurer le nombre de microorganismes (appelée abondance cellulaire) présents dans les échantillons à chaque prélèvement. Ils ont observé un très faible nombre de cellules à T0, entre 100 à 3 000 cellules par cm3 (Figure 3). À titre de comparaison, ceci est environ 3 à 4 fois plus faible en moyenne que dans d’autres sédiments de la zone [1]. L’abondance a fortement augmenté à partir de T1 avant d’atteindre un maximum à T2 (de l’ordre de la centaine de milliers (105) au million (106) de cellules par cm3) puis de stagner jusqu’à la fin de l’expérience (Figure 3).
Les auteurs ont alors mesuré le pourcentage de microorganismes qui a été réactivé — c’est-à-dire réveillé/réanimé et donc capable de reprendre une activité biologique — lors de l’expérimentation. Celui-ci est compris entre 24 et 99 % (avec une moyenne à 77 %) sur l’ensemble de l’expérience. C’est dans l’échantillon le plus ancien (E2, âgé de 101,5 Ma) que le pourcentage de réactivation a été le plus élevé (99 %). Qu’est-ce que cela signifie ? Cela veut dire que la plus grande partie des microorganismes vivants dans ces sédiments est encore en vie après plusieurs millions d’années passés dans un milieu très pauvre en éléments nutritifs.
Les scientifiques ont aussi voulu savoir en combien de temps la masse des microorganismes doublait. Cette information permet de savoir à quelle vitesse ils se multiplient. En moyenne, il leur a fallu quasiment 5 jours d’incubation (allant de 1,5 jour à presque 18 jours en fonction des échantillons). Les temps de doublement les plus courts ont été observés pour les sédiments les plus jeunes et inversement, les temps les plus longs dans les sédiments les plus âgés. L’ensemble des résultats obtenus avec l’échantillon daté de 101,5 Ma montre que tous les microorganismes restant dans ces sédiments sont capables de se réactiver quand les conditions leurs redeviennent favorables, même s’il leur faut un temps d’adaptation plus long que pour ceux des sédiments plus jeunes.
Qu’est-ce qu’il y a au menu ?
Nous venons de voir qu’avec des conditions environnementales adaptées, les microorganismes enfouis depuis des millénaires sont capables de retrouver une activité métabolique. Les questions qui se posent maintenant sont les suivantes : que mangent-ils ? ont-ils un plat préféré parmi ceux fournis lors de l’expérience ? Pour rappel, les échantillons ont été mis en présence de différentes sources nutritives à base de carbone et d’azote. Ces éléments ont été marqués pour que l’on puisse suivre leur consommation par les microorganismes tout au long de l’expérimentation. Ainsi, pour chaque échantillon, on sait quelle source nutritive a été consommée et en quelle quantité pendant toute l’expérience. Chaque échantillon a été mis en présence d’une source de carbone, à savoir du glucose, de l’acétate, du pyruvate, du bicarbonate et une source d’azote : de l’ammonium. Un mélange de 20 acides aminés (molécules constitutives des protéines) à base de carbone et d’azote (abréviation AAmix) a aussi été testé. De plus, un témoin a été réalisé avec seulement de l’azote (Figure 3).
Les résultats ont montré une réponse hétérogène en fonction des sources nutritives. Toutefois, les réponses ont toujours été rapides, dès T1 (21 jours), et avec une préférence pour la source d’azote par rapport au carbone. Ceci est dû, d’après l’équipe de recherche, au bon rapport qualité/coût de l’assimilation de la source d’azote utilisée lors de l’expérience. En effet, l’ammonium est facilement assimilable par les microorganismes et avec un faible coût énergétique par rapport à d’autres sources d’azote déjà présentes naturellement dans les sédiments (sous forme de nitrate). Pour les sources de carbone, il y a peu de différence entre elles, à part un faible intérêt pour le bicarbonate. Ceci est normal car les autres sources de carbone sont facilement utilisables par les microorganismes pour leur croissance et leur fonctionnement. Ces molécules ont un grand intérêt métabolique pour les microorganismes donc elles ont été assimilées facilement.
À ce stade, il nous reste donc à savoir qui sont ces microorganismes survivants enfouis depuis si longtemps ?
L’heure de démasquer les microbes !
Les connaissances de la diversité des microorganismes vivants dans les sédiments marins profonds sont très faibles. Ceci s’explique d’une part par le très petit nombre de cellules dans ces sédiments (rappel : 100 à 3 000 cellules par cm3 ; Figure 3) et d’autre part par la nature même de ceux-ci. Ils sont composés d’argiles et de limons très fins (rappel : autour de 0,02 micron) qui ont tendance à se coller à l’ADN lors de son extraction et rendre son analyse plus difficile. Or, pour identifier précisément ces microorganismes, il faut justement extraire leur ADN puis le séquencer. Donc, pour récolter un maximum d’informations, les chercheurs ont commencé par faire un tri des cellules pour les séparer du sédiment avant d’extraire leur ADN.
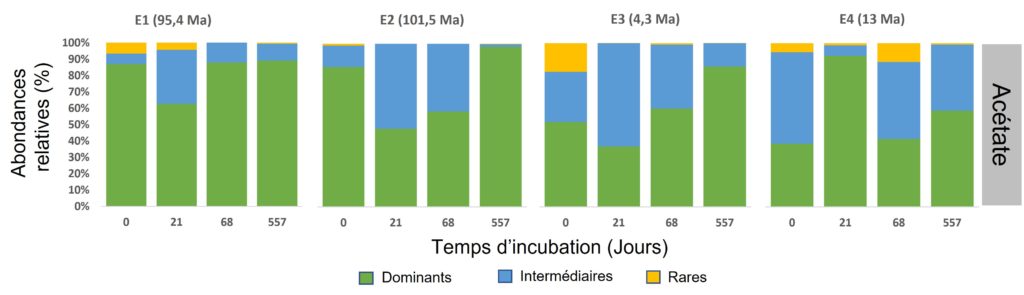
Grâce à ce travail, l’équipe de recherche a pu identifier différentes espèces de microorganismes, principalement des bactéries, que nous pouvons regrouper en trois grandes catégories (Figure 4) :
- les dominants : représentés par les Alpha et Gammaprotéobactéries. Ils sont présents dans tous les échantillons, dans toutes les conditions et tout au long de l’expérience avec, généralement, plus de 50 % de l’abondance cellulaire ;
- les intermédiaires : représentés par les Beta et Deltaprotéobactéries, les Actinobactéries, les Bacteroïdetes et les Firmicutes. Ils sont présents dans la plupart des échantillons, des conditions et des temps de prélèvements mais en abondance beaucoup plus faible ;
- les rares : telles que les Acidobactéries, les Chloroflexi, les Cyanobactéries et bien d’autres sont présents ponctuellement dans l’un ou l’autre des échantillons ou à un temps ou une condition données et en faible abondance généralement.
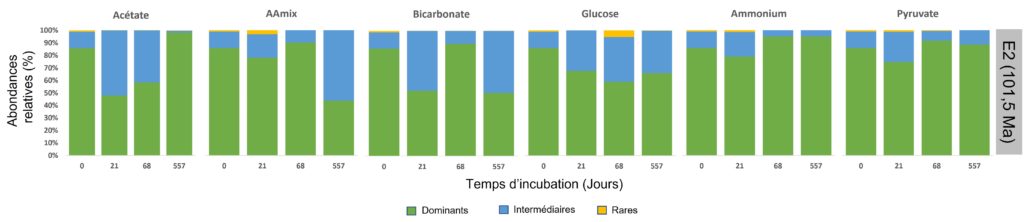
Afin de vérifier que cette diversité est bien le reflet réel de la composition des microorganismes dans les sédiments et non le reflet des conditions expérimentales mises en place, l’équipe a étudié à chaque prélèvement la structure de la communauté, c’est-à-dire le nombre d’espèces présentes et leurs abondances respectives, en fonction de différents paramètres (tels que l’apport des sources nutritives en carbone (C) et azote (N), le temps d’incubation, l’âge des sédiments, etc.). Elle a alors remarqué que l’ajout des différentes sources nutritives n’avait pas fait changer globalement la composition des microorganismes dans les différents échantillons (Figure 5). En revanche, la ou les communautés dominantes peuvent varier au cours du temps au sein d’un échantillon (Figure 5). Ceci s’explique par le fait que les microorganismes ne répondent pas tous de la même façon, certains ont besoin de plus de temps que d’autres pour réactiver leur métabolisme. À chacun son rythme !
L’échantillon le plus âgé, E2, montre une composition microbienne qui diffère des autres échantillons (Figure 4), et ceci, quelle que soit la source nutritive testée ou le temps d’incubation. L’âge de cet échantillon (101,5 millions d’années) a donc eu un impact sur la composition des organismes qui y vivent. Ou plutôt, c’est la durée depuis laquelle ils sont enfouis dans ces sédiments aux conditions de vie extrêmes qui a impacté la composition microbienne.
Pour conclure, cette étude nous montre que les microorganismes sont capables de survivre très longtemps dans des conditions extrêmes et d’être réactivés à la faveur de conditions environnementales plus favorables (apports nutritifs notamment). Il est à noter que bien que nous connaissions l’âge des sédiments, nous ne connaissons pas l’âge réel des microorganismes qui ont été réactivés. Toutefois, les caractéristiques du milieu (faible mobilité, peu d’apport nutritif et faible taux de sédimentation) permettent d’envisager que des organismes sont relativement âgés (peut être que certains ont croisé un mégalodon, qui sait !).
[*] Les sédiments ont été prélevés lors de l’Expédition 329 du Integrated Ocean Drilling Program (IODP).
[1] D’Hondt S., et al., Subseafloor sedimentary life in the South Pacific Gyre. PNAS, 2009. DOI : 10.1073/pnas.0811793106. [Publication scientifique]
Écriture : Élodie Billard
Relecture scientifique : Éléonore Bellot
Relecture de forme : Sylvain Le Grill et Eléonore Pérès
Temps de lecture : environ 10 minutes.
Thématiques : Microbiologie (Biologie) et Écologie
Publication originale : Morono Y., et al., Aerobic microbial life persists in oxic marine sediment as old as 101.5 million years. Nature Communications, 2020. DOI : 10.1038/s41467-020-17330-1

Si on vous dit qu’une équipe de recherche a réussi à faire revivre des organismes vivants il y a 100 millions d’années, vous imaginez probablement une bande de T-rex semant la panique en ville (merci Jurassic Park !). Exit les dinosaures, bonjour les bactéries. Ici nous allons expliquer comment une équipe de chercheurs japonais et américains a réussi à faire revivre et se multiplier, sur une période de 18 mois, des microorganismes vivants dans des sédiments marins datés d’il y a 101,5 millions d’années.
Les sédiments marins recouvrent environ 70 % de la surface de la Terre et recèlent une incroyable diversité microbienne. Toutefois, celle-ci est encore largement mal comprise tant dans sa diversité que dans sa physiologie. Alors, pour tenter de percer les mystères qui entourent l’écophysiologie des microorganismes vivants dans les profondeurs des sédiments marins, l’équipe emmenée par le chercheur Yuki Morono a travaillé sur des sédiments issus du gyre subtropical du Pacifique Sud (entre l’Amérique du Sud et l’Australie) (Figure 1). Les gyres (signifiant rotation en grec) sont des tourbillons d’eau océanique formés par un ensemble de courants marins. Ils sont provoqués par la force de Coriolis et tournent dans le sens des aiguilles d’une montre dans l’hémisphère Nord et en sens inverse dans l’hémisphère Sud (Figure 1).

Le gyre subtropical du Pacifique Sud (abréviation SPG) est le plus grand gyre océanique sur Terre et c’est une zone particulièrement pauvre en vie marine [*]. À titre de comparaison, à profondeur égale l’abondance en microorganismes au niveau du SPG est 1 à 7 fois plus faible que dans les marges océaniques ou les upwelling (remontées d’eau froide en surface le long de certains littoraux océaniques). C’est aussi la région du monde où la productivité — c’est-à-dire la quantité de matière organique produite dans un volume d’eau pendant un temps donné — est la plus faible sur Terre. De ce fait, les sédiments de cette zone sont particulièrement pauvres en éléments nutritifs.
À cela s’ajoute une accumulation sédimentaire extrêmement faible (d’un à deux mètres par million d’années) et une très faible perméabilité, liée à la nature des sédiments : les argiles, par exemple, sont constituées de très petits espaces (des pores, d’une taille d’environ 0,02 micron) qui ne permettent pas à l’eau de s’infiltrer facilement. Cette propriété impacte le déplacement des microorganismes dans les sédiments en limitant leur mobilité. Toutes ces caractéristiques combinées font que les sédiments de cette zone ont permis le piégeage des communautés microbiennes probablement peu de temps après leur dépôt. L’étude des microorganismes benthiques issus du SPG permet donc de savoir si la vie peut exister dans un environnement aussi limité en nutriments. Et si oui, pendant combien de temps elle peut s’y maintenir.
| Nom de l’échantillon | Caractéristiques des sédiments | Âge (en Million d’années) | Profondeur sous l’eau (en mètre) | Profondeur dans les sédiments (en mètre) |
| U1365 8H-2 | Argile pélagique | 95,4 Ma | 5 697 m | 68,9 m |
| U1365 9H-3 | Argile pélagique | 101,5 Ma | 5 697 m | 74,5 m |
| U1368 1H-2 | Calcaire oligotrophe | 4,3 Ma | 3 739 m | 1,6 m |
| U1368 2H-5 | Calcaire oligotrophe | 13 Ma | 3 739 m | 14,7 m |
| U1370 7H-6 | Argile métallifère | 65,5 Ma | 5 075 m | 62,9 m |
Pour cette étude, les sédiments ont été prélevés dans la plaine abyssale du SPG lors d’une campagne en 2010 [**] dont les caractéristiques sont résumées sans le Tableau 1 et la Figure 2.
Mise en culture et expérimentation : « Il y a quelqu’un ? »
Afin de pouvoir identifier les communautés microbiennes benthiques autotrophes et hétérotrophes, les sédiments récoltés ont été mis en incubation très rapidement à bord lors de l’expédition. Les échantillons ont été mis en présence d’oxygène (sauf pour l’échantillon U1370, plus de détails plus bas) et avec des substrats marqués par des isotopes stables [***] afin de suivre les activités métaboliques microbiennes. Au démarrage de l’incubation, un prélèvement a été réalisé, figé puis congelé immédiatement afin de servir de point de référence (T0). Ensuite 3 prélèvements ont été effectués à T1 : 21 jours après le début de l’incubation, à T2 : 68 jours (6 semaines) et à T3 : 557 jours (18 mois).
À T0, il a été observé dans les échantillons un nombre de cellules extrêmement faible, allant de 102 à 3.103 cellules.cm-3 (Figure 3). Pour les quatre échantillons U1365 et U1368, les scientifiques ont montré, dès le prélèvement à T1, une augmentation significative de l’abondance des cellules qui se poursuit jusqu’à T2, atteignant un maximum de l’ordre de 105 à 106 cellules.cm-3 avant de globalement stagner jusqu’à la fin de l’expérimentation (Figure 3).
L’échantillon U1370 (daté de 65,5 Ma) n’a pas été mis en présence d’oxygène supplémentaire du fait de la faible quantité d’O2 disponible dans l’eau interstitielle de cette zone (1,5 µM contre 70 et 150 µM [****] pour les deux autres). Ceci a permis de tester si l’on pouvait faire repartir les microorganismes dans de faibles conditions d’oxygénation du milieu avec seulement un apport nutritif. Après incubation, il n’y a pas eu d’augmentation significative de l’abondance cellulaire et une faible incorporation des différents substrats testés. Les auteurs suggèrent donc que l’activité métabolique a eu des difficultés à reprendre et n’a pas persisté dans ces conditions expérimentales (absence d’ajout d’oxygène) pour les communautés microbiennes qui ont été exposées à de faibles quantités d’O2 dissous sur une très longue période géologique (ici 65 Ma). Ceci a pu éteindre les microorganismes anaérobies ou au moins les rendre très difficiles à faire revivre.
Concernant les quatre échantillons U1365 et U1368, les auteurs ont mesuré la partie microbienne hétérotrophe qui a été réactivée lors de l’expérimentation. Celle-ci est comprise entre 24,1 et 99,1 % (pour une moyenne de 77,7 %). Le plus surprenant est que le pourcentage maximum de microorganismes réactivés (99,1 %) a été observé dans l’échantillon le plus ancien (U1365 9H-3 ; 101,5 Ma). Les chercheurs ont aussi observé que la biomasse des microorganismes doublait en moyenne au bout de 4,9 jours d’incubation (variant entre 1,4 et 17,9 jours). Les temps de doublement les plus courts ont été observés pour les sédiments les plus jeunes et une différence significative a été montrée pour les sédiments de l’échantillon le plus ancien avec un temps de doublement moyen de 9,8 jours (compris entre 5,1 et 17,9 jours).
Suivi de l’activité métabolique : fini la sieste !
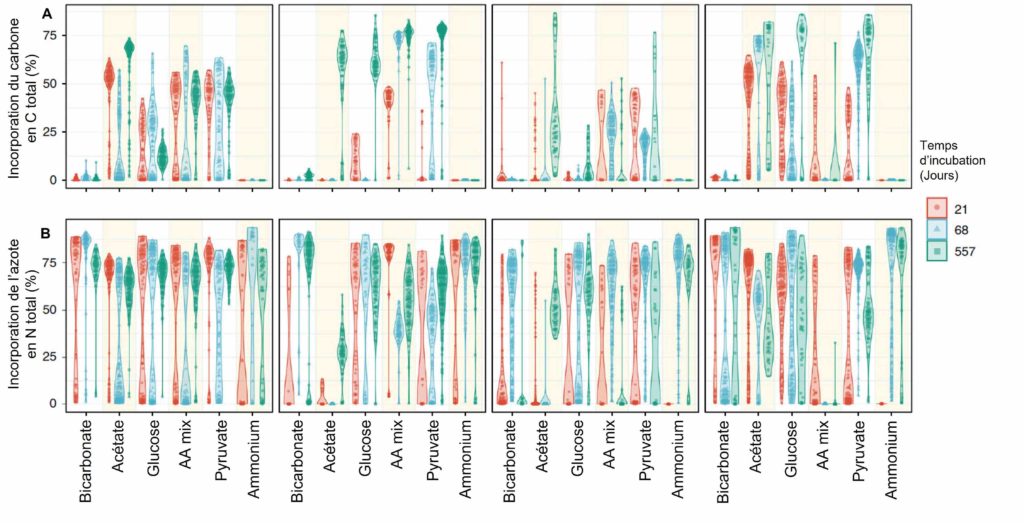
Afin de suivre l’activité métabolique des communautés microbiennes réactivées, les différentes sources de carbone et d’azote ont été marquées avec des isotopes stables. Un contrôle a aussi été réalisé, uniquement avec de l’ammonium et sans source de carbone supplémentaire. La réponse des communautés microbiennes à l’addition de ces substrats a été hétérogène mais globalement très rapide, dès T1, et plus importante pour l’azote que pour le carbone (Figure 4). Pour les auteurs, l’incorporation préférentielle de l’ammonium (15N) par rapport au nitrate (déjà présent dans les échantillons, environ 40 µM) est liée au coût énergétique plus important pour transformer le nitrate en acides aminés par rapport à l’ammonium. Cette incorporation préférentielle a aussi été observée en absence de source carbonée (Figure 4, courbe « Ammonium »). Quant à l’incorporation des sources de carbone, l’acétate, le glucose et le pyruvate sont incorporés sans différence significative. Seul le bicarbonate montre une très faible incorporation à la biomasse cellulaire (Figure 4), ceci étant cohérent, d’après les auteurs, avec la dépendance des communautés microbiennes à l’égard de la matière organique comme source de carbone pour la production de biomasse.
Étude de la diversité microbienne : qui est-ce ?
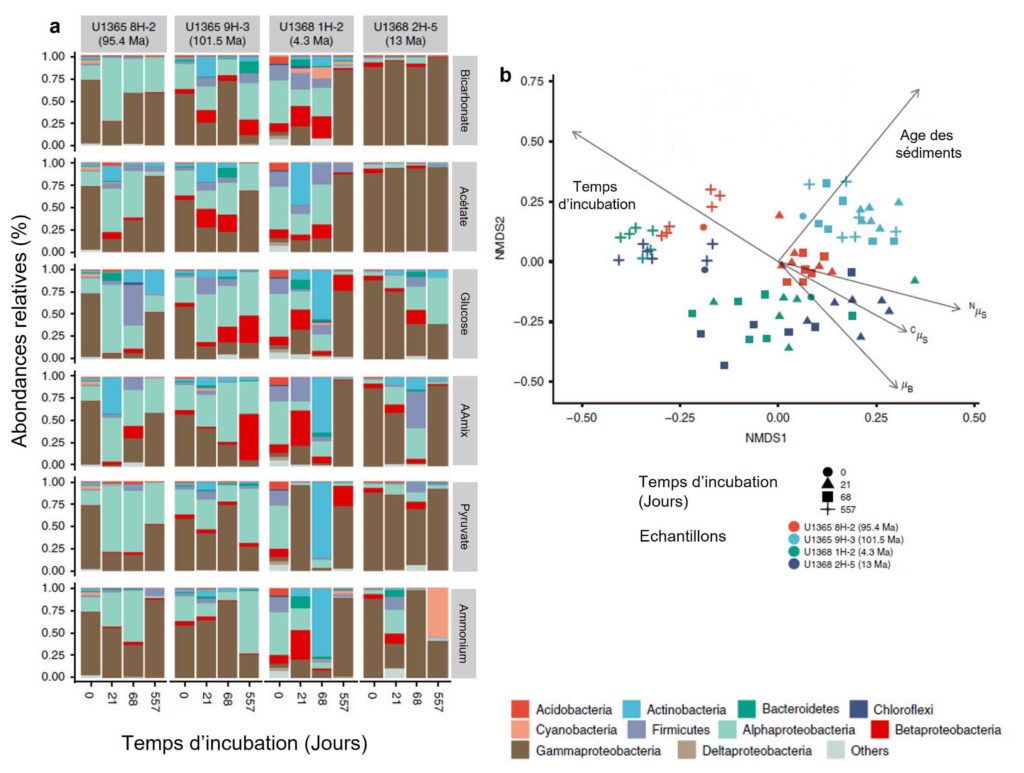
Pour finir, les auteurs ont aussi analysé la diversité microbienne. Celle-ci n’avait jusqu’alors été effectuée que dans le premier mètre dans la profondeur des sédiments. L’absence de données sur la composition microbienne dans les sédiments marins profond est liée, d’une part, à la faible abondance des cellules (100 à 3 000 cellules.cm-3, de l’ordre 3 à 4 fois plus faible en moyenne que dans d’autres sédiments de la zone [1]) et d’autre part à la nature même des sédiments, fait d’argile et de limon très fins. En effet, ceux-ci adsorbent l’ADN libéré par la lyse cellulaire lors de son extraction. Les chercheurs ont donc séparé et trié les cellules du sédiment avant l’extraction de l’ADN afin de pouvoir obtenir la composition taxonomique des communautés présentes. Ainsi, ils ont observé que les communautés dominantes dans les sédiments (échantillons U1365 et U1368) sont les Protéobactéries (alpha, bêta, gamma et delta) ainsi que les Actinobatéries, les Bacteroides et les Firmicutes (Figure 5a). Une petite fraction de Chloroflexi (entre 0 et 2,6 %), de Cyanobactéries (dans l’échantillon U1368 2H-5, 13 Ma) et d’Archées thermophiles (environ 7 %, U1368 2H-5, 13 Ma) a aussi pu être identifiée.
Il n’a pas été observé de modification significative de la diversité microbienne dans les échantillons au cours de l’incubation en lien avec les différents substrats ajoutés (Figure 5b, flèches µB, CµS et NµS). Les auteurs estiment donc que l’addition des substrats participe à la stimulation de l’activité microbienne pour les composés carbonés et azotés naturellement présents dans les sédiments. En revanche, les auteurs n’ont pas trouvé de dépendance entre la composition des communautés et le temps d’incubation, ce qui suggère que les différentes communautés ont répondu à l’incubation à différentes échelles de temps (Figure 5b). On observe aussi que les échantillons du site le plus âgé (U1365 9H-2) montrent une différence dans la structure des communautés par rapport aux autres échantillons, et ceci, quel que soit le temps d’incubation ou les substrats mis en présence (Figure 5b, en bleu clair).
Pour conclure, les résultats de cette étude suggèrent que les communautés microbiennes présentes dans les sédiments abyssaux du SPG, pauvres en matière organique, sont principalement des microorganismes aérobies qui conserveraient leur potentiel métabolique dans des conditions de très faible énergie et ceci pendant au moins 100 millions d’années. Il est important de rappeler qu’aucune information concernant la vitesse de multiplication des microorganismes dans les sédiments avant l’expérimentation n’est connue. En conséquence, nous n’avons pas connaissance de l’âge réel des communautés réactivées. Toutefois, la composition des sédiments qui limite fortement la mobilité des organismes (faible perméabilité), le peu d’éléments nutritifs à disposition (multiplication limitée) et le faible taux de sédimentation de cette région permettent d’envisager que ces organismes sont toutefois assez âgés (peut être que certains ont croisé un mégalodon, qui sait !).
[*] Les nutriments sont emportés par les courants marins (flèches blanches Figure 1), et, comme dans l’œil d’un cyclone, c’est le calme plat au centre de ces courants. Ici, le gyre est tellement grand que les courants marins sont très éloignés du centre. Il y a donc particulièrement peu de nutriments. Pour plus d’informations, voir le résumé de l’expédition.
[**] Les sédiments ont été prélevés lors de l’Expédition 329 du Integrated Ocean Drilling Program (IODP).
[***] Liste des isotopes stables utilisés lors de l’expérimentation : 13C6-glucose, 13C2-acétate, 13C3-pyruvate, 13C-bicarbonate, 13C-15N mix d’acides aminés (mélange de 20 acides aminés, abréviation AAmix) et 15N-ammonium
[****] M pour molaire = mol/L, voir aussi ici.
[1] D’Hondt S., et al., Subseafloor sedimentary life in the South Pacific Gyre. PNAS, 2009. DOI : 10.1073/pnas.0811793106. [Publication scientifique]