L’expérience historique à l’origine de la chimie prébiotique
Écriture : Ulysse Pedreira-Segade
Relecture scientifique : Caroline Bouvier et Lambert Baraut-Guinet
Relecture de forme : Carine Mira et Aurélien Schwob
Temps de lecture : environ 23 minutes.
Thématiques : Géochimie & Cosmochimie (Chimie & Géologie)
Publication originale : Miller S.L., A Production of Amino Acids Under Possible Primitive Earth Conditions. Science, 1953. DOI : 10.1126/science.117.3046.528

L’étude des origines de la vie sur Terre a longtemps manqué d’une identité propre pour les biologistes et les chimistes qui menaient ce travail en parallèle de leur recherche institutionnalisée. Aujourd’hui pourtant, cette discipline que l’on nomme astrobiologie est en vogue : NASA, rovers martiens, sondes spatiales, télescopes géants sur Terre et dans l’espace, roches anciennes et fossiles de microbes, etc. Il y a 70 ans, Stanley Miller, alors doctorant, publie seul un article qui va révolutionner cette science. Un petit retour en arrière, ça vous tente ?
À Chicago, vous pourriez marcher dans les couloirs universitaires du G.H. Jones Laboratory et découvrir sur un mur, à côté d’une porte tout ce qu’il y a de plus banal, une plaque noire dans un cadre couleur or. Rien, jusque-là, ne vous laisserait penser que ce laboratoire a été par deux fois au moins déterminant pour l’étude des origines de la vie sur Terre et la recherche de vie dans l’Univers, le champ disciplinaire que l’on nomme aujourd’hui astrobiologie. En vous approchant de cette plaque, vous y verriez de grosses lettres dorées déclarant que la pièce 405 de ce bâtiment, la porte juste à côté de vous, a été consacrée Site National Historique des États-Unis. C’est là qu’a été produit, isolé, puis caractérisé pour la première fois un élément chimique artificiel : le plutonium [1]. Cet élément radioactif est aujourd’hui moteur dans notre exploration de l’Univers. À la surface de Mars, deux rovers, Curiosity et Perseverance, cherchent inlassablement de possibles traces du vivant, équipés d’un système qui génère de l’énergie à partir de la désintégration du plutonium. Je trouve fascinant qu’on puisse ainsi relier, dans l’espace et le temps, des événements qui, d’apparence, n’ont pas grand-chose à voir… Comment ? Et le deuxième haut fait astrobiologique de ce laboratoire ? Je vois que vous ne perdez pas le nord ! J’y viens, j’y viens.
De ce même laboratoire donc, émane une publication scientifique qui a transformé durablement la recherche des origines de la vie. Elle est d’ailleurs souvent créditée comme étant à l’origine de l’astrobiologie moderne. Pourtant, ce papier de 1953, publié par Stanley L. Miller, alors doctorant, est presque surprenant de sobriété. Pourquoi un papier d’apparence si simple a-t-il eu un tel impact ? Menons l’enquête ensemble sur cette expérience historique.
Les faits : une publication presque cryptique
Dans l’édition du 15 mai 1953 du prestigieux journal Science, un article, parmi les huit publiés dans la section « Papiers Techniques », capte l’attention des lecteurs et lectrices [*]. Pour l’œil aguerri d’une personne habituée à lire ce genre de journaux scientifiques spécialisés, quelque chose de rare semble se jouer dès la découverte du titre de l’article : « Une production d’acides aminés dans des conditions possibles de la Terre primitive ». C’est un papier qui se focalise sur un domaine où les résultats expérimentaux sont encore rares : comprendre la formation des briques élémentaires du vivant avant l’apparition de la vie sur la surface de notre planète, il y a plus de 4 milliards d’années.
Attardons-nous un instant sur sa structure. De prime abord, il est vrai que le papier fait deux pages à peine, figures et références incluses. C’est certes court, mais rien d’alarmant. D’ailleurs, sept des huit articles de cette édition font deux pages.
Plus étonnant, avec seulement trois références pour appuyer son travail, l’auteur fait dans la sobriété. À y regarder de plus près, ce sont même des références généralistes et théoriques qui viennent uniquement servir de base aux hypothèses énoncées. L’auteur ne cite aucun travail précédent pouvant faire écho aux résultats expérimentaux qu’il présente, ce qui d’ordinaire est une pratique courante. Pour un œil non averti, ce pourrait être le signe d’un papier en avance sur son temps. Est-ce vraiment le cas ?
De plus, si on plisse les yeux et qu’on lit la fine écriture qui termine l’article, on découvre que le manuscrit a été reçu en février 1953. Les sept autres papiers de cette édition, eux, proviennent de manuscrits soumis à l’éditeur en septembre 1952. Trois mois, plutôt que neuf, pour que cet article passe par toutes les étapes qui mènent à sa publication. Nous nous pencherons sur le contenu de ce papier et son contexte pour comprendre cette rapidité de publication.
Le papier se démarque également par le champ disciplinaire qu’il aborde. Si la majorité des publications de cette édition traitent de chimie, de biologie ou d’une combinaison des deux, celui-ci évoque un domaine de la recherche expérimentale encore balbutiant : la recherche des origines de la vie sur la Terre primitive. Cette question agite les chimistes autant que les biologistes depuis de nombreuses années. Toutefois, les travaux les plus marquants dans ce domaine sont au choix théoriques et manquent d’éléments empiriques pour enrichir le propos, ou alors portent secondairement sur la question des origines de la vie sur Terre et n’ont qu’un impact auxiliaire, annexe. Un papier qui présente une étude s’attaquant frontalement à ce problème et qui a produit des résultats expérimentaux sur ce thème est donc une rareté à l’époque et il captera à coup sûr l’attention de lecteurs et lectrices avertis.
Enfin, il y a le nom de l’auteur, et de son laboratoire. Le prestigieux G.H. Jones Laboratory de Chicago a hébergé de nombreux excellents chimistes et sa réputation n’est plus à faire. L’auteur, lui, est un inconnu dans ce domaine. Un rapide coup d’œil aux notes de bas de page nous révèle deux choses surprenantes : Stanley L. Miller est doctorant et il publie seul ce papier dans un des journaux scientifiques généralistes les plus réputés et difficile d’accès pour les auteurs. Stanley L. Miller est doctorant et il remercie son directeur de thèse, Harold Urey, prix Nobel de chimie en 1934, dans une note de bas de page au lieu de partager la signature de cette publication avec lui, comme c’est traditionnellement le cas ! Il s’agit là vraiment d’une curiosité !
Résumons le premier faisceau d’éléments de cette enquête : ce papier émane d’un prestigieux laboratoire de chimie et apparaît dans un éminent journal scientifique. Pour autant, il traite d’un domaine très spécialisé et peu reconnu, il a été publié plus rapidement que les autres articles de cette édition et le directeur de thèse n’a pas signé le papier de son doctorant. Que faut-il donc y comprendre ? Penchons-nous maintenant sur le contenu du papier. Quelles sont les expériences et les résultats présentés ?
Le monde dans une bouteille : une expérience pour comprendre les origines de la vie sur Terre
En un mot, Stanley Miller annonce avoir reproduit, en laboratoire, les conditions physiques et chimiques de la Terre primitive. Dans ces conditions, il écrit avoir obtenu rapidement des composés chimiques organiques d’intérêt pour le vivant, ouvrant ainsi la voie à une compréhension des origines de la vie sur Terre. Il y a beaucoup d’éléments dans cette phrase qui feraient hausser les sourcils (de curiosité comme de scepticisme) de scientifiques s’intéressant un tant soit peu à ce sujet à l’époque, mais suspendons notre jugement un instant pour nous intéresser à l’expérience qui est décrite ici.
L’auteur détaille donc l’utilisation d’un montage expérimental unique et fabriqué sur mesure pour ses besoins (Figure 1A). Il s’agit d’un assemblage de verreries en pyrex, scellé sur toute sa longueur et dont la seule ouverture est reliée à une ligne sous vide permettant le transfert de gaz de manière contrôlée. Le montage est pensé pour représenter le cycle de l’eau sur Terre, de manière très simplifiée : un petit ballon contenant de l’eau liquide, représentant l’océan, est relié à un ballon plus volumineux rempli de gaz, représentant l’atmosphère. En faisant chauffer « l’océan » d’un côté et condenser par refroidissement « l’atmosphère » de l’autre, Miller simule dans ce système fermé le cycle évaporation/pluie à la surface de notre planète. Le scientifique ajoute une source d’énergie supplémentaire dans ce système : à l’aide de deux électrodes [**] et d’une bobine à induction, il peut générer sur commande des arcs électriques d’un bleu tirant sur le violet, simulant ainsi des éclairs zébrant l’atmosphère. S’appuyant sur les travaux de son directeur de thèse, Urey, sur la formation des planètes du système solaire et leurs environnements premiers [2], Miller construit un monde miniature, scellé, et réduit à l’espace d’une paillasse de laboratoire (Figure 1B). Fascinant, n’est-ce pas ?
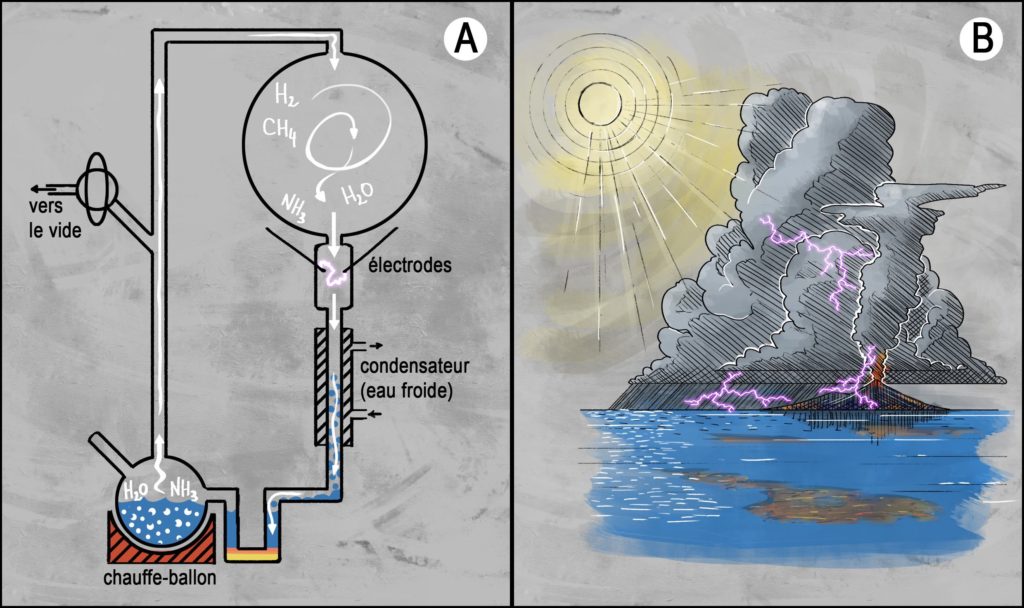
Miller souhaite tester la théorie de l’évolution chimique, qui propose un chemin (si ce n’est même le chemin [***]) menant du non-vivant au vivant [pour approfondir : voir note A]. Selon cette théorie rassemblant les connaissances scientifiques les plus actuelles de l’époque, l’origine de la vie sur Terre pourrait être décrite comme une succession d’étapes de phénomènes et réactions chimiques [3]. Lors de sa formation au sein de notre système solaire, la Terre primitive, trop chaude et inhospitalière, serait dénuée d’organismes vivants. À mesure de son refroidissement, un océan vaste et chaud ainsi qu’une atmosphère sans oxygène ni ozone, traversée par le rayonnement intense du jeune soleil, se formeraient à sa surface. Des terres seraient peut-être émergées, mais rien n’est moins sûr. La composition chimique initiale de l’océan et de l’atmosphère serait extrêmement simple ; quelques molécules petites et simples en grande concentration en seraient les ingrédients majoritaires. Au gré de phénomènes énergétiques brefs et intenses (des éclairs, des éruptions volcaniques) ou par rayonnement ultraviolet sous la lumière du pâle soleil, les composés inorganiques réagiraient entre eux. Cet apport d’énergie, sous quelque forme que ce soit, permettrait la formation puis la combinaison de molécules organiques, composées d’un assemblage de carbone, d’hydrogène, d’oxygène, et d’azote. Par une cascade d’événements chimiques, ces molécules se complexifieraient et formeraient des briques élémentaires du vivant, les composés que l’on trouve à la base de toute vie sur Terre. Le temps géologique [****] pourrait faire le reste, en concentrant et combinant avec patience des briques élémentaires durant les millions d’années qui précèdent l’émergence des premiers organismes.
C’est pour apporter une preuve expérimentale à cette théorie de l’évolution chimique que Miller réalise cette expérience. Son montage expérimental est un modèle « analogue » : il représente un monde lointain dans le temps, inaccessible et complexe, par un système plus simple, contrôlable, et analysable. Ce genre de modèle expérimental permet d’affiner notre compréhension du monde réel par répétition d’expériences en se concentrant sur une variable à la fois. En changeant progressivement les conditions de l’expérience, notre connaissance du modèle, et donc du système réel, avance. C’est une méthode qui a fait ses preuves dans l’histoire des sciences naturelles. Newton, déjà, résume cette approche dans ses Principia en 1687 : « Expliquer toute la nature est une tâche trop ardue pour un seul homme ou une seule époque. Il est plus sage de faire peu en étant sûr de soi et laisser le reste à ceux qui viendront après, que présumer de tout sans être sûr de rien » (cité dans [4]).
En ayant un contrôle fin sur la composition initiale de l’océan et la teneur de départ en gaz dans l’atmosphère, Miller espère donc pouvoir reproduire dans son laboratoire les premières étapes d’une évolution chimique de la vie.
Une méthode simple et des résultats déconcertants
En quelques paragraphes, Miller donne les détails de cette expérience de Terre primitive réduite à l’échelle d’une salle de laboratoire. Dans ce système expérimental fermé, préalablement nettoyé et mis sous vide pour en retirer tout l’air, Miller suit la recette proposée par la théorie de l’évolution chimique. Il introduit 200 mL d’eau puis des gaz : du méthane (CH4) et de l’ammoniac (NH3) en quantité égale et moitié moins de dihydrogène (H2). L’ammoniac se dissout dans l’eau, alors que le méthane et le dihydrogène restent sous forme gazeuse. L’eau est chauffée jusqu’à ébullition et les décharges de la bobine à induction sont déclenchées de manière continue pendant une semaine d’expérience. Les cycles d’évaporation et de condensation se suivent, la vapeur d’eau et les gaz réagissent sous l’action des décharges électriques, les molécules volatiles (=qui s’évaporent facilement) passent de « l’océan » à l’atmosphère et les molécules moins volatiles se concentrent dans « l’océan ». Au bout de quelques heures déjà, les électrodes se recouvrent d’une poussière sombre et fibreuse, et « l’océan » se colore de rouge profond et de jaune. À la fin de la semaine d’expérience, Miller ouvre le dispositif et récupère le liquide pour l’analyser immédiatement.
Miller s’attend à trouver quantité de molécules organiques différentes. Il s’attend à tout un bestiaire, une grande diversité mais à une faible concentration. En somme, il pense que son expérience produirait un petit peu, juste un petit peu, de tout ce qui existe dans le catalogue des molécules organiques simples. Cependant, il suit une procédure permettant d’extraire uniquement les acides aminés de la soupe organique qu’il a récupérée. En effet, les acides aminés sont les constituants des protéines, et une cible de choix pour Miller : on sait à l’époque avec certitude que les protéines sont des molécules centrales dans la biochimie du vivant. Elles sont nécessaires à une panoplie d’activités cellulaires et sont probablement les molécules dont la structure et la fonction sont les mieux comprises par les biochimistes à l’époque [5]. Trouver des acides aminés, c’est trouver l’une des briques élémentaires du vivant ! L’échantillon extrait par Miller est donc analysé par une méthode simple et directe, dont le principe théorique est source de recherches actives à l’époque : la chromatographie sur papier (Figure 2A) [6]. Cette technique repose en partie sur un principe similaire aux autotests Covid dont vous êtes peut-être familiers : la capillarité d’une bandelette test. Une goutte de solution à tester est déposée au coin d’un papier préalablement humidifié et placé à la verticale, c’est la phase stationnaire. Si on n’y touche pas, la goutte s’étalera peut-être légèrement à cause de la gravité et de sa diffusion dans la couche d’eau, puis sèchera. Mais si vous ajoutez un solvant liquide en excès en bas du papier tenu verticalement, comme le café dans un sucre, ce liquide migre d’un bout à l’autre du papier par capillarité en créant un front de migration. On parle de phase mobile (Figure 2A). Comme dans votre test Covid, le solvant emporte l’échantillon avec lui dans sa course. Cet échantillon est composé de plusieurs types de molécules qui n’ont pas toutes la même force d’adhésion au papier humide et qui, face à la force d’entraînement du liquide mobile, seront plus ou moins déplacées le long du trajet. Plus une molécule est liée au papier humide, moins elle sera déplacée par le solvant liquide. On peut de cette manière séparer physiquement, sur une feuille de papier, des composés qui étaient mélangés dans un même échantillon. La feuille de papier séchée après migration et séparation est appelée chromatogramme (Figure 2A). Un tel chromatogramme peut être comparé à des références obtenues pour des composés préalablement connus, qui ont migré dans les mêmes conditions (même solvant, même durée).
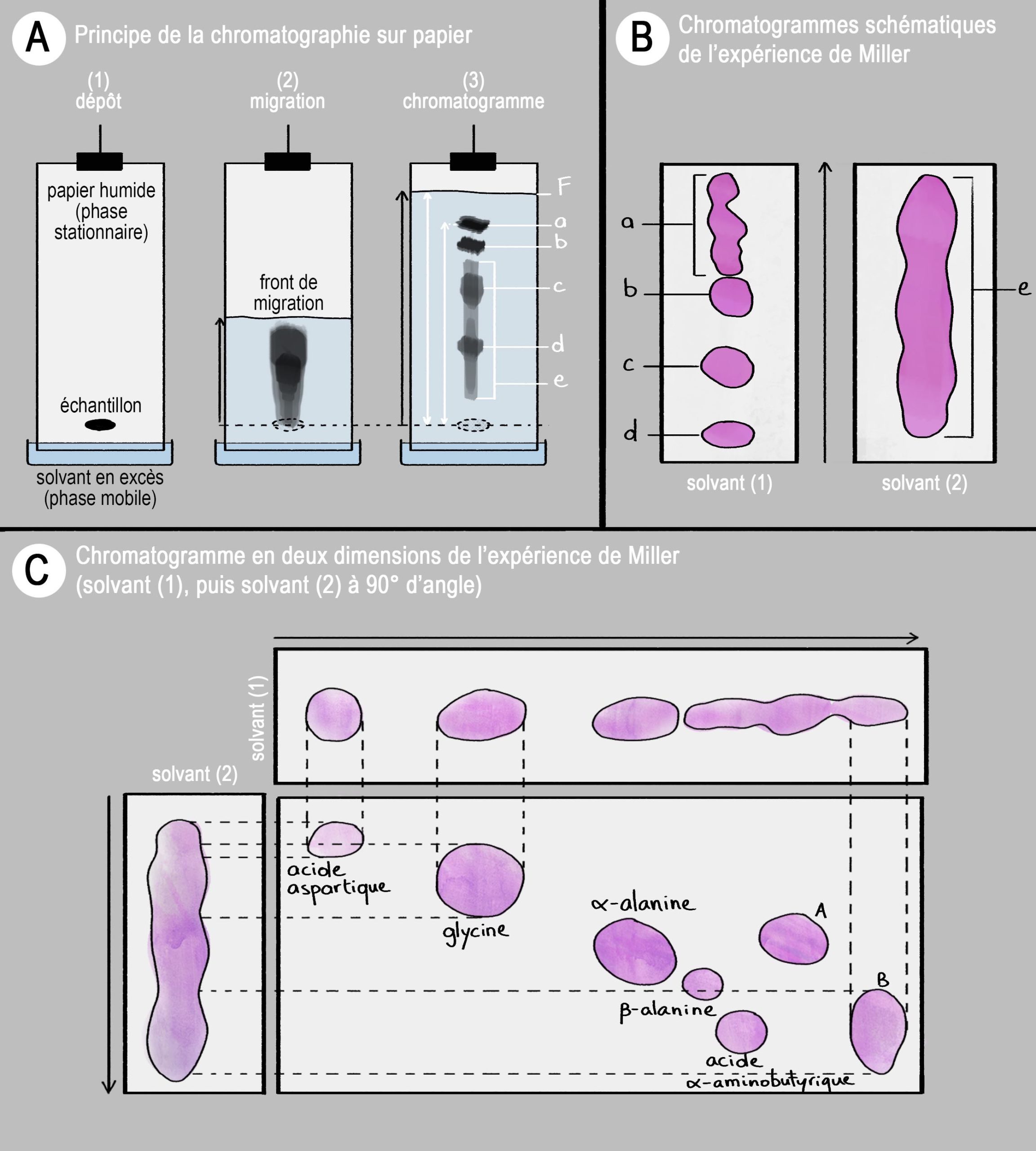
En utilisant un solvant unique, les acides aminés présents dans l’échantillon ne se séparent pas correctement mais s’étalent en une longue bande car ils ont des comportements très similaires (Figure 2B). Les forces qui les attirent dans le papier humide ou le liquide mobile sont proches. C’est un problème car sans chromatogramme montrant des tâches précises et bien définies, il est impossible de justifier de la présence des acides aminés tant recherchés ! Miller ajoute donc une étape à cette méthode. Il choisit avec précaution non pas un, mais deux solvants liquides : c’est la chromatographie sur papier en deux dimensions. Utilisés séparément, ces solvants ne donnent pas de bons résultats de séparation (Figure 2B). Cependant, après la première migration le long de la feuille de papier, celle-ci peut être tournée de 90° afin de procéder à une deuxième migration avec le deuxième solvant. Cette méthode permet de séparer au mieux des molécules aux comportements assez proches, comme les acides aminés. À la suite de cette deuxième migration, qui dure 12 à 48 heures, Miller développe le papier en y appliquant un agent colorant et découvre sept tâches (Figure 2C). Miller les compare à celles obtenues sur des chromatogrammes d’acides aminés purs et connus. Il identifie les tâches résultant de son expérience comme étant bel et bien des acides aminés ! Mais là où il attendait une constellation de points représentant une grande partie des acides aminés connus (plus de 500), il n’en découvre que sept…
Alors ? Cette expérience est-elle un échec ? Cette tentative de reproduire les conditions de la Terre primitive n’a produit que peu de composés organiques… Est-ce suffisant pour justifier la publication de cet article ?
Le résultat qu’il manquait pour confirmer les suspicions
La théorie de l’évolution chimique, c’est-à-dire l’idée que l’origine de la vie résulte de la transformation lente et progressive de la matière dans un environnement favorable, rencontre un grand succès parmi les scientifiques s’intéressant aux origines de la vie. Elle s’est affinée à mesure que les connaissances des origines de la Terre, du système solaire, et de la biochimie se sont accumulées, entre les années 1920 et 1950 [3]. L’ensemble des étapes proposées dans cette théorie sont interdépendantes. On ne peut passer à une étape qu’en ayant trouvé la solution à la précédente. Mais tout ceci ne repose sur aucune preuve empirique et, au début des années 1950, il devient crucial d’amasser des résultats expérimentaux qui pourraient la confirmer.
Stanley Miller n’est pas le seul chercheur à s’intéresser à la théorie de l’évolution chimique. En 1951, l’équipe californienne de Melvin Calvin publie un court papier, avant-gardiste, mais dont l’expérience décrite échoue à produire des briques élémentaires du vivant [7] [pour approfondir : voir note B]. Il manque donc toujours une expérience originale comme preuve de cette théorie… Et c’est précisément ce qu’apporte l’expérience de Miller. Même si toutes les molécules importantes ne sont pas produites dans cette expérience unique, c’est un point de départ essentiel pour montrer la possibilité de l’évolution chimique ! Miller confirme l’hypothèse que sur la Terre primitive, de la matière organique se concentrait dans les océans à partir de réactions chimiques de quatre composés très simples et abondants. À partir de ces briques élémentaires, toutes les réactions de chimie organique semblaient possibles et l’expérience de Miller ouvrait la porte à une évolution chimique lente et progressive permettant, par étapes, de passer du non-vivant au vivant.
Le doute reste permis
Vous comprenez que ce résultat vient bousculer des années de tentatives infructueuses, de frustrations et une incapacité des scientifiques à confirmer une théorie centrale à la réflexion sur les origines de la vie. Ce papier est donc extrêmement important, mais pour autant, on est en droit de se demander si Miller ne manquerait pas de preuves pour confirmer son interprétation de cette expérience. N’y aurait-il pas de quoi faire douter raisonnablement la communauté scientifique ?
En effet, même si la chromatographie sur papier est une méthode simple, elle peut être considérée comme une démonstration insuffisante de la synthèse d’acides aminés lors de l’expérience… L’expérience semble avoir produit un certain nombre de composés inconnus, et la procédure pour extraire puis analyser les acides aminés présents dans l’échantillon est longue et possède de nombreuses étapes. Des questions se posent : comment vérifier que les étapes de préparation de l’échantillon n’introduisent pas un biais expérimental, c’est-à-dire une transformation systématique de l’échantillon à cause de la méthode elle-même ? Auquel cas la présence d’acides aminés serait due à la méthode d’analyse et pas à l’expérience… Est-ce que la présence dans l’échantillon analysé d’un composé (ou un mélange de composés) différent des acides aminés pourrait conduire à l’obtention du même chromatogramme ? On parlerait alors d’un artefact sur le chromatogramme… Apporter la preuve que ces résultats ne sont ni des artefacts ni des biais expérimentaux sera le point sur lequel se focalisera toute l’argumentation de Miller dans les années qui suivent [8, 9] [pour approfondir : voir note B].
Mais, pour les besoins de cette publication, il y a un problème que Miller doit nécessairement aborder : la contamination. Depuis les travaux de Pasteur ayant réfuté l’hypothèse de la génération spontanée [*****], on sait que le vivant est capable de contaminer les expériences des scientifiques, qui doivent faire preuve de précaution s’ils souhaitent travailler dans des conditions parfaitement stériles. Dans ces expériences complexes, tout l’enjeu est là. Le vivant a-t-il contaminé l’expérience de Miller ? Les acides aminés ne pourraient-ils pas tout simplement être les résidus de microorganismes qui auraient été introduits dans le montage expérimental avant l’expérience ou dans l’échantillon lors de sa manipulation pour analyse ?
Sachant l’importance d’une telle découverte, et la propension du vivant à contaminer les échantillons, Miller apporte donc dans ce papier quelques détails sur les précautions prises pour éviter la contamination. Tout d’abord, il apporte un soin tout particulier au nettoyage du montage expérimental. Il note ensuite que l’ébullition constante de l’eau durant toute la durée de l’expérience, puis l’utilisation de composés toxiques pour le vivant lors de l’extraction de l’échantillon (des sels de mercure) réduisent les risques de contamination pendant et après l’expérience. De plus, la relative « pauvreté » de l’échantillon en acides aminés (seulement quelques acides aminés détectés par rapport aux 20 acides aminés qui composent les protéines des organismes vivants) a au moins un avantage : le produit analysé a peu de chances de provenir d’une contamination par des organismes vivants.
Ce qui peut être vu de prime abord, par l’œil averti que vous êtes en train de développer, comme une faiblesse méthodologique de l’auteur, se justifie en fait partiellement par l’importance fondamentale de ce résultat. Cela excuse temporairement le manque de preuves apportées par empressement à publier. Mais c’est un choix très subjectif du jeune doctorant et de son directeur de thèse. Miller est conscient de ce problème majeur et passera les années suivantes à répéter son expérience, améliorer les procédés d’analyse, et à décrire les réactions chimiques se déroulant dans son modèle.
Une expérience sans garantie, une compétition qui fait rage
Une telle découverte peut tenir de la chance, du contexte et découle souvent de tout un tas de causes externes au seul « génie » des scientifiques. Comme nous l’avons vu tout au long de cet article, les conditions sont réunies pour que l’expérience de Miller soit un succès. La science est construite sur la base de connaissances collectives et de collaborations.
Rappelons qu’au début des années 1950, l’étude des origines de la vie sur Terre n’est pas un domaine de recherche à part entière. C’est souvent par curiosité ou amusement que des scientifiques dont la carrière est généralement bien avancée mènent en parallèle de leur recherche un travail, souvent théorique et synthétique, sur ce sujet. La question des origines du vivant est certes fascinante, mais elle est considérée comme annexe, probablement aussi parce qu’il est difficile de s’attaquer à ce vaste problème interdisciplinaire. Alors, lorsque Stanley Miller demande à son directeur de thèse, Harold Urey, de travailler sur ce sujet, celui-ci tente d’abord de le décourager. Après discussion, les deux chercheurs arrivent à un compromis : Miller n’a qu’un an pour obtenir des résultats expérimentaux probants. Dans le cas où son expérience ne produirait pas de composés organiques d’intérêt pour le vivant, Miller devrait bifurquer sur un autre sujet de thèse, moins risqué pour sa carrière [4].
Lorsque le jeune doctorant présente ses résultats à son directeur de thèse, celui-ci devine l’impact que cette découverte pourrait avoir sur la science. Il propose à Stanley Miller de publier vite et de publier seul [10]. Pour ne pas faire de l’ombre à son doctorant par sa notoriété, le directeur de thèse décide de faire retirer son nom du papier, ce qui est pour le moins un geste rare. Il reconnaît cependant qu’une telle découverte serait difficilement acceptée si elle provenait simplement d’un doctorant. La hiérarchie a, par la structure même de la recherche universitaire, un poids certain en science, et Urey use de son autorité pour que le papier soit publié le plus rapidement possible. Même si publier un papier n’est pas simple [pour approfondir : voir note C], et que publier des résultats préliminaires est risqué, les deux scientifiques décident de suivre cette voie car il se dit dans les couloirs de l’université que d’autres équipes sont sur le point de faire la même découverte…
On voit donc que, sous couvert de simplicité et de sobriété, ce papier repose sur un savant mélange de nouveauté, de concision, de chance et d’argumentation pour permettre à l’auteur de présenter sa découverte tout en se laissant le temps d’y apporter plus de preuve par la suite. Un vrai exemple de communication scientifique qui laisse une marque.
L’émergence d’une nouvelle discipline
Pour la première fois, une expérience simule de manière complexe les conditions environnementales de la Terre primitive. De plus, ses résultats montrent à quel point ces conditions sont favorables à la production des molécules du vivant, avec une diversité restreinte et une abondance élevée. L’étude des origines de la vie était jusqu’alors considérée comme une discipline accessoire de la chimie et de la biologie. Soudainement, à la suite de ce papier, elle se voit accorder une légitimité toute nouvelle. Stanley Miller donne ses lettres de noblesse aux simulations en laboratoire des conditions de la Terre primitive. Il fait entrer l’étude des origines de la vie dans le domaine des sciences expérimentales modernes et de ce fait, crée la discipline de la chimie prébiotique, la chimie d’avant la vie [pour approfondir : voir note D].
Cette découverte aura des échos bien au-delà des sphères érudites intéressées par les origines de la vie sur Terre. Le bruit court dans les journaux grand public qu’on aurait trouvé la réponse à la question de la « création » de la vie. Dans un contexte de guerre froide, cette idée est étonnamment vite acceptée dans la société conservatrice américaine car le progrès scientifique est un des nœuds de la compétition globale que se livrent les deux blocs [4]. Le contexte, encore une fois, est favorable à l’apparition d’une discipline comme la chimie prébiotique. L’expérience de Miller deviendra une expérience classique, célébrée au même titre que celles de Pasteur [*****] ou Mendel [******].
En 1953, cette expérience convainc de nombreux chimistes et biologistes que l’émergence de la vie est probablement un phénomène commun dans l’univers et s’interrogent : est-il possible que nous ne soyons pas seuls dans l’Univers ? Cette question, cependant, reste en suspens. Et aujourd’hui, inlassablement, des robots parcourent la surface d’autres planètes et tentent, encore et toujours, d’y apporter une réponse définitive.
Éléments pour approfondir
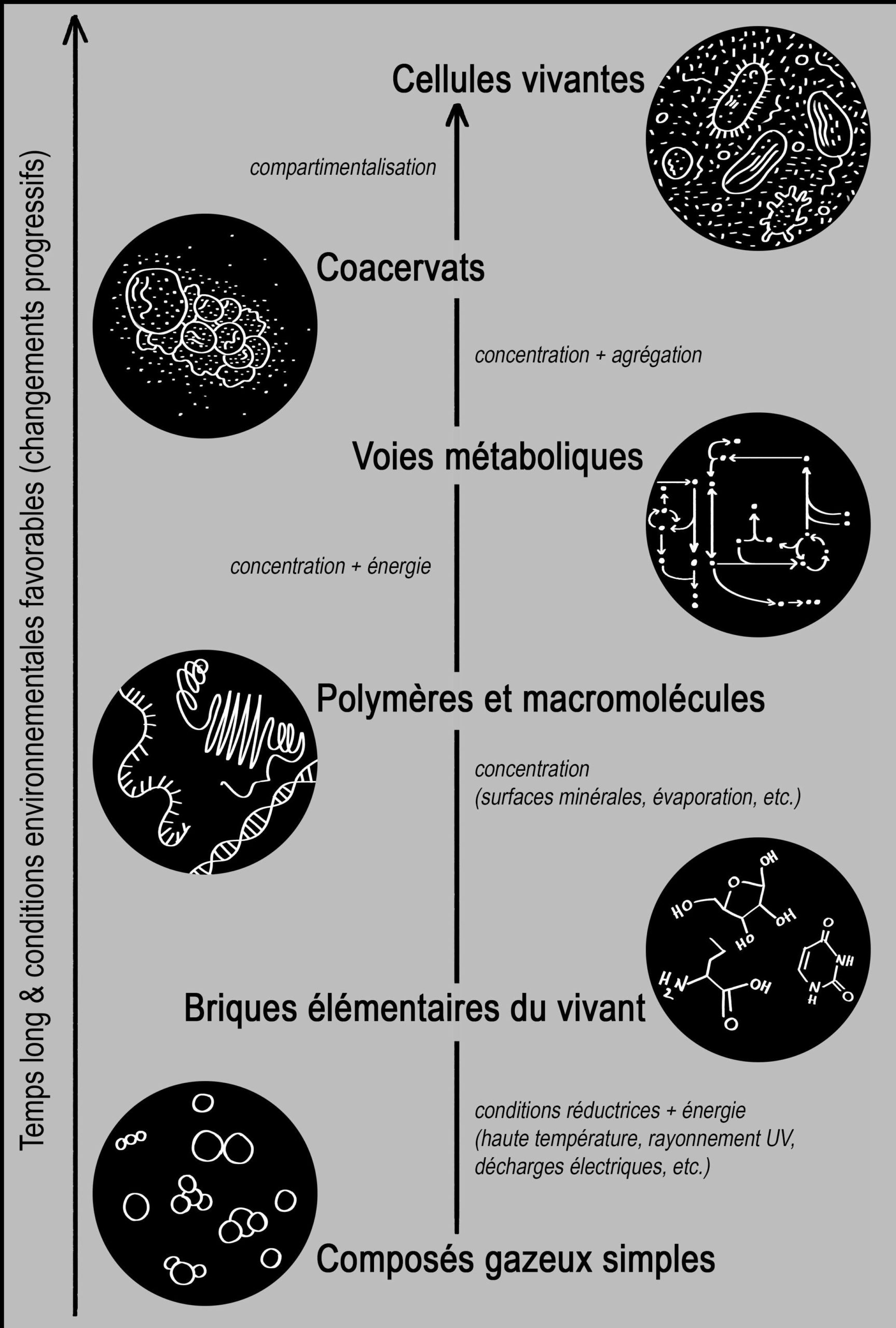
La théorie de l’évolution chimique. En 1953, Stanley Miller s’intéresse à la première étape de la théorie de l’évolution chimique : produire des briques élémentaires du vivant à partir de composés prébiotiques simples et abondants sur la Terre primitive. Il s’appuie sur une version de la théorie de l’évolution chimique qui est une synthèse des travaux de Alexander Oparin, John B.S. Haldane, John D. Bernal, et Harold C. Urey [3]. En regroupant des données de géologie, d’astronomie, de biologie et de chimie, ces auteurs ont produit une théorie d’évolution graduelle de la matière inanimée jusqu’à la formation des premières cellules vivantes. Ils font l’hypothèse que les conditions environnementales primordiales étaient différentes d’aujourd’hui (flux d’énergie, conditions d’oxydation, température, etc.). Le temps long (jusqu’à 700 millions d’années) aurait permis par « le hasard et la nécessité », comme dit Jacques Monod, l’émergence de la vie sur Terre. Cette théorie importante, que rien n’est venu invalider jusqu’à présent, peut être représentée par une suite d’étapes clés, comme dans la Figure 3 ci-dessous. Cette représentation linéaire, bien que simpliste pour symboliser une évolution qui par nature est foisonnante, est extrêmement utile pour les astrobiologistes. Elle permet de tester chaque étape du processus de manière indépendante et trouver quelles sont les conditions favorables pour passer d’une étape à l’autre. Il s’agit de trouver des ponts, des clés, des voies qui permettent d’aller du plus simple au plus complexe.
Quelques définitions des termes présents sur la Figure 3. Des conditions réductrices sont des conditions environnementales (physiques et chimiques) qui permettent de maintenir un milieu pauvre en oxygène et molécules oxydantes (capables d’oxyder la matière, c’est-à-dire de provoquer la perte d’électrons de cette matière et de récupérer ces électrons). Une macromolécule est une très grosse molécule ; elle est souvent composée d’un assemblage de plus petites molécules, comme les briques élémentaires du vivant par exemple dans le cas des origines de la vie. Un polymère est une macromolécule qui a pour particularité de posséder une structure que l’on peut décrire simplement comme la répétition d’un motif, le monomère, lié par des liaisons fortes. Le métabolisme désigne la totalité des réactions chimiques se déroulant à l’intérieur des cellules vivantes ; il existe des réactions chimiques essentielles à la vie, qui se déroulent par étapes successives et interconnectées : on parle dans ce cas de voies métaboliques. Un coacervat est un agrégat de molécules qui se stabilise spontanément sous forme de gouttelettes dans un autre liquide ; ici on envisage que certaines macromolécules peu stables dans l’eau se regroupent pour former des sortes de gels dynamiques : des gouttelettes fondamentalement différentes de leur milieu, qui échangent avec lui, grossissent, se scindent, et peut-être même se reproduisent (voir [3] pour une explication détaillée et précise de ces étapes).
Un peu de chimie prébiotique. Stanley Miller n’est pas le seul chercheur à s’intéresser à la théorie de l’évolution chimique. En 1951, l’équipe californienne de Melvin Calvin publie un court papier avant-gardiste. Cette équipe a tenté de reproduire l’étape de fixation du carbone, c’est-à-dire la transformation du CO2 en matière organique, dans des conditions primitives. Calvin est l’autorité en matière de fixation biologique du carbone, dont une manifestation est une réaction chimique que vous connaissez peut-être, sous le nom de photosynthèse. Calvin et son équipe pensent que, à la manière de la photosynthèse végétale, la vie émerge par la voie de fixation du CO2 en carbone organique réduit. Dans cette expérience, qui inspirera sûrement Miller, l’équipe prouve bien que le CO2 peut être réduit en carbone organique (acide formique (CH2O2)) dans des conditions spécifiques et en l’absence de vie. Mais l’expérience reste anecdotique car les molécules formées ne sont pas des briques élémentaires du vivant et, bien que le résultat soit positif, il manque d’impacts. « La question des conditions menant à l’émergence de la vie à la surface de la Terre est toujours un sujet limité à la spéculation théorique. Cette spéculation a une plus grande chance d’approcher la vérité quand elle inclut et est basée sur la grande variété des faits scientifiques établis. » écrivent les auteurs… Il manque donc toujours une expérience originale comme preuve de cette théorie… Et c’est précisément ce qu’apporte l’expérience de Miller. Une preuve expérimentale établie qui confirme l’idée d’une évolution chimique.
De plus, ces premiers résultats probants font le lien entre la théorie des origines de la vie (l’évolution chimique) et celle détaillant l’environnement terrestre primitif (la théorie de formation de planètes de Urey, le directeur de thèse de Miller). L’expérience de Miller montre que les conditions de la Terre primitive, telles que pensées par les scientifiques à l’époque, sont favorables à la formation de molécules nécessaires à toute forme de vie aujourd’hui et par extension nécessaires à l’apparition du vivant. Il faut dire que, si les expériences précédentes n’ont pas apporté de résultats positifs jusque-là, c’est au moins en partie dû à leur complexité. Reproduire un environnement naturel, c’est mener une expérience dont on ne contrôle que très peu de paramètres. On parle souvent de système complexe : un ensemble constitué de nombreux éléments en interactions les uns avec les autres, de telle sorte qu’une prédiction sur son devenir est très difficile à faire. Contrairement à la logique propre aux chimistes organiques de son temps, visant la synthèse de composés purs avec le meilleur rendement possible, Miller ne cherche pas à maximiser la synthèse des acides aminés, mais à imiter des réactions chimiques peu efficaces, qui produisent de nombreux composés dans les environnements naturels. Les possibilités et les combinaisons sont nombreuses, très nombreuses. La question se pose : parmi toutes les molécules qui pourront être produites, lesquelles chercherait-on à identifier en priorité ? C’est un grand défi auquel s’attache la chimie analytique, qui a fait des progrès remarquables dont Miller bénéficie au moment de son expérience.
Miller ne pouvant rien prédire des résultats et donc des composés chimiques qui seront produits, il doit faire un choix et se focaliser sur un type de molécules synthétisées qui permettrait à coup sûr de confirmer son hypothèse que l’environnement de la Terre primitive est favorable à l’émergence de molécules organiques d’intérêt pour le vivant. Son choix se porte sur les acides aminés comme nous l’avons vu plus haut. Il lui faut donc prélever l’échantillon, séparer les acides aminés sans les détruire (s’ils sont présents) du reste des molécules en solution, utiliser une méthode de détection ciblée et fiable (dont le résultat est sans équivoque). L’expérience de Miller a été maintes fois répétée depuis, en changeant le montage expérimental lui-même ou en modifiant les conditions initiales de l’expérience. On sait aujourd’hui décrire avec précision quelles sont les réactions abiotiques (=sans aide du vivant) qui s’y déroulent.
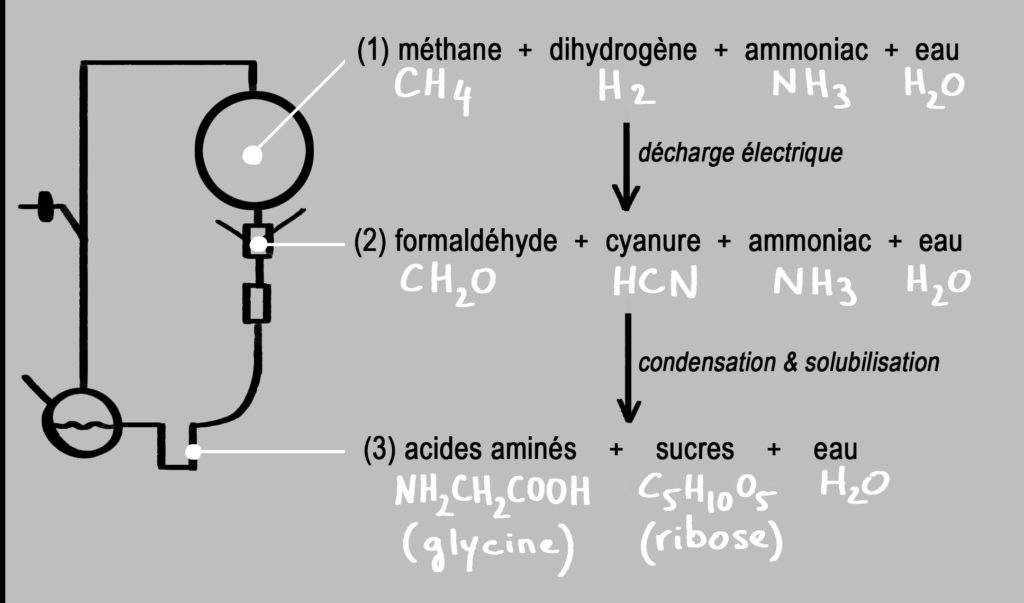
La Figure 4 ci-dessous montre quelques détails de ces réactions chimiques qui seront décrites plus tard (voir par exemple [11]). La particularité de ces réactions est qu’elles sont spatialisées : elles dépendent de conditions différentes et ne peuvent se produire au même endroit dans le montage expérimental. (1) Les gaz se mélangent dans le grand ballon, puis une décharge électrique (2) permet la production de composés intermédiaires très importants en chimie prébiotique : le formaldéhyde (formol sous forme liquide) et le cyanure d’hydrogène (acide cyanhydrique). C’est ensuite la condensation de la vapeur d’eau et la solubilisation de ces molécules qui déclenchent la formation d’acides aminés (synthèse de Strecker) et de sucres (synthèse de Butlerov). Pour produire les briques élémentaires du vivant, une séquence de réactions est nécessaire et les produits d’une réaction doivent passer par un changement de conditions afin de procéder à la réaction suivante.
Publier n’est pas chose aisée. En 1953, les papiers sont encore manuscrits, c’est-à-dire écrits à la main ! Imaginez un peu ! Le processus de publication dépend lui aussi de correspondances manuscrites. Cela prend énormément de temps et de ressources. Soumettre un papier en vue de sa publication n’est donc ni anodin ni trivial. Il faut être certain de la validité et de la portée de ses résultats et éviter au maximum le risque de voir son manuscrit rejeté pour cause de manque de preuves ou d’un impact jugé trop faible par le comité de lecture du journal, qui suit une ligne éditoriale souvent focalisée sur le facteur de nouveauté d’une découverte. Pour Stanley Miller, publier un résultat qui est encore préliminaire, alors que les analyses sont incomplètes et qu’il ne comprend pas toutes les subtilités de son expérience, est risqué. Mais c’est aussi nécessaire s’il veut justifier de la « paternité » de son travail à une époque où la recherche des origines de la vie attire de nombreux scientifiques de renom.
70 ans d’astrobiologie. Une courte frise chronologique. L’expérience de Miller a été publiée il y a 70 ans. Depuis, les découvertes et les avancées spectaculaires se sont accumulées [3, 4, 10, 12, 13]. La place de l’être humain dans l’Univers a maintes fois été remise en perspectives. L’astrobiologie, dans sa quête scientifique (toujours active) de nos origines, est également propice à la réflexion philosophique. Que sommes-nous, dans ce vaste univers ? Où choisissons-nous d’aller ? La Figure 5 présentant quelques-uns des événements qui ont été déterminants dans la construction de l’astrobiologie en tant que discipline scientifique vous donnera peut-être envie d’en savoir plus sur le sujet !

[*] Sommaire de l’édition du 15 mai 1953 du journal Science : https://www.jstor.org/stable/i298369
[**] Les électrodes sont en contact direct avec le milieu expérimental. Stanley Miller observe d’ailleurs un dépôt de filaments sombres sur leur surface au cours de l’expérience. Par la suite, en développant de nouveaux montages expérimentaux produisant les mêmes résultats et ne possédant pas d’électrodes, Miller prouve que ni le matériau constitutif des électrodes ni leur surface n’ont d’influence sur le résultat de cette expérience.
[***] L’évolution chimique ne répond pas à toutes les questions sur les origines de la vie. Y a-t-il une seule façon de passer du non-vivant au vivant ? En d’autres termes, la vie se produit-elle « facilement » ? Les étapes proposées dans le cadre de l’évolution chimique n’ont pas nécessairement une solution unique. Il peut exister plusieurs manières de résoudre chaque étape indépendamment. Les chercheurs et chercheuses s’interrogent alors, car si les solutions étaient nombreuses, la vie serait probablement abondante dans l’Univers. Sur Terre, le chemin des origines de la vie serait alors la combinaison des solutions les plus favorables au regard du contexte et de l’histoire de la planète et du système solaire. Rien d’unique à cela, la vie apparaît facilement car il y a beaucoup d’options pour qu’elle apparaisse. Si la solution était unique, la vie serait probablement peu abondante dans l’Univers. Sur Terre, il aurait fallu que les conditions favorables à l’évolution chimique s’enchaînent parfaitement dans l’espace et dans le temps afin qu’émergent les premiers organismes vivants. L’histoire de la Terre suivrait alors un chemin très rare, voire unique, qui serait le seul ou presque à permettre l’apparition du vivant. Ce débat reste ouvert. La réponse à ce questionnement conditionne la possible abondance du vivant dans l’Univers et donc nos chances de découvrir de la vie (ou des traces de vie passée) ailleurs.
[****] À partir du début des années 1900, les scientifiques repoussent l’âge de la Terre de plusieurs milliers, plusieurs millions, puis plusieurs milliards d’années. Quand la théorie de l’évolution chimique prend forme, les scientifiques sont conscients de l’immense durée qui nous sépare de nos origines. En laboratoire, on ne peut pas reproduire facilement des processus qui évoluent sur un temps très long. De ce fait, les scientifiques proposent que certaines étapes de l’évolution chimique ne sont pas réalisables en laboratoire mais au cours de millions d’années. Dans cette théorie, le temps très long de l’histoire géologique de notre planète est donc essentiel à l’origine de la vie.
[*****] En 1864, à l’issue de trois années d’expérimentation, Louis Pasteur apporte la preuve que la présence et la croissance de « germes » dans des contenants supposés propres étaient dues à une contamination par des spores ou des microbes. En prenant des précautions expérimentales qui sont aujourd’hui enseignées et utilisées dans de nombreuses expériences, il parvint à garder un contenant stérile et prouva qu’il n’y avait pas de génération spontanée de la vie à l’échelle de l’observation humaine.
[******] En 1866, Gregor Mendel, moine et botaniste, étudie la transmission de caractères visibles chez les végétaux. Il utilise l’outil statistique pour suivre les croisements de pois de formes ou de couleurs différentes. De ses travaux émanent trois lois qui furent les fondements de la génétique moderne.
Pour aller plus loin :
- Meunier A., La naissance de la Terre. De sa formation à l’apparition de la Vie. Dunod, 2014. ISBN : 978-2-10-070682-2 [Livre]
- Le site de la Société Française d’Exobiologie et son parcours pédagogique interdisciplinaire [Ressources pédagogiques]
[1] Jones Laboratory, The Atomic Heritage Foundation, 2019 [Site web, consulté le 02/02/23 ; en anglais]
[2] Urey H.C., On the Early Chemical History of the Earth and the Origin of Life. PNAS, 1952. DOI : 10.1073/pnas.38.4.351 [Publication scientifique]
[3] Raulin Cerceau F., Les origines de la vie. Histoire des idées. Ellipses, 2009. ISBN : 978-2-7298-5171-2 [Livre]
[4] Bill M. & Cleaves II H.J., A Brief History of Creation. Norton, 2016. ISBN : 978-0-393-08355-2 [Livre]
[5] Corey R.B., X-Ray Studies of Amino Acids and Peptides. Advances in Protein Chemistry, 1948. DOI : 10.1016/S0065-3233(08)60010-8 [Chapitre de livre de science]
[6] Clegg D.L., Paper Chromatography. Journal of the American Chemical Society, 1950. DOI : 10.1021/ac60037a014 [Review]
[7] Garrison W.M., et al, Reduction of Carbon Dioxide in Aqueous Solutions by Ionizing Radiation. Science, 1951. DOI : 10.1126/science.114.2964.416 [Publication scientifique]
[8] Miller S.L., Production of Some Organic Compounds under Possible Primitive Earth Conditions. Journal of the American Chemical Society, 1955. DOI : 10.1021/ja01614a001 [Publication scientifique]
[9] Miller S.L. & Urey H.C., Organic Compound Synthesis on the Primitive Earth. Science, 1959. DOI : 10.1126/science.130.3370.245 [Publication scientifique]
[10] Lazcano A. & Bada J.L., The 1953 Stanley L. Miller Experiment: Fifty Years of Prebiotic Organic Chemistry. Origins of life and evolution of the biosphere, 2003. DOI : 10.1023/A:1024807125069 [Review]
[11] Bada J.L., New insights into prebiotic chemistry from Stanley Miller’s spark discharge experiments. Chemical Society Reviews, 2013. DOI : 10.1039/C3CS35433D [Review]
[12] NASA Ames – NASA Searches for Life from the Moon in Recently Rediscovered Historic Footage. [Site web ; en anglais]
[13] WHOI – 1977 – Astounding discoveries. [Site web, consulté le 02/02/23 ; en anglais]