Chargement de l'article...
Écriture : Fanny Grisetto
Relecture scientifique : Estelle Nakul et Prany Wantzen
Relecture de forme : Alexandre Fauquette et Audrey Denizot
Temps de lecture : environ 10 minutes.
Thématiques : Neurosciences cognitives (Sciences cognitives)
Publication originale : Scoville, W. B. & Milner, B., Loss of recent memory after bilateral hippocampal lesions. Journal of neurology, neurosurgery, and psychiatry, 1957. DOI : 10.1136/jnnp.20.1.11.

En 1953, le patient H.M. est opéré par le chirurgien William Beecher Scoville en raison de violentes crises d’épilepsie qui le handicapent au quotidien. Au cours de cette opération, une structure cérébrale, l’hippocampe, est lésée. Peu de temps après l’opération, l’équipe médicale observe chez ce patient une perte de mémoire massive. Le patient H.M. est ainsi devenu un cas d’école dans l’étude du lien entre l’hippocampe et les fonctions mnésiques.
Notre cerveau est le siège de nombreuses capacités cognitives que l’on utilise au quotidien, telles que l’attention, la perception ou bien le langage, et qui font de nous qui nous sommes. En particulier, la mémoire est une fonction cognitive centrale pour apprendre, retenir le contenu d’une conversation et se souvenir de certains épisodes de notre vie, construisant ainsi notre socle de connaissances, compétences et même, notre identité. La mémoire humaine est complexe et organisée en différentes sous-catégories. Pour mieux comprendre son fonctionnement et ses dysfonctionnements, tels que dans la maladie d’Alzheimer, les chercheuses et les chercheurs étudient depuis des décennies le lien entre le fonctionnement du cerveau et nos capacités mnésiques. Le cas clinique du patient H.M. représente une étape clé de ce pan de la recherche, ayant permis de percer à jour le rôle d’une structure cérébrale particulièrement importante pour la mémoire humaine : l’hippocampe.
Qui est le patient H.M. ?
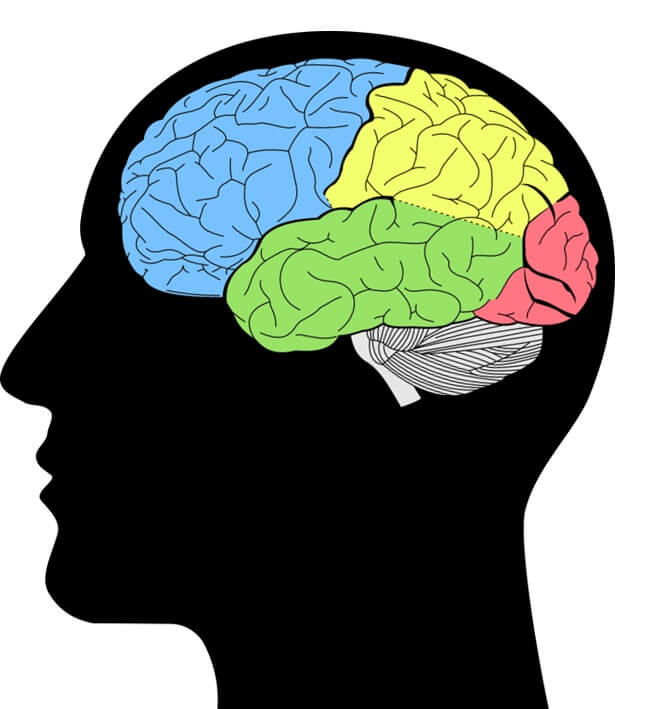
En 1953, Henry Molaison (H.M.) est un jeune homme de 27 ans, souffrant d’épilepsie [*] depuis ses 10 ans. Malgré la prise de traitements médicamenteux importants, ses crises épileptiques sont de plus en plus violentes, fréquentes et le handicapent au quotidien. En dernier recours, William B. Scoville, un neurochirurgien, lui propose une opération chirurgicale importante ayant pour objectif de réduire la sévérité de son épilepsie. Cette opération, que l’on appelle ablation, consiste à enlever une partie de la zone du cerveau considérée comme responsable des crises, qui se situe au niveau du lobe temporal (Figure 1, zone verte). Cette ablation du lobe temporal a été effectuée à de nombreuses reprises sur des patients psychotiques [**]. C’est cependant la première fois que cette opération est utilisée pour traiter l’épilepsie. Les résultats de cette opération pratiquée sur le patient H.M. sont illustrés dans la Figure 2.
Après l’opération réalisée en 1953, les médecins observent chez le patient H.M. une amélioration de son état épileptique. Ses crises sont plus espacées dans le temps et sont également moins violentes. L’entourage du patient H.M. ne remarque pas de différences de personnalité, ni d’intelligence malgré l’ablation massive qui a été opérée sur son cerveau. Cependant, le patient H.M. présente de profonds troubles de la mémoire : il est incapable de retenir les noms des membres du personnel de l’hôpital, ni même de simplement les reconnaître alors qu’il les côtoie quotidiennement !
Scoville s’interroge alors sur le lien potentiel entre l’opération réalisée et les troubles mnésiques observés chez son patient. Avec l’aide de Brenda Milner, une neuropsychologue, ils décident d’évaluer et de comparer les capacités mnésiques de plusieurs patients ayant subi une ablation du lobe temporal, dont le patient H.M. Ils publient leurs résultats en 1957 dans un article intitulé « Perte de la mémoire à court terme après des lésions hippocampiques bilatérales ». Dans cette publication, Scoville et Milner cherchent en effet à comprendre si l’on peut associer une lésion cérébrale spécifique (ici, la lésion du lobe temporal) à certaines conséquences cognitives (ici, les troubles de la mémoire). Il s’agit d’une étude lésionnelle, l’un des fondements des neurosciences cognitives. En effet, si la lésion d’une zone du cerveau induit le dysfonctionnement d’une capacité cognitive, alors cette région cérébrale était importante (voire nécessaire) au bon fonctionnement de celle-ci ! L’étude de patients atteints de lésions cérébrales est ainsi l’une des portes d’entrée qu’utilisent les chercheuses et chercheurs pour mieux comprendre l’organisation de la cognition humaine. En étudiant l’impact d’une lésion, d’une ablation ou de la stimulation électrique d’une zone cérébrale sur le fonctionnement d’une capacité cognitive spécifique (mémoire, inhibition, perception, etc.), les scientifiques parviennent à associer certaines structures à certaines fonctions cognitives. Au fil des recherches et des études de cas, comme celle du patient H.M., cette démarche scientifique permet de dévoiler les liens intimes entre cerveau, cognition et comportement.
En comparant les capacités mnésiques des différents patients ayant subi une ablation du lobe temporal, Scoville et Milner espèrent donc comprendre d’où proviennent les troubles mnésiques du patient H.M.
Quel est le lien entre le lobe temporal et la mémoire humaine ?
Pour réaliser leur étude, Scoville et Milner rencontrent dix patients, dont le patient H.M. Ces patients ont tous subi une ablation du lobe temporal, plus ou moins étendue, causant des lésions plus ou moins importantes de la zone hippocampique. Pour certains patients, dont le patient H.M., l’hippocampe est totalement lésé. D’autres patients ont une lésion hippocampique partielle, voire aucune lésion hippocampique. Lors de sa rencontre avec les patients, Brenda Milner évalue leurs capacités mnésiques au travers de tests standardisés et étalonnés [***].
Scoville et Milner observent que lorsque l’hippocampe est intact, la mémoire des patients n’est pas perturbée. Des déficits mnésiques, donc des performances significativement plus faibles que la moyenne aux tests standardisés, ne sont trouvés que chez des patients pour lesquels l’opération a lésé l’hippocampe. De plus, ils observent que plus l’hippocampe est lésé (pour les ablations les plus massives comme celle opérée sur le patient H.M.), plus les difficultés en mémoire sont importantes. Les troubles massifs de la mémoire du patient H.M. sont notamment caractérisés par une amnésie antérograde : il est incapable de créer de nouveaux souvenirs, ni d’apprendre de nouvelles informations (Figure 3, droite).
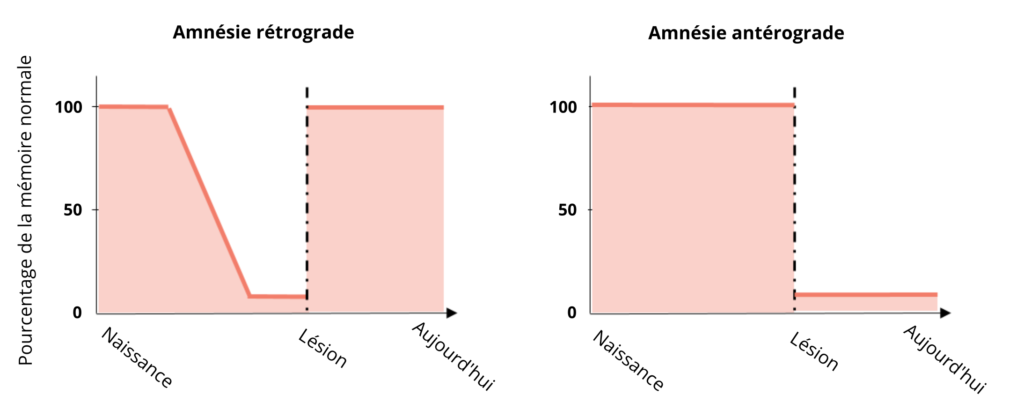
À mesure que les tests s’enchaînent, il n’est plus capable de se rappeler, ou même de reconnaître, les tests déjà réalisés. S’il est capable de retenir pendant quelques minutes une série de trois chiffres ou une paire de mots, le souvenir de ces éléments disparaît dès qu’un événement perturbe son attention sur la tâche. Sa mémoire est très fragile : les informations ne sont pas stockées à long terme. Dans la vie quotidienne, ce trouble explique pourquoi le patient H.M. ne peut pas retenir la nouvelle adresse de son domicile, ni retenir les noms des membres du personnel hospitalier, ni même connaître son âge réel ! Il peut également lire le même journal jour après jour et y redécouvrir l’intégralité des articles avec surprise… Enfin, malgré le fait que ses souvenirs les plus anciens, comme ceux de son enfance, restent intacts, le patient H.M. présente également une amnésie rétrograde partielle : certains événements de sa vie pré-opératoire semblent avoir été effacés (Figure 3, gauche). Il a, par exemple, oublié la mort de son oncle, dont il était pourtant très proche, survenue trois ans avant l’opération.
La comparaison des capacités mnésiques des différents patients opérés a ainsi mis en évidence un lien entre les difficultés de mémoire et les lésions hippocampiques. Les résultats de cette étude amènent Scoville et Milner à conclure sur le rôle central de l’hippocampe dans la mémoire humaine. Cette structure serait le siège de la mémoire, essentielle à la création de nouveaux souvenirs et à la mémorisation de nouvelles informations.
Les différents systèmes mnésiques et le rôle de l’hippocampe
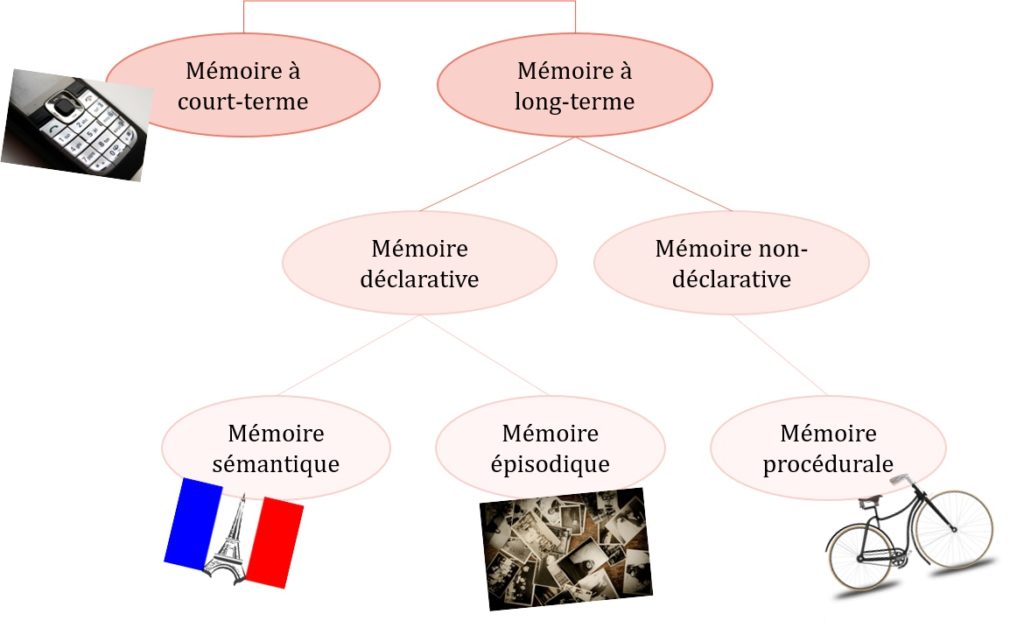
Le patient H.M. est inoubliable pour la recherche sur la mémoire humaine puisque son cas est le point de départ de nombreuses recherches sur le rôle de l’hippocampe. Jusqu’à sa mort en 2008, le patient H.M. a continué de participer à ces recherches, principalement menées à l’Université McGill à Montréal par l’équipe de recherche de Brenda Milner et Suzanne Corkin. Leurs études ont montré que, contrairement à ce que l’on pourrait penser, toute la mémoire du patient H.M. n’est pas déficitaire ! Les recherches sur la mémoire du patient H.M. ont ainsi participé à la découverte de différentes formes de mémoire (Figure 4). Les formes de mémoire préservées chez le patient H.M. sont donc gérées par d’autres structures cérébrales que l’hippocampe. Ainsi, le patient H.M. est capable de mémoriser de manière immédiate une suite de chiffres qui lui sont présentés à l’oral [1]. Cette mémoire à court-terme permet, par exemple, de retenir un numéro de téléphone le temps de chercher de quoi le noter. Ces informations sont ensuite oubliées, si elles ne sont pas stockées en mémoire à long-terme.
Au sein de ce que l’on appelle mémoire à long-terme, on retrouve la mémoire procédurale qui est la mémoire des savoir-faire, des habiletés motrices dont le souvenir est automatique, telles que la conduite, la pratique du vélo ou encore d’un instrument de musique (Figure 4). Quand vous dîtes « c’est comme le vélo, ça ne s’oublie pas », vous parlez donc de mémoire procédurale. La mémoire déclarative, elle, stocke les informations dont le rappel est conscient et que l’on peut exprimer à travers le langage (la définition d’un mot, la soirée de nos 18 ans, etc.). La mémoire déclarative est en partie composée de la mémoire sémantique et de la mémoire épisodique. La mémoire sémantique nous permet de nous souvenir de la forme et de la prononciation des mots, ainsi que de leur signification. Elle est également chargée du stockage des connaissances générales que nous avons sur le monde comme savoir que Paris est la capitale de France. La mémoire épisodique permet le maintien en mémoire et le souvenir d’événements personnellement vécus, en les replaçant dans leur contexte (où ? avec qui ?).
Après son opération, et malgré son incapacité à créer de nouveaux souvenirs, le patient H.M. est toutefois capable d’apprendre de nouvelles séquences motrices, des sortes de « chorégraphies » [2]. De plus, il a conservé en mémoire toutes ses connaissances acquises avant son opération, lui permettant de tenir des conversations normales. L’ensemble des recherches de l’Université McGill ont ainsi montré que seule la mémoire épisodique du patient H.M. a été perturbée par l’opération. Cette forme de mémoire permet de se souvenir des événements de vie. Grâce au patient H.M., et à sa participation aux recherches, le rôle de l’hippocampe dans la mémoire humaine a donc pu être précisé : l’hippocampe est nécessaire à l’encodage et au maintien de nouveaux souvenirs épisodiques.
D’autres patientes et patients ont également marqué l’histoire des neurosciences cognitives. En particulier, la description des changements de comportements et de personnalité de Phinéas Gage après son accident en 1848 ont permis de mettre en lumière le rôle des régions cérébrales frontales dans la régulation des comportements et le contrôle des impulsions [****] [3]. Le rôle de l’amygdale dans la capacité à percevoir et à ressentir les émotions a été en partie révélé par le cas de la patiente S.M. qui ne connaissait pas la peur [4]. En parallèle des recherches neuroscientifiques sur des participants sains, les études lésionnelles de cas uniques apportent des éléments clés et posent de nombreuses questions sur le lien entre cerveau et cognition.
[*] L’épilepsie est une maladie chronique caractérisée par des dérèglements soudains, ponctuels et répétés de l’activité électrique du cerveau. Les crises épileptiques sont le résultat d’un « orage cérébral », au cours duquel de nombreux neurones sont hyper activés simultanément.
[**] La psychose est marquée par une perte de contact avec la réalité, altérant les pensées, les croyances et les perceptions de l’individu qui en souffre. Ces altérations engendrent plusieurs formes de délires (par exemple : persécution, mégalomanie) avec présence ou non d’hallucinations sensorielles.
[***] L’étalonnage est une étape cruciale lors de la création de tests puisqu’elle établit la performance moyenne à une tâche d’une population donnée (par tranches d’âge, par sexe, etc.). Cette performance moyenne est ensuite comparée à celle d’un individu. Plus la performance de cet individu s’éloigne de la moyenne, plus celle-ci est atypique.
[****] Un article si vous souhaitez en savoir plus sur Phinéas Gage.
[1] Milner B., et al., Further analysis of the hippocampal amnesic syndrome: 14-year follow-up study of HM. Neuropsychologia, 1968. DOI : 10.1016/0028-3932(68)90021-3. [Publication scientifique]
[2] Gabrieli J. D., et al., The impaired learning of semantic knowledge following bilateral medial temporal-lobe resection. Brain and cognition, 1988. DOI : 10.1016/0278-2626(88)90027-9. [Publication scientifique]
[3] Damasio H., et al., The return of Phineas Gage: clues about the brain from the skull of a famous patient. Science, 1994. DOI : 10.1126/science.8178168. [Publication scientifique]
[4] Adolphs R., et al., Impaired recognition of emotion in facial expressions following bilateral damage to the human amygdala.Nature, 1994. DOI : 10.1038/372669a0. [Publication scientifique]
Écriture : Fanny Grisetto
Relecture scientifique : Estelle Nakul et Prany Wantzen
Relecture de forme : Alexandre Fauquette et Audrey Denizot
Temps de lecture : environ 15 minutes.
Thématiques : Neurosciences cognitives (Sciences cognitives)
Publication originale : Scoville, W. B. & Milner, B., Loss of recent memory after bilateral hippocampal lesions. Journal of neurology, neurosurgery, and psychiatry, 1957. DOI : 10.1136/jnnp.20.1.11.

En 1953, le patient H.M. est opéré par le chirurgien William Beecher Scoville en raison de violentes crises d’épilepsie qui le handicapent au quotidien. Au cours de cette opération, une structure cérébrale, l’hippocampe, est lésée. Peu de temps après l’opération, l’équipe médicale observe chez ce patient une perte de mémoire massive. Le patient H.M. est ainsi devenu un cas d’école dans l’étude du lien entre l’hippocampe et les fonctions mnésiques.
« It’s a funny thing — you just live and learn. I’m living, and you’re learning. »
le patient H.M. [*]
Depuis ses 10 ans, Henry Molaison souffre d’épilepsie [**]. Malgré les traitements médicamenteux lourds prescrits par le neurochirurgien William Becher Scoville, le cas de Henry Molaison ne fait qu’empirer. Ses crises sont si fréquentes, pouvant aller jusqu’à dix épisodes par jour, qu’il lui est impossible de garder un emploi stable. En dernier recours, pour le soulager de ses crises, Scoville lui propose d’être opéré. En 1953, à l’âge de 27 ans, Henry Molaison, qui sera plus tard connu par ses initiales comme le patient H.M., est le premier patient épileptique à subir cette opération, que Scoville décrit alors comme « franchement expérimentale ».
L’opération et ses conséquences cliniques pour le patient H.M.
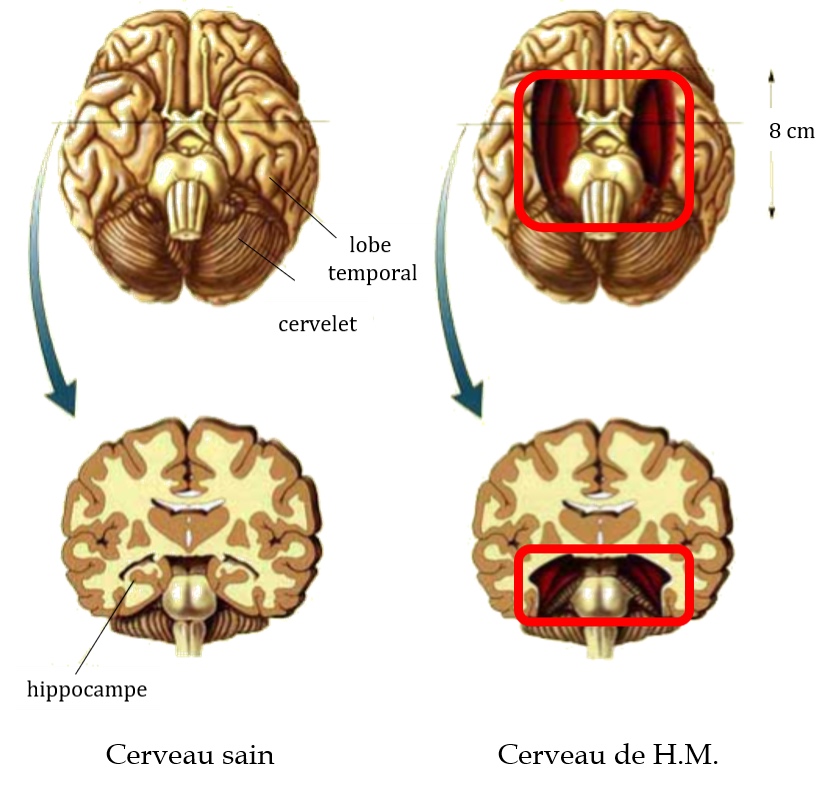
L’opération proposée par Scoville au patient H.M. est une procédure chirurgicale reconnue car déjà opérée à de multiples reprises sur des patients psychotiques [***], pour qui les traitements médicamenteux n’ont pas ou peu d’effet thérapeutique. Cette opération de dernier recours vise à réduire la sévérité et la fréquence des symptômes de la maladie, en lésionnant les zones du cerveau qui en seraient responsables. Ici, il s’agit de l’ablation bilatérale du lobe temporal médian (Figure 1), qui comprend, entre autres structures, l’hippocampe. Scoville propose cette opération au patient H.M. car l’hippocampe est suspecté de favoriser l’apparition de crises épileptiques. Ainsi, malgré le caractère expérimental de cette opération dans un cas d’épilepsie, Scoville espère atténuer les crises du patient H.M. en lui retirant cette région cérébrale. Le 01 septembre 1953, une résection bilatérale du lobe temporal, étendue sur huit centimètres à partir des extrémités des lobes temporaux (Figure 1, droite), est alors opérée sur le patient H.M.

Le patient H.M. montre rapidement les bénéfices de cette opération. La fréquence et la sévérité de ses crises épileptiques diminuent considérablement. Malgré l’ablation d’une grosse partie du cerveau, l’entourage du patient H.M. ne remarque aucun changement de personnalité, de capacités de communication, ni d’intelligence. Le maintien de ce niveau cognitif, ainsi que l’amélioration de son état physique, contrastent fortement avec une sévère perte de mémoire, rapidement observée par Scoville. Le patient H.M. est en effet désorienté, ne reconnaît plus les membres du personnel hospitalier et oublie après quelques minutes le contenu d’une conversation. Cette observation clinique entraîne alors un questionnement sur le rôle potentiel des structures lésées dans la mémoire humaine. Dans leur publication de 1957, Scoville et sa collaboratrice Brenda Milner, neuropsychologue de l’Institut Neurologique de Montréal, publient les premiers éléments de réponse. Leur étude constitue ainsi l’une des premières recherches fondamentales sur la mémoire et ses liens structurels avec les régions hippocampiques du cerveau. De nombreux travaux de recherche ont suivi cet article de 1957, et ont fait du cas du patient H.M. un cas d’école pour l’étude du système mnésique, à la fois au niveau neuroanatomique et au niveau cognitif, établissant les premiers fondements des modèles théoriques des différents types de mémoire.
Le point de départ de la recherche sur la mémoire
Après avoir observé la perte de mémoire massive du patient H.M., Scoville entreprend d’évaluer et de comparer les capacités mnésiques de plusieurs patients ayant subi une résection du lobe temporal. En effet, cette comparaison entre les patients permettrait de déterminer si les troubles de la mémoire du patient H.M. résultent effectivement de l’opération, et si oui, de dessiner les contours des zones cérébrales où siège la mémoire humaine. Par ailleurs, l’étendue des résections du lobe temporal médian diffère entre les patients, permettant de comparer les capacités cognitives des patients en fonction de la taille des lésions de l’hippocampe.
Dans leur publication de 1957, William Scoville et Brenda Milner évaluent l’efficience cognitive globale et la mémoire de dix patients ayant subi une résection temporale, dont le patient H.M. L’efficience étant la capacité d’un système à fournir un bon rendement, l’efficience cognitive globale est la capacité du cerveau à fonctionner de manière normale à tous les niveaux (attention, fonctionnement exécutif, perception, mémoire, etc). Pour quantifier l’efficience cognitive des patients, Scoville et Milner utilisent l’échelle d’intelligence de Wechsler-Bellevue, aujourd’hui connue sous sa forme révisée comme l’échelle d’intelligence pour adultes de Wechsler (Wechsler Adult Intelligence Scale, WAIS). De manière générale, Scoville et Milner n’observent pas d’altération de l’efficience cognitive globale chez leurs patients après l’opération. Pour caractériser la mémoire des patients, au-delà des observations cliniques, l’échelle de Mémoire de Wechsler (1945) est utilisée. Dans ces tests, les patients doivent rappeler à l’oral et immédiatement des dessins ou des histoires qui viennent de leur être présentés.
Le patient H.M. passe ces tests quatre ans après son opération. En mémoire, il obtient un score se situant dans la moyenne très basse des performances étalonnées [****]. De plus, à mesure que les tests s’enchaînent, il n’est plus capable de se rappeler, ou de reconnaître, les tests déjà réalisés. Enfin, s’il est capable de retenir pendant quelques minutes une série de trois chiffres ou une paire de mots, le souvenir de ces items disparaît dès qu’un événement perturbe son attention sur la tâche. La mémoire du patient H.M. est ainsi très fragile : les informations ne semblent pas être stockées sur le long terme. De plus, Brenda Milner observe que le patient est désorienté : il pense avoir 27 ans puisqu’il croit être toujours en 1953, l’année de son opération. Pour H.M., le temps s’est comme arrêté. À mesure que le temps passe, nous mettons à jour les dates et, par conséquent, notre âge. Le déficit de stockage de nouvelles informations en mémoire par le patient H.M. l’empêche de mettre à jour et se souvenir de son âge. Le patient H.M. semble ne plus être capable de créer de nouveaux souvenirs, déficit caractérisant l’amnésie antérograde (Figure 2, droite). Le patient H.M. ne peut donc pas retenir la nouvelle adresse de son domicile, ni retenir les noms des membres du personnel hospitalier, qu’il côtoie pourtant tous les jours depuis son opération. Il peut également lire le même journal jour après jour et y redécouvrir l’intégralité des articles avec surprise. De plus, malgré le fait que ses souvenirs les plus anciens restent intacts (par exemple les souvenirs de son enfance), le patient H.M. présente une amnésie rétrograde partielle : certains événements de sa vie préopératoire semblent avoir été effacés (Figure 2, gauche). Il a, par exemple, oublié la mort de son oncle, dont il était très proche, survenue trois ans avant l’opération.

Un profil amnésique similaire est également observé chez l’un des patients psychotiques, la patiente M.B., ayant subi la même opération chirurgicale et dont les lésions sont étendues sur huit centimètres (Figure 1). Ses troubles de la mémoire restés inaperçus après l’opération, du fait d’un état émotionnel instable, ont été mis en lumière grâce à l’échelle de Mémoire de Weschler. Les souvenirs des dessins et des histoires lors des tests sont fragiles et incomplets. Comme le patient H.M., elle est incapable de reconnaitre les tests déjà réalisés. Lors de l’entretien clinique, elle n’a aucune difficulté à parler de sa vie pré-opératoire, mais elle est incapable de donner des informations sur son séjour à l’hôpital. Cinq autres patients étudiés dans l’article de 1957 présentent des troubles de la mémoire modérés. Ces patients sont toujours capables de décrire le médecin qu’ils ont vu le matin même, mais ont des difficultés à se rappeler certaines informations après quelques minutes occupés avec une autre activité. Ces patients avaient subi une résection du lobe temporal médian plus petite que les patients H.M. et M.B. : leur hippocampe était donc seulement partiellement lésé. Enfin, les patients restants, ayant subi une résection unilatérale massive du lobe temporal médian ou limitée à l’extrémité de l’hippocampe, ne présentent aucun trouble de la mémoire et ont des scores de mémoire dans la moyenne ! Pour résumer ces comparaisons, il semble que tous les patients dont l’hippocampe pouvait être considéré comme lésé bilatéralement, que ce soit partiellement ou totalement, ont présenté des déficits de mémoire. L’ablation unilatérale, ou limitée à l’extrémité de l’hippocampe, ne sont, quant à elles, pas associées à des troubles mnésiques.
Ainsi, les résultats de Scoville et Milner suggèrent l’existence d’un lien neuropsychologique entre l’hippocampe et la capacité à retenir en mémoire de nouvelles informations. De plus, la sévérité des déficits mnésiques semble être associée à l’étendue des lésions des régions hippocampiques. Plus la résection du lobe temporal lèse les structures hippocampiques, plus les déficits mnésiques sont importants, le patient H.M. étant un des cas d’amnésie les plus marquants. Néanmoins, dans leur publication de 1957, les scientifiques soulignent qu’il ne leur est pas possible d’assurer l’exactitude de la nature des régions lésées. En effet, à cette époque, l’observation précise des zones lésées ne pouvait se faire qu’au travers de… l’autopsie ! Il faudra donc attendre quelques années, avec l’évolution des techniques d’imagerie cérébrale, mais également la mort du patient H.M., en 2008, pour analyser plus en détail les régions lésées de son cerveau…
Le patient H.M. : inoubliable participant à la recherche
Le patient H.M. est ainsi considéré comme le cas clinique ayant amené la recherche neuroscientifique à s’interroger sur le rôle de l’hippocampe dans la mise en mémoire de nouvelles informations. Par la pureté de la nature de ses troubles, qui ne sont limités qu’à la mémoire, il fut l’un des patients les plus étudiés tout au long de sa vie pour améliorer les connaissances sur le lien entre les structures hippocampiques et les processus mnésiques. Au fil des années, Brenda Milner a continué de suivre le patient H.M., avec l’aide de son équipe de recherche dont Suzanne Corkin, neuropsychologue de l’Université McGill de Montréal, qui a étudié la mémoire du patient H.M. jusqu’à la mort de celui-ci. Leurs recherches ont permis d’affiner les connaissances sur les conséquences d’une lésion hippocampique bilatérale sur la mémoire en constatant que l’ensemble de la mémoire du patient H.M. n’était pas altérée.
En 1988, cette équipe de recherche explore la mémoire sémantique du patient H.M., celle qui stocke la signification, la reconnaissance et la prononciation des mots, ainsi que les connaissances générales que nous avons sur le monde (par exemple que Paris est la capitale de France) [1]. Ses capacités sémantiques étaient intactes, lui permettant de tenir des conversations normales avec l’ensemble de ses connaissances pré-opératoires. L’équipe constate également que le patient H.M. est capable de redessiner les plans de sa maison, alors qu’il y a emménagé après son opération, et de reconnaître des célébrités, devenues connues après son opération. Ces nouvelles informations sont donc encodées dans sa mémoire, c’est-à-dire maintenues en mémoire à long terme, malgré la lésion des structures hippocampiques, et sont stockées ailleurs que dans les zones lésées par l’opération. L’exposition continuelle et répétée, sur plusieurs années, de ces nouvelles informations sont les mécanismes qui ont permis de les maintenir en mémoire, malgré l’amnésie antérograde massive et persistante. Le patient H.M. est également capable d’apprendre des séquences motrices, démontrant une distinction entre la mémoire déclarative (la mémoire des informations dont le rappel est conscient et que l’on peut exprimer à travers le langage, telles que la définition d’un mot, ou l’anniversaire de nos 18 ans) et la mémoire procédurale (la mémoire des habiletés dont le rappel est automatique, tels que la conduite) qui, elle, semble trouver son siège au niveau du cervelet (Figure 1). Enfin, la mémoire à court terme de H.M., évaluée par le test des empans mnésiques, qui consiste à retenir et répéter immédiatement une suite de chiffres, et une suite de chiffres dans l’ordre inverse, était également préservée [2].
Peu à peu, les études ont alors précisé la nature des déficits mnésiques du patient H.M., dessinant par la même occasion les contours des différents systèmes mnésiques et des régions cérébrales associées. Dans le cas du patient H.M., la mémoire procédurale, la mémoire sémantique ou la mémoire à court terme sont restées intactes, seule sa mémoire épisodique est perturbée. Cette forme de mémoire permet de retenir des événements vécus, et de les replacer dans leur contexte (par exemple les personnes présentes, le lieu, l’humeur associée). L’hippocampe aurait ainsi un rôle spécifique dans l’encodage et le maintien de nouveaux souvenirs épisodiques [3]. En parallèle de l’exploration de la cognition du patient H.M., son cerveau a été grandement étudié pour préciser l’étendue des lésions et la nature des structures qui avaient été touchées lors de l’opération. L’évolution des techniques d’imagerie cérébrale a largement participé à l’enrichissement de ces connaissances. De son vivant, l’analyse du cerveau du patient H.M par IRM (Imagerie par Résonance Magnétique, Figure 3) a ainsi montré que l’étendue des lésions supposée par Scoville avait été surestimée.
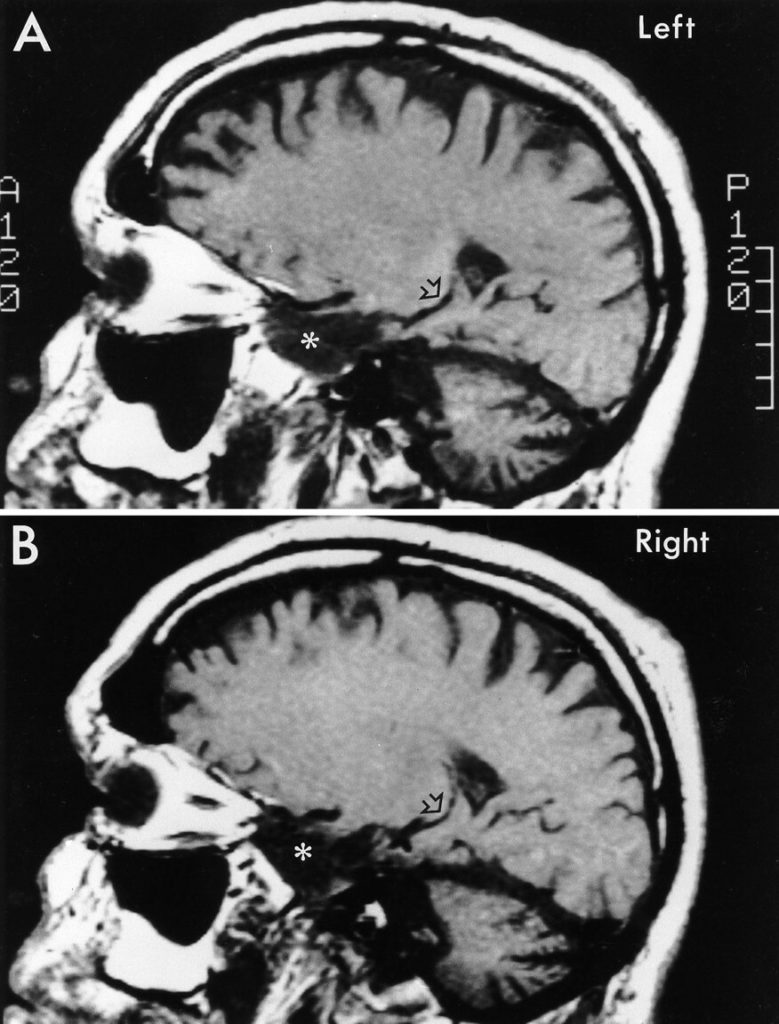
Après sa mort, l’autopsie de son cerveau a précisé davantage les régions lésées. Des analyses histologiques, c’est-à-dire des tissus biologiques, combinées à des reconstructions 3D du cerveau (disséqué plus finement que ce que permet l’IRM) ont cherché à délimiter précisément ces lésions [5].
L’importance des études lésionnelles en neurosciences cognitives
L’étude des lésions cérébrales et leurs conséquences est fondamentale pour la recherche en neuropsychologie. La lésion cérébrale est une porte d’entrée pour la compréhension de l’organisation de la cognition humaine. En effet, en étudiant leurs effets, il est possible d’inférer sur le fonctionnement normal des systèmes cognitifs. Les études lésionnelles sur des patients permettent alors de percer à jour les secrets du lien intime entre cerveau, cognition et comportement. D’autres patients, ayant des lésions touchant d’autres régions que celles de l’hippocampe, ont d’ailleurs marqué l’histoire des neurosciences cognitives. En particulier, l’observation des changements de comportements et de personnalité de Phinéas Gage après son accident en 1848 a permis de mettre en lumière le rôle des régions cérébrales frontales dans la régulation des comportements et le contrôle des impulsions [*****].
Le cas du patient H.M. a mis en lumière le rôle de l’hippocampe dans la rétention de nouveaux souvenirs d’événements vécus. Aujourd’hui, les chercheuses et chercheurs considèrent que l’hippocampe encode toutes les dimensions d’une expérience au service de la mémoire [6], expliquant par exemple pourquoi certaines odeurs nous ramènent en enfance. Les recherches sur certaines maladies neurodégénératives, et en particulier la maladie d’Alzheimer, ont ainsi ciblé l’hippocampe pour mieux comprendre les troubles mnésiques liés aux démences et en améliorer les prises en charge [7].
[*] « C’est une chose amusante — vous vivez et apprenez. Je vis et vous apprenez ». Tiré du livre « Permanent Present Tense » de Suzanne Corkin.
[**] L’épilepsie est une maladie chronique caractérisée par des dérèglements soudains, ponctuels et répétés de l’activité électrique du cerveau. Les crises épileptiques sont le résultat d’un « orage cérébral » pendant lequel de nombreux neurones sont hyper activées simultanément.
[***] La psychose est marquée par une perte de contact avec la réalité, altérant les pensées, les croyances et les perceptions de l’individu qui en souffre. Ces altérations engendrent plusieurs formes de délires (e.g., persécution, mégalomanie) avec présence ou non d’hallucinations sensorielles.
[****] L’étalonnage est une étape cruciale lors de la création de tests psychométriques standardisés. Elle permet d’établir l’étendue des scores ainsi que leur moyenne dans une population donnée (par tranches d’âge, par sexe). Cet étalonnage permet de situer la performance d’un individu par rapport à ce qui est observé dans une population de référence. Plus la performance s’éloigne de la moyenne, plus celle-ci est atypique.
[*****] Un article si vous souhaitez en savoir plus sur Phinéas Gage.
[1] Gabrieli J. D., et al., The impaired learning of semantic knowledge following bilateral medial temporal-lobe resection. Brain and cognition, 1988. DOI : 10.1016/0278-2626(88)90027-9. [Publication scientifique]
[2] Milner B., et al., Further analysis of the hippocampal amnesic syndrome: 14-year follow-up study of HM. Neuropsychologia, 1968. DOI : 10.1016/0028-3932(68)90021-3. [Publication scientifique]
[3] Dossani R. H., et al., The legacy of Henry Molaison (1926–2008) and the impact of his bilateral mesial temporal lobe surgery on the study of human memory. World neurosurgery, 2015. DOI : 10.1016/j.wneu.2015.04.031. [Publication scientifique]
[4] Corkin S., et al., HM’s medial temporal lobe lesion: findings from magnetic resonance imaging. Journal of Neuroscience, 1997. DOI : 10.1523/JNEUROSCI.17-10-03964.1997. [Publication scientifique]
[5] Annese J., et al., Postmortem examination of patient HM’s brain based on histological sectioning and digital 3D reconstruction. Nature communications, 2014. DOI : 10.1038/ncomms4122. [Publication scientifique]
[6] Ekstrom A. D. & Ranganath C., Space, time, and episodic memory: The hippocampus is all over the cognitive map. Hippocampus, 2018. DOI : 10.1002/hipo.22750. [Publication scientifique]
[7] Mu Y. & Gage F.H., Adult hippocampal neurogenesis and its role in Alzheimer’s disease. Molecular Neurodegeneration, 2011. DOI : 10.1186/1750-1326-6-85. [Publication scientifique]