La vascularisation de l’implant, clé d’une réparation osseuse efficace ?
Écriture : Charlotte Garot
Relecture scientifique : Nathalie Douard et Quentin Müller
Relecture de forme : Camille Thomas et Audrey Denizot
Temps de lecture : environ 13 minutes.
Thématiques : Biomatériaux & Génie tissulaire (Biologie et Ingénierie)
Publication originale : Vidal L., et al., Regeneration of segmental defects in metatarsus of sheep with vascularized and customized 3D-printed calcium phosphate scaffolds. Scientific Reports, 2020. DOI : 10.1038/s41598-020-63742-w. Accès sur HAL (pdf).

Les pertes osseuses faisant suite à des fractures mal réparées ou à un cancer des os, par exemple, sont traditionnellement réparées à l’aide d’une greffe d’os provenant du même patient que celui qui la reçoit : on parle d’autogreffe. Cette solution est efficace mais présente de nombreux inconvénients, notamment des douleurs sur le site de prélèvement. Ainsi, de nombreux chercheurs développent des implants synthétiques comme alternative aux autogreffes. Luciano Vidal et ses collègues proposent, en 2020, une approche particulière en combinant l’impression 3D, donc la fabrication sur-mesure des implants, avec l’insertion de vaisseaux sanguins dans l’implant pour optimiser la réparation osseuse. Cette nouvelle approche a été évaluée chez la brebis.
Pourquoi s’intéresser aux implants ?
Après un choc violent, il est courant que la victime souffre de fractures osseuses. Dans la majorité des cas, ces fractures vont se réparer par elles-mêmes en immobilisant l’os touché. Cependant, dans 5 à 10 % des cas, la fracture est si importante que l’os ne pourra pas se réparer de lui-même [1]. C’est ce que l’on appelle un défaut osseux de taille critique. Ces défauts sont aujourd’hui réparés par une greffe osseuse, le plus souvent une autogreffe, ce qui signifie que le patient donneur est également le patient receveur. Cette solution, bien qu’efficace, présente des inconvénients : des risques de douleurs et de maladies sur le site de prélèvement et une quantité limitée d’os disponible, rendant son utilisation impossible lorsque les défauts sont trop volumineux. Pour s’affranchir de ces désavantages, cela fait maintenant plusieurs années que les chercheurs développent des implants ayant vocation à remplacer la greffe osseuse. Ces implants doivent donc supporter la régénération osseuse tout en étant acceptés par le corps humain sans provoquer de forte réaction immunitaire [*] : c’est ce que l’on appelle la biocompatibilité. De nombreux implants ont ainsi été développés. Cependant, aucun n’a permis une régénération osseuse aussi efficace que l’autogreffe, qui est donc restée la technique de référence à ce jour.
Le sang : élément fondamental de la réparation osseuse
Une des raisons pour lesquelles les implants précédemment développés n’ont pas réussi à détrôner la greffe osseuse est leur manque de vascularisation, c’est-à-dire le manque de colonisation de l’implant par des vaisseaux sanguins. En effet, l’apport de sang est primordial dans la régénération osseuse, car c’est lui qui fournit l’oxygène et les nutriments aux cellules qui constituent l’os [2]. Cela permet aux cellules osseuses de survivre et de se multiplier et d’enfin coloniser l’implant, induisant ainsi une régénération plus efficace de l’os. Face à ce constat, Luciano Vidal et ses collègues ont cherché une solution permettant d’apporter suffisamment de sang dans l’implant, afin d’obtenir une régénération osseuse efficace.
La vascularisation de l’implant : solution pour la réparation osseuse ?
Pour cela, l’équipe de chercheurs a fait une étude sur des brebis. Ils ont étudié leur métatarse, l’os situé juste au-dessus de leurs sabots. Le but de l’étude était de régénérer, à l’aide d’un implant, un défaut osseux de 35 mm de long créé dans ces métatarses. Pour cela, les métatarses ont été scannés avant la création du défaut osseux afin de concevoir un implant sur mesure, correspondant parfaitement aux dimensions de l’os à réparer. L’implant a alors été fabriqué par impression 3D [pour approfondir : voir note A]. L’avantage de l’impression 3D est que cette technique permet de fabriquer des implants poreux, dont la taille et la forme des pores sont parfaitement contrôlées [pour approfondir : voir note B]. Cette porosité permet aux vaisseaux sanguins de traverser l’implant et donc d’améliorer la vascularisation de celui-ci.
L’implant développé ici est composé de phosphates de calcium synthétiques. Les phosphates de calcium sont des minéraux qui composent la phase inorganique de l’os, ce qui rend l’implant biocompatible. De plus, sa géométrie interne et sa porosité permettent à l’implant de servir d’échafaudage aux cellules : elles peuvent s’attacher à lui, migrer et se multiplier en suivant son motif, comme une vigne suit le treillis qui la supporte lorsqu’elle croît. On dit alors que l’implant est ostéoconducteur, ce qui signifie qu’il guide la régénération osseuse. Cet implant est conçu en deux parties : une partie principale, avec une rainure au centre, et une sorte de bouchon qui vient s’insérer dans la rainure, appelé bouchon vasculaire (Figure 1).
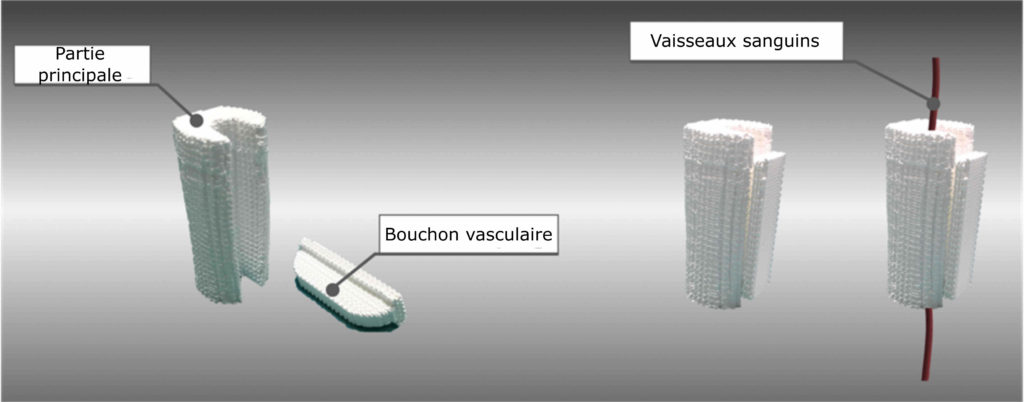
Après création du défaut osseux, la partie principale de l’implant y a été insérée, en positionnant les vaisseaux sanguins environnants dans la rainure centrale. Ces vaisseaux ont ensuite été maintenus au centre de l’implant à l’aide du bouchon vasculaire. Il est important de noter qu’ici, des angioscanners, c’est-à-dire une imagerie des vaisseaux sanguins en plus de celle de l’os, ont été réalisés avant et après l’implantation permettant ainsi de replacer correctement les vaisseaux sanguins dans l’implant. Cette approche est très inhabituelle car la vascularisation est le plus souvent obtenue par ajout de molécules actives dans l’implant, telles que des facteurs de croissance qui favorisent la multiplication et la survie des cellules qui constituent les vaisseaux sanguins. Ici, le chirurgien utilise directement les vaisseaux sanguins de l’animal et les déplace au centre de l’implant pour maximiser la vascularisation et donc l’apport de nutriments aux cellules, favorisant une régénération de l’os plus efficace.
Les chercheurs ont ensuite comparé la régénération osseuse dans trois conditions différentes :
- un groupe contrôle : le défaut a été laissé vide (sans implant mais avec une plaque pour assembler les deux parties de l’os) ;
- le groupe : le défaut a été comblé avec un implant où les vaisseaux sanguins sont restés à l’extérieur de l’implant, dans leur position naturelle ;
- le groupe 2 : le défaut a été comblé avec un implant dans lequel les vaisseaux sanguins ont été positionnés dans sa rainure centrale.
La comparaison du groupe contrôle avec les groupes 1 et 2 permet de vérifier que le défaut osseux créé est bien de taille critique, c’est-à-dire qu’il ne va pas se réparer spontanément. La comparaison permet également de tester si l’ajout d’un implant est bénéfique et nécessaire à la régénération osseuse. La comparaison entre les groupes 1 et 2 permet quant à elle de savoir si la position des vaisseaux sanguins au centre de l’implant permet une meilleure vascularisation de celui-ci ainsi qu’une meilleure régénération osseuse.
Les scanners effectués au cours de l’étude, qui a duré 3 mois au total, ont montré que la présence de l’implant, avec ou sans vaisseaux sanguins en son sein, a largement amélioré la régénération osseuse par rapport au défaut laissé vide (Figure 2).
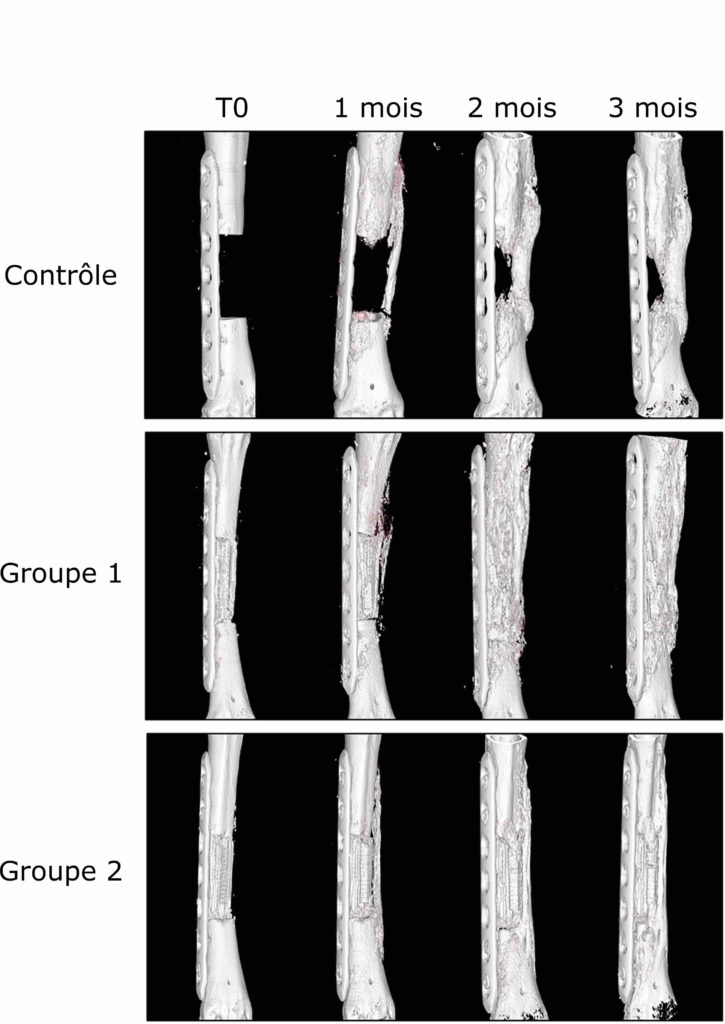
De plus, l’ajout des vaisseaux sanguins au centre de l’implant plutôt qu’à l’extérieur a permis une régénération plus efficace (Figure 3).
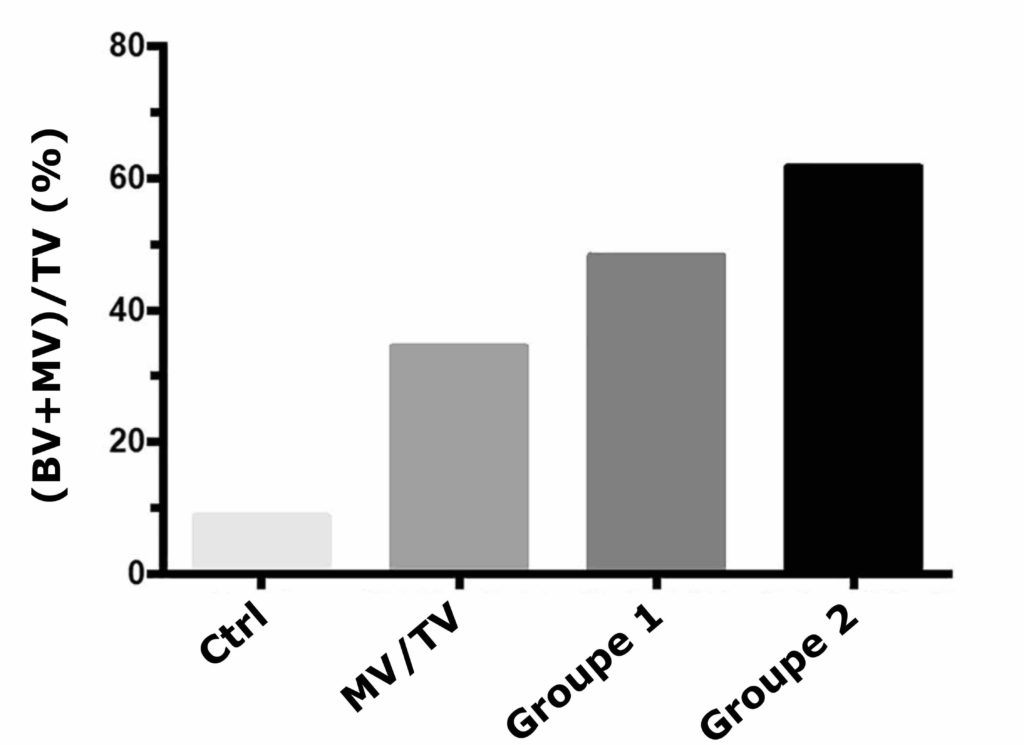
Bientôt des implants sur-mesure pour réparer nos os ?
Le modèle animal utilisé ici est intéressant car les brebis adultes présentent une masse, une composition minérale osseuse, un métabolisme et un taux de renouvellement osseux similaires à ceux des humains [3]. Ainsi, la vitesse de réparation osseuse est comparable entre les deux. De plus, le métatarse de brebis a pour spécificité d’être particulièrement mal vascularisé et sa réparation est donc réputée comme étant difficile [4]. Par ailleurs, la technologie utilisée, à savoir l’association des scanners et de l’impression 3D, permet une médecine personnalisée. Ainsi, les défauts osseux aux formes les plus complexes et aux tailles les plus importantes pourront être réparés sur mesure.
Ici, les auteurs n’ont utilisé qu’une brebis par groupe, permettant de sacrifier moins d’animaux. Un inconvénient majeur de cette étude est donc que les résultats sont très dépendants de l’animal et on ne peut alors pas conclure si l’effet observé est dû à une différence entre les brebis ou au type d’implant. Bien que cette étude ne soit que préliminaire et ait besoin d’être confirmée, notamment avec des expérimentations sur l’humain, elle ouvre des perspectives très prometteuses pour réparer les défauts osseux de grande taille sans avoir recours à l’autogreffe osseuse.
Éléments pour approfondir
Note A
Il existe différentes méthodes d’impression 3D pour fabriquer des implants osseux [5]. La plus connue est l’impression par dépôt de fil fondu. C’est la technologie qui vient le plus rapidement à l’esprit lorsque l’on parle d’impression 3D. Dans cette méthode, le matériau, la plupart du temps du plastique, se trouve sous forme de filament. Ce filament passe par une buse d’impression qui le chauffe au-delà de son point de fusion et qui le dépose couche par couche sur un plateau en le faisant immédiatement refroidir et donc durcir. Le matériau le plus utilisé avec cette méthode, que ce soit en usage pour particuliers ou pour fabriquer des implants, est l’acide polylactique (PLA). Pour la régénération osseuse, le PLA peut être utilisé seul ou avec ajout de phosphates de calcium pour une meilleure induction de la régénération osseuse. Une autre méthode d’impression 3D est la stéréolithographie. Les imprimantes 3D utilisant cette technologie sont constituées d’un bac contenant une résine qui durcit lorsqu’elle reçoit des UV. Un support est plongé dans le bac. De la lumière est projetée sur ce support, avec un motif prédéfini par l’utilisateur, ce qui fait durcir la résine. Le support remonte ensuite d’un cran dans le bac et l’opération peut recommencer autant de fois que nécessaire jusqu’à obtenir la forme souhaitée. Pour la fabrication d’implants osseux, la résine est souvent remplacée par des gels composés d’éléments constitutifs de l’os comme le collagène ou l’acide hyaluronique par exemple. D’autres technologies d’impression 3D permettent d’imprimer des métaux en partant d’une poudre métallique. Cette poudre est chauffée au-delà du point de fusion du métal utilisé, en général avec un laser, ce qui permet aux particules de s’agglomérer. L’opération est répétée en ajoutant à chaque fois de la poudre métallique par-dessus la couche qui vient d’être réalisée. Cette méthode est utilisée pour la fabrication d’implants en titane, qui est un matériau biocompatible très utilisé dans le biomédical.
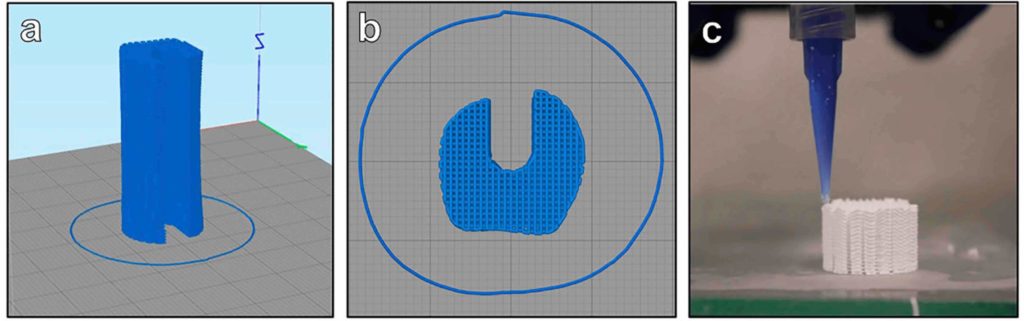
La technique utilisée ici est le robocasting. Le principe est relativement simple : une sorte de pâte de céramique contenue dans une petite seringue est poussée et extrudée suivant un motif prédéfini par l’utilisateur sur un logiciel pilotant l’imprimante 3D (Figure 4). En fait, c’est le même principe que l’impression par dépôt de fil fondu, sauf qu’ici le matériau n’a pas besoin d’être chauffé pour être déposé.
Note B
Il existe deux types de porosité : la macroporosité et la microporosité (Figure 5). La macroporosité est celle qui est visible à l’œil nu, c’est-à-dire lorsque la taille des pores est comprise entre 100 µm et quelques mm (Figure 5a et 5b).

C’est la macroporosité qui permet la croissance du nouvel os entre les mailles de l’implant. De plus, elle joue un rôle important dans la bonne intégration de l’implant à l’os environnant. Cette porosité peut être interconnectée, c’est-à-dire que les pores sont connectés les uns aux autres. Une porosité interconnectée est essentielle pour une régénération osseuse efficace. En effet, elle va permettre aux fluides biologiques, notamment aux vaisseaux sanguins, de pénétrer dans l’implant. De plus, plus il y a de pores et d’interconnections, plus il y a de surface d’implant disponible pour que les cellules puissent s’y attacher et ensuite former de l’os. Dans cette étude, les chercheurs ont choisi d’utiliser des pores orthogonaux, à la forme cubique. Cela a permis d’obtenir un implant avec une porosité d’environ 81 %, qui inclut à la fois la macro et la microporosité. Ainsi, les vaisseaux sanguins ont suffisamment d’espace pour pénétrer dans l’implant. La microporosité est quant à elle propre au matériau utilisé. La taille des pores varie de quelques µm à quelques dizaines de µm, ce qui correspond à peu près à la taille d’une cellule osseuse (~10 µm). Ici, le matériau étant une céramique, une microporosité sera présente entre les grains de phosphate de calcium (Figure 5c et 5d). La microporosité est importante pour la pénétration des cellules dans le matériau. Sans microporosité, les cellules peuvent passer dans l’implant mais pas dans les « branches » du matériau. Cette pénétration dans le matériau est pourtant intéressante car elle facilite la dégradation du matériau et son remplacement par du nouvel os. La microporosité permet également d’augmenter la surface de l’implant et donc la surface disponible pour que les cellules s’y attachent [6]. La régénération osseuse est donc favorisée.
[*] Si les implants ne doivent pas provoquer de forte réaction immunitaire, ils doivent en revanche permettre une légère inflammation du tissu osseux ! En effet, bien que les termes d’inflammation et de réaction immunitaire soient généralement perçus négativement, une inflammation est indispensable à la réparation osseuse et même à la réparation de tous les tissus de façon plus générale. L’inflammation est d’ailleurs la première étape de la réparation osseuse après une lésion [1].
[1] Gaston M. S., et al., Inhibition of fracture healing. The Journal of Bone and Joint Surgery. British volume, 2007. DOI : 10.1302/0301-620X.89B12.19671. [Review]
[2] Hankenson K. D., et al., Angiogenesis in bone regeneration. Injury, 2011. DOI : 10.1016/j.injury.2011.03.035. [Publication scientifique]
[3] Cipitria A., et al., Polycaprolactone scaffold and reduced rhBMP-7 dose for the regeneration of critical-sized defects in sheep tibiae. Biomaterials, 2013. DOI : 10.1016/j.biomaterials.2013.09.011. [Publication scientifique]
[4] Petite H., et al., Tissue-engineered bone regeneration. Nature Biotechnology, 2000. DOI : 10.1038/79449. [Publication scientifique]
[5] Garot C., et al., Additive Manufacturing of Material Scaffolds for Bone Regeneration: Toward Application in the Clinics. Advanced Functional Materials, 2020. DOI : 10.1002/adfm.202006967. [Review]
[6] Woodard J. R., et al., The mechanical properties and osteoconductivity of hydroxyapatite bone scaffolds with multi-scale porosity. Biomaterials, 2007. DOI : 10.1016/j.biomaterials.2006.08.021. [Publication scientifique]