Chargement de l'article...
Écriture : Audrey Denizot
Relecture scientifique : Christine Duthoit
Relecture de forme : Carlotta Figliola et Jérémy Ferrand
Temps de lecture : environ 10 minutes.
Thématiques : Biologie cellulaire (Biologie)
Publication originale : Thillaiappan N. B., et al., Ca2+ signals initiate at immobile IP3 receptors adjacent to ER-plasma membrane junctions. Nature Communications, 2017. DOI : 10.1038/s41467-017-01644-8
Le calcium, c’est bon pour les os mais aussi pour nos cellules. En effet, il permet à ces dernières de communiquer. Thillaiappan et ses collègues utilisent des techniques à très haute résolution spatiale pour montrer que les molécules qui sont à l’origine des signaux calcium sont… confinées ! Rien à voir avec la pandémie : il semble qu’ici le confinement leur permet en fait de communiquer de manière plus efficace !
Les cellules, ça communique ?
Quand deux personnes communiquent entre elles, il y a une personne qui émet un message et l’autre qui le reçoit et y répond. Prenons l’exemple de Gertrude et Monique. Lorsque Gertrude dit à Monique « Tu reprendras bien un peu de soupe ? », Gertrude émet un signal. Ce signal va être perçu par les oreilles de Monique (bien qu’avec son âge avancé, son ouïe n’est plus ce qu’elle était !). Ce signal sonore va ensuite être analysé par le cerveau de Monique. Cette étape correspond à la transduction du message, qui permet à Monique de comprendre le signal de Gertrude et de proposer une réponse adaptée, ici : « Oh oui, volontiers ! Elle est délicieuse ta soupe, Gertrude, comme toujours ! ». Eh bien, figurez-vous que nos cellules communiquent aussi !
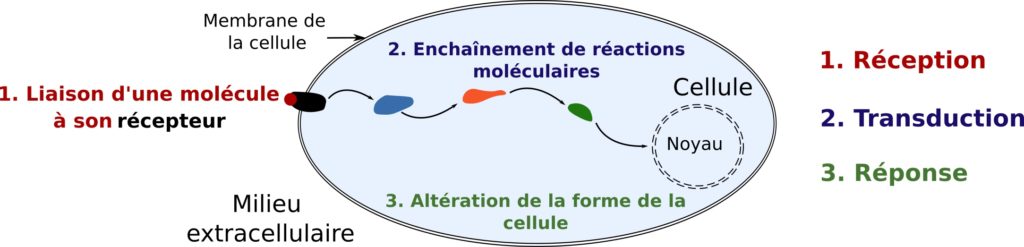
La Figure 1 montre un exemple dans lequel une cellule reçoit un signal (sous la forme de molécules présentes à proximité) et y répond par un changement de forme. Les signaux que les cellules reçoivent sont divers et leurs réponses varient à la fois en fonction du signal et en fonction de l’état dans lequel se trouve la cellule. Si l’on reprend l’exemple de Monique, elle ne va pas réagir de la même façon si Gertrude lui propose de manger de la soupe ou de faire la vaisselle. D’autre part, elle n’aura pas la même réaction si Gertrude lui propose de la soupe en début de repas ou en plein milieu d’après-midi ! Au niveau cellulaire, la libération de molécules par la cellule voisine (signal émis) peut être détectée par des récepteurs spécifiques sur la cellule qui reçoit l’information. La liaison des molécules en question à ces récepteurs engendre un enchaînement de réactions dans la cellule, qui aboutit à une réponse de la cellule adaptée au signal reçu, comme par exemple un changement de forme. Revenons à Monique : sa réponse consiste à sourire et à répondre à Gertrude qu’elle reprendrait bien un peu de soupe.
Le calcium, bon pour les os mais aussi pour la communication cellulaire
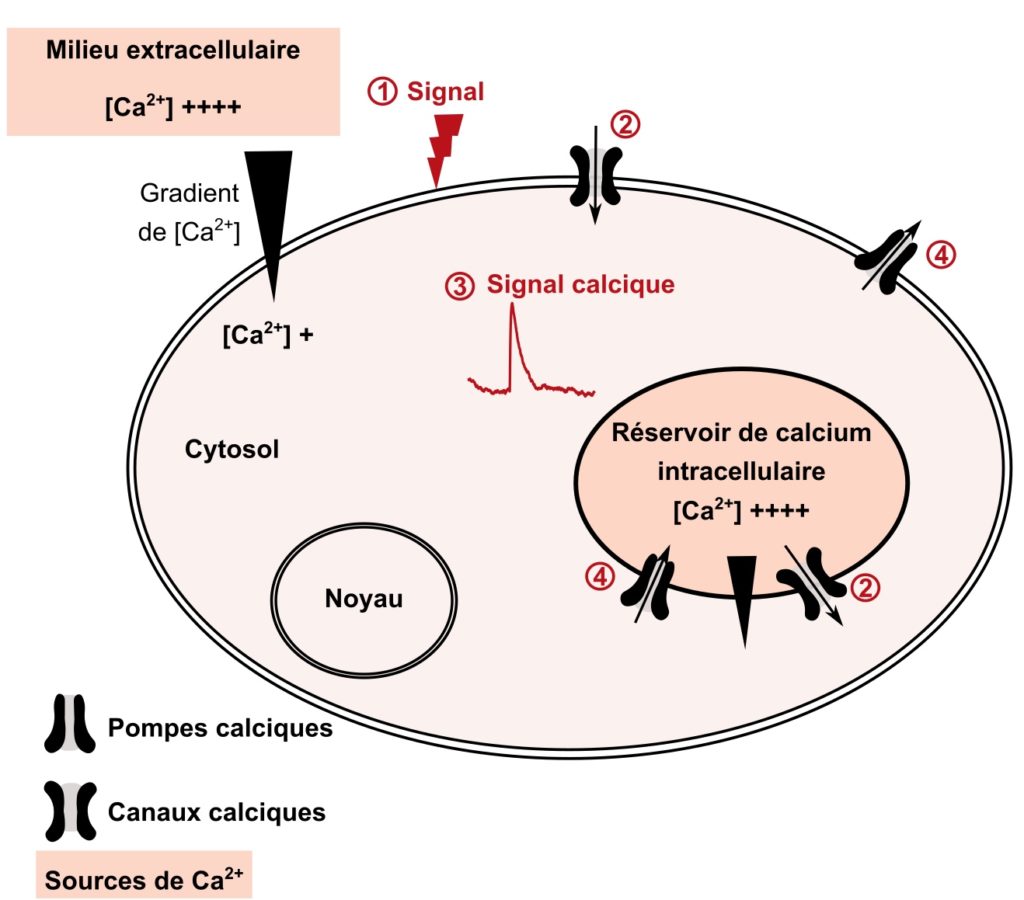
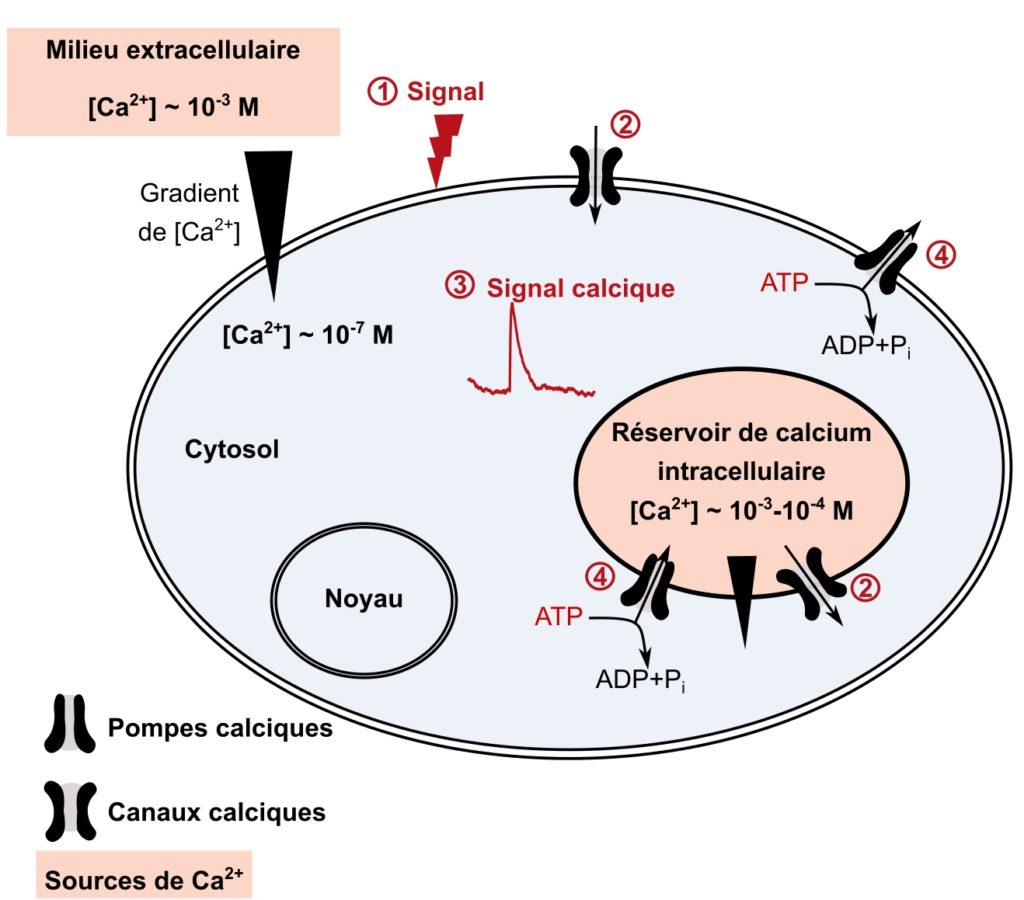
Le calcium, sous sa forme d’ion Ca2+, est un élément chimique indispensable pour la communication des cellules. « Comment donc ? », me demande Gertrude. Eh bien en fait, les cellules possèdent une quantité très régulée de calcium en leur sein. Dès que cette quantité augmente, la cellule comprend qu’il se passe quelque chose et peut agir en conséquence. Laissez-moi ici vous présenter l’exemple des cellules de nos muscles. Lorsque l’on veut effectuer un mouvement, notre système nerveux libère des molécules à proximité des cellules des muscles à contracter. Ces molécules activent les cellules du muscle. Ce message engendre l’ouverture de molécules appelées canaux qui, une fois ouvertes, permettent l’entrée de calcium dans la cellule. Cette augmentation de la concentration en calcium dans la cellule forme ce que l’on appelle un signal calcique. Ce dernier active une succession de réactions qui aboutissent à un raccourcissement des cellules musculaires et donc à la contraction du muscle. L’augmentation de la concentration en calcium ne dure que quelques secondes grâce à l’activité de molécules, les pompes calciques, qui renvoient le calcium à l’extérieur de la cellule. Le calcium se dissocie alors rapidement des molécules avec lesquelles il interagissait, ce qui engendre un allongement des cellules du muscle et donc un relâchement musculaire [*]. Le principe général de la formation des signaux calciques est résumé dans la Figure 2.
Le récepteur à l’IP3, une protéine primordiale pour la signalisation calcique
Comme expliqué dans la Figure 2, les signaux calciques résultent de l’ouverture de molécules appelées canaux calciques. La publication scientifique que je vous présente ici s’intéresse tout particulièrement à l’un d’entre eux : le récepteur à l’IP3 (inositol triphosphate pour les intimes) ou IP3R. Ces canaux sont situés à la membrane d’un compartiment présent à l’intérieur de nos cellules : le réticulum endoplasmique (RE). Le but de l’article présenté ici, écrit par Thillaiappan et ses collègues, est de mieux comprendre l’influence de la localisation des IP3R dans la cellule sur les signaux calciques. Ils montrent en particulier que certains IP3R sont confinés à la maison. Ces IP3R, dits « immobiles » et en apparence bien peu actifs, sont en fait à l’origine des signaux calciques dans les cellules étudiées. A l’inverse, des IP3R dits « mobiles » ne semblent pas s’ouvrir, n’étant de fait pas impliqués dans la communication de la cellule.
Confinés = qualifiés pour mieux communiquer ?
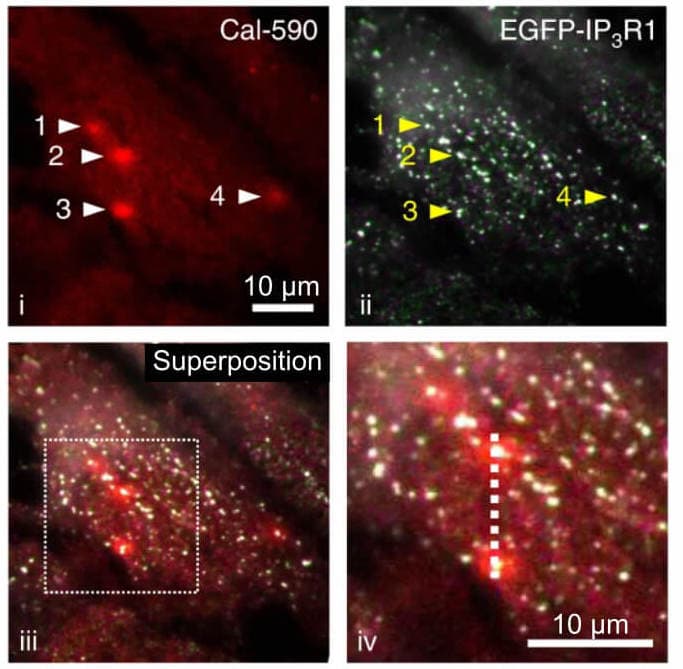
Pour arriver à ces résultats, ils ont utilisé des techniques dites de microscopie à super-résolution qui permettent d’observer de très petits objets (de l’ordre de 100 nanomètres, c’est-à-dire dix-millionièmes de mètre soit environ 1 000 fois plus petit que le diamètre d’un cheveu), Thillaiappan et ses collègues ont montré que les IP3R peuvent être divisés en deux catégories : mobiles et immobiles. Ils se sont ensuite demandés dans quelle mesure ces variabilités de mobilité des IP3R impactent les signaux calciques de la cellule. Pour cela, ils ont utilisé des protéines fluorescentes de différentes couleurs pour visualiser à la fois les IP3R (en vert) et les signaux calciques (en rouge). Les signaux calciques correspondent alors à des « gros points rouges » sur l’image de microscopie. En superposant les images montrant la localisation des IP3R et celles montrant la localisation des signaux calciques, les chercheurs se sont rendus compte que les signaux calciques étaient observés à côté des IP3R immobiles et pas à côté des IP3R mobiles (Figure 3). Ce sont donc les IP3R immobiles qui font le gros du travail de communication de la cellule, des vrais pros du travail confiné !
L’immobilité des IP3R leur donnerait donc un rôle central dans la cellule. Le fait que les signaux soient déclenchés à des endroits précis dans la cellule (ici, au niveau des IP3R immobiles) permet d’activer des réponses elles aussi localisées. Cela favorise la formation d’une réponse rapide au signal reçu. Si l’on reprend l’exemple de Monique, le fait qu’elle soit assise dans la cuisine à côté de Gertrude lui permet de bien l’entendre et de répondre à sa proposition de soupe. Si Monique était dans le salon et Gertrude dans la cuisine, Monique n’entendrait probablement pas la voix de Gertrude, couverte par le son de la télé ! Je vous laisse imaginer ce que la discussion pourrait alors donner : « Tu reprendras bien un peu de soupe ? » « Ah ça tu l’as dit, ils forment une sacrée troupe ! » La localisation des canaux calciques est donc un paramètre fondamental régissant la communication cellulaire.
Conclusion
Le calcium est nécessaire aux cellules, intervenant dans leur communication comme présenté ici, mais aussi dans leur croissance et leur mort, par exemple. Il intervient de plus dans la contraction des muscles, la fertilisation des ovules par les spermatozoïdes, notre protection contre les agents pathogènes et le bon fonctionnement de notre cerveau [2]. Le fait que ces signaux puissent être localisés à des endroits très précis au sein de la cellule pourrait donc permettre à cette dernière de gérer plusieurs communications simultanément (Figure 4). Les cellules, des as du multi-tâche ! Finalement, dans les cellules, le confinement est source d’efficacité en termes de communication, de quoi nous inspirer en cette période de pandémie ;).
[*] Pour plus de détails, vous pouvez vous référer à cette page.
[1] Denizot A., Simulation de la signalisation calcique dans les prolongements fins astrocytaires. 2019. [Manuscrit de thèse de doctorat]
[2] Maklad A., et al., Calcium Signaling in Brain Cancers: Roles and Therapeutic Targeting. Cancers, 2019. DOI : 10.3390/cancers11020145. [Publication scientifique]
Écriture : Audrey Denizot
Relecture scientifique : Christine Duthoit
Relecture de forme : Carlotta Figliola et Jérémy Ferrand
Temps de lecture : environ 17 minutes.
Thématiques : Biologie cellulaire (Biologie)
Publication originale : Thillaiappan N. B., et al., Ca2+ signals initiate at immobile IP3 receptors adjacent to ER-plasma membrane junctions. Nature Communications, 2017. DOI : 10.1038/s41467-017-01644-8

Le calcium, c’est bon pour les os mais aussi pour nos cellules. En effet, il permet à ces dernières de communiquer. Thillaiappan et ses collègues utilisent des techniques à très haute résolution spatiale pour montrer que les molécules qui sont à l’origine des signaux calcium sont… confinées ! Rien à voir avec la pandémie : il semble qu’ici le confinement leur permet en fait de communiquer de manière plus efficace !
L’ion calcium joue un rôle de second messager intracellulaire, omniprésent dans les cellules eucaryotes. Il est essentiel à de nombreuses fonctions comme la transmission des signaux, la croissance cellulaire, l’apoptose, la différenciation, le métabolisme, la transcription des gènes. Il intervient de plus dans la contraction musculaire, la fertilisation, l’immunité et la transmission de l’information nerveuse [1]. En réponse à un signal, comme par exemple une molécule libérée par la cellule voisine, des protéines membranaires nommées canaux calciques sont activées. Cela permet l’entrée de calcium et par conséquent une augmentation de la concentration en calcium dans la cellule : un signal calcique (Figure 1).
Par exemple, l’activité des neurones moteurs déclenche la libération d’un neurotransmetteur, l’acétylcholine, qui va se fixer à son récepteur à la membrane de la cellule musculaire. Ce signal active l’ouverture de canaux, engendrant la formation d’un signal calcique. Cette augmentation de la concentration en calcium permet des changements de conformations de protéines liant le calcium, aboutissant à un raccourcissement de la cellule musculaire et à la contraction du muscle. L’augmentation de la concentration en calcium ne durant que quelques secondes du fait de l’activité de protéines appelées pompes calciques, le calcium se dissocie rapidement des molécules avec lesquelles il interagit, ce qui aboutit au relâchement musculaire [*].
Les signaux calciques sont extrêmement régulés et temporaires (si une trop forte concentration en calcium est maintenue dans la cellule, cette dernière meurt). Du fait de leur rôle central dans la physiologie cellulaire, on observe une altération des signaux calciques dans de nombreuses maladies, notamment le cancer [2].
Le récepteur à l’IP3, une protéine primordiale pour la signalisation calcique
Comme expliqué dans la Figure 1, les signaux calciques intracellulaires résultent de l’ouverture des canaux calciques. L’article que je vous présente ici s’intéresse tout particulièrement à l’un d’entre eux : le récepteur à l’IP3 (inositol triphosphate pour les intimes) ou IP3R. Ce canal ne s’ouvre que lorsque l’IP3 et le calcium sont simultanément fixés à sa surface [**]. Les IP3R sont situés à la membrane d’un compartiment intracellulaire : le réticulum endoplasmique (RE), qui intervient notamment dans les processus de synthèse et de maturation des protéines. La concentration en calcium dans le RE est 1 000 fois plus grande que celle du cytosol. L’ouverture des IP3R engendre de fait un signal calcique.
Le but de l’article présenté ici, écrit par Thillaiappan et ses collègues, est de mieux comprendre l’influence de la localisation des IP3R sur les signaux calciques de la cellule. Leur principal résultat est que certains IP3R sont confinés à la maison dans des sites privilégiés de communication cellulaire. Ils montrent de plus que ces IP3R, à l’apparence bien peu actifs car immobiles, sont en fait à l’origine des signaux calciques dans les cellules étudiées (cellules HeLa [***]).
Les récepteurs à l’IP3 se rassemblent en famille
Dans la communauté des chercheurs qui travaillent sur les signaux calciques, il est bien connu que les IP3R se déplacent le long de la membrane du RE [4-6]. Cependant, il semble que la majorité des signaux calciques se forment de manière répétée à des endroits bien précis dans la cellule [7]. Cette observation suggère de fait que les IP3R sont immobiles, formant des sites intracellulaires au niveau desquels les signaux calciques ont une plus grande probabilité de se former, appelés hotspots (points chauds en anglais). Comment expliquer ces observations, en apparence contradictoires ?
Dans cette étude, les chercheurs utilisent des techniques de microscopie à super-résolution qui permettent de mieux caractériser non seulement la localisation mais aussi la mobilité de molécules fluorescentes, avec une très bonne résolution spatiale. En étudiant les IP3R avec ces méthodes, ils espèrent comprendre la controverse que je vous ai présentée dans le paragraphe précédent. Pour pouvoir marquer les IP3R par fluorescence et ensuite pouvoir visualiser leur localisation dans la cellule, Thillaiappan et ses collègues ont utilisé la technique dite de nucléases effectrices de type activateur de transcription (Transcription activator-like effector nucleases, TALEN, en anglais), qui consiste à utiliser des enzymes, appelées nucléases, qui coupent l’ADN au niveau d’une séquence spécifique. Ces nucléases sont générées en laboratoire afin de pouvoir se fixer à une région de l’ADN d’intérêt et ainsi être utilisées pour modifier spécifiquement l’ADN des cellules étudiées. Dans cette étude, elles ont été créées afin de marquer à la fois les IP3R et le RE par fluorescence avec des protéines fluorescentes différentes : EGFP (vert) et mCherry (rouge), respectivement. Cela a permis aux chercheurs de visualiser précisément la localisation des IP3R sur la surface du RE.
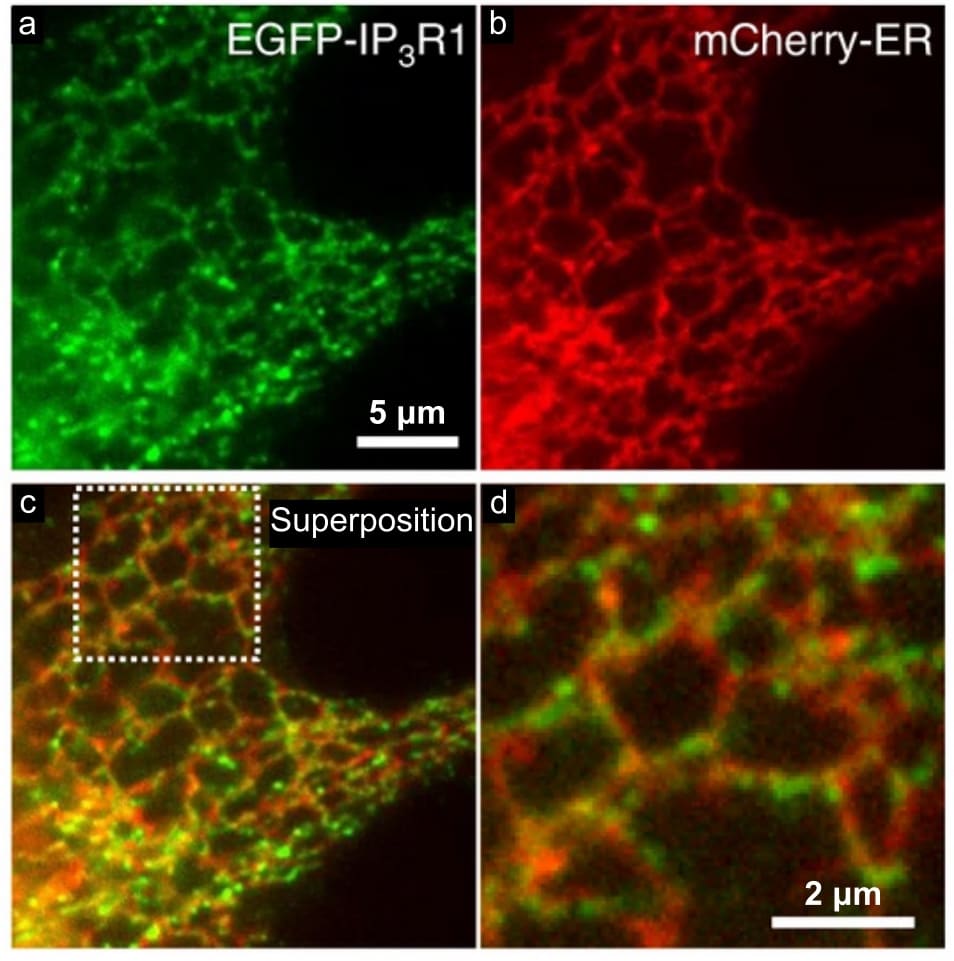
Si les IP3R, marqués en vert, étaient répartis de manière homogène sur la membrane du RE, marquée en rouge, on observerait une couleur orange, résultant de la superposition des deux fluorescences tout au long du RE. Ce n’est pas ce que les auteurs de l’article ont observé : il semblerait que les IP3R se rassemblent en petits amas à la surface du RE, caractérisés par une intensité de fluorescence plus grande, car résultant de l’accumulation de fluorescence de plusieurs molécules (Figure 2). Ces rassemblements de protéines sont communément appelés clusters (mais ceux-là ne sont pas des foyers de contagion !).
Ça fait quelle taille une famille d’IP3R ?
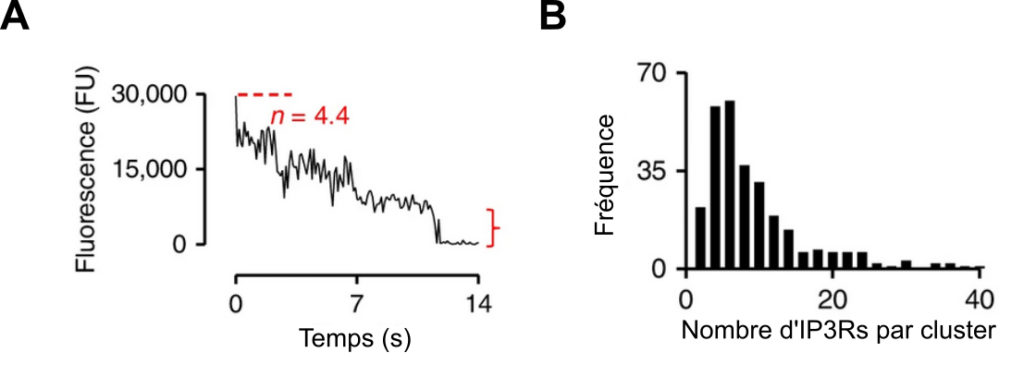
Comment faire pour déterminer le nombre de molécules présentes dans chaque cluster (famille) d’IP3R ? Thillaiappan et ses collègues ont utilisé pour cela la technique du photoblanchiment par étape (single-step photobleaching en anglais) sur les clusters d’IP3R. Lors du photoblanchiment, les molécules fluorescentes d’intérêt sont soumises à un flash lumineux de forte intensité dans une zone restreinte, ce qui engendre un changement de conformation des protéines fluorescentes, inhibant leur capacité à émettre de la fluorescence. Dans la technique du photoblanchiment par étape, le flash lumineux est choisi de telle sorte qu’une seule molécule est blanchie à la fois, engendrant une légère baisse de la fluorescence du cluster auquel la molécule appartient. Après des étapes de blanchiment successives, on arrive donc à une fluorescence nulle du cluster, ce qui signifie que tous les IP3R ont été blanchis. La diminution de fluorescence à la dernière étape (accolade rouge dans la Figure 3A) permet de définir la fluorescence d’une unique molécule. Si l’on divise la fluorescence initiale par cette fluorescence unitaire, on peut donc en déduire le nombre d’IP3R présents dans le cluster. Les chercheurs ont effectué cette expérience sur plusieurs centaines de clusters et en ont ainsi déduit le nombre d’IP3R par famille : 8 en moyenne mais pouvant aller jusqu’à 40 (Figure 3B). De grandes tablées en perspective pour ces familles d’IP3R pour les fêtes de fin d’année je présume !
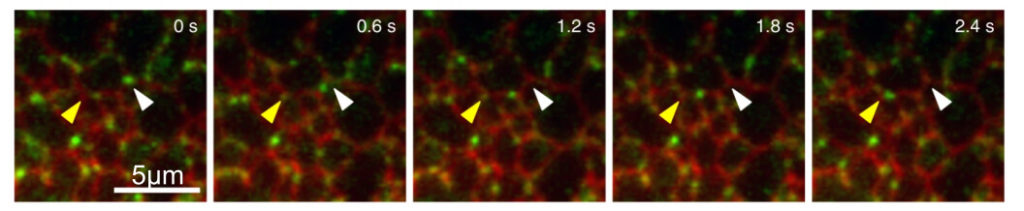
La majorité des familles d’IP3R sont nomades !
Comment ça, les molécules membranaires peuvent bouger ? Ne sont-elles pas fixées à la membrane ? Eh bien, oui, mais les protéines membranaires peuvent aussi se déplacer le long de la membrane par un phénomène appelé diffusion latérale. Sur la Figure 4, vous pouvez voir des images tirées d’une vidéo [#] montrant le déplacement d’une famille d’IP3R le long de la membrane du RE.
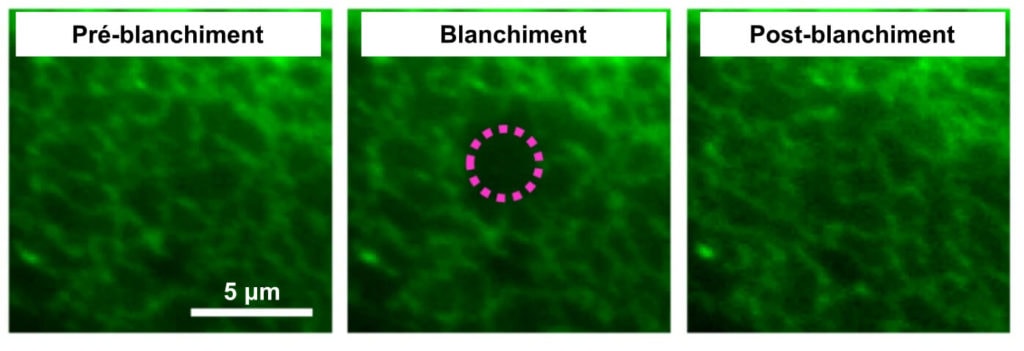
Il semble donc bien que les IP3R bougent. Comment expliquer alors le fait que les signaux calciques apparaissent de manière répétée aux mêmes endroits dans la cellule ? Essayons de caractériser de manière un peu plus précise les déplacements de ces IP3R. Pour ce faire, les chercheurs utilisent ici une technique très ingénieuse : la redistribution de fluorescence après photoblanchiment (en anglais fluorescence recovery after photobleaching, FRAP). Cette technique se base elle aussi sur le principe du photoblanchiment. La zone blanchie, ou bleachée, va ensuite progressivement redevenir fluorescente du fait du déplacement des molécules fluorescentes qui étaient situées en dehors de la zone blanchie. Le principe de cette technique est résumé dans la Figure 5. Elle permet donc à la fois de caractériser la proportion d’IP3R mobile mais aussi leur vitesse de déplacement.
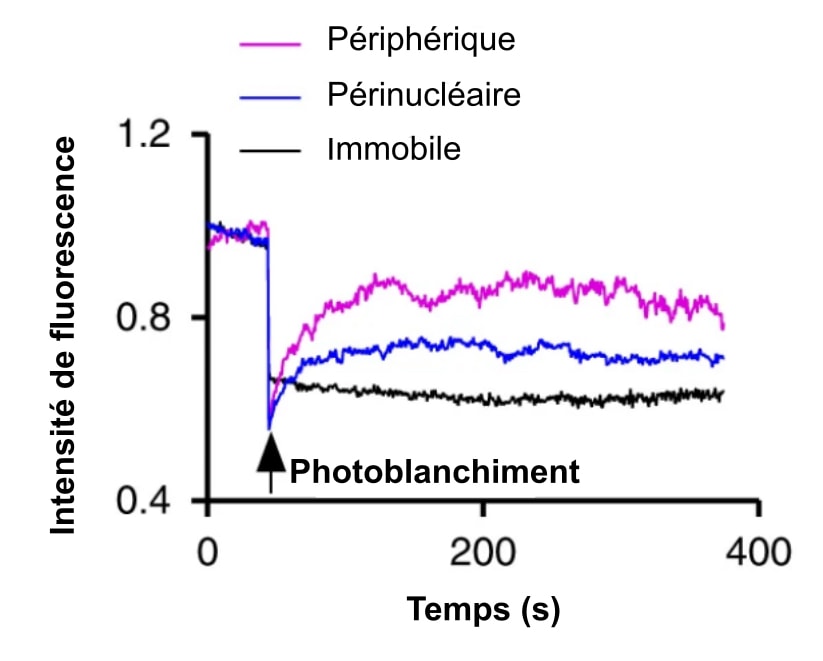
En utilisant la technique présentée dans la Figure 5, Thillaiappan et ses collègues ont étudié la mobilité des IP3R. Si, suite à un photoblanchiment, la fluorescence ne change pas au cours du temps, on en déduit que les IP3R sont immobiles. Les chercheurs ont par ce biais montré que certains clusters d’IP3R se déplacent tandis que d’autres semblent être immobiles (Figure 6).
Tous confinés ? Pas les IP3R !
Pour étudier le mouvement des IP3R, les chercheurs ont utilisé la technique de suivi individuel de particules (single particle tracking, SPT en anglais). Cette méthode permet de suivre la localisation de chaque molécule marquée par fluorescence à l’échelle nanométrique (Figure 7), échelle non observable par microscopie optique conventionnelle.
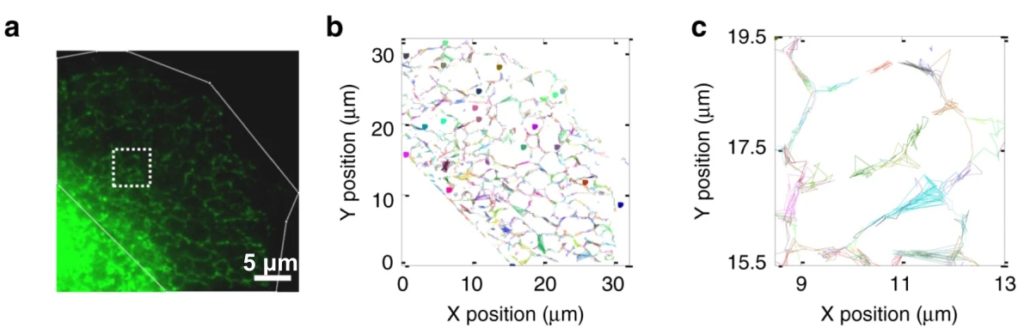
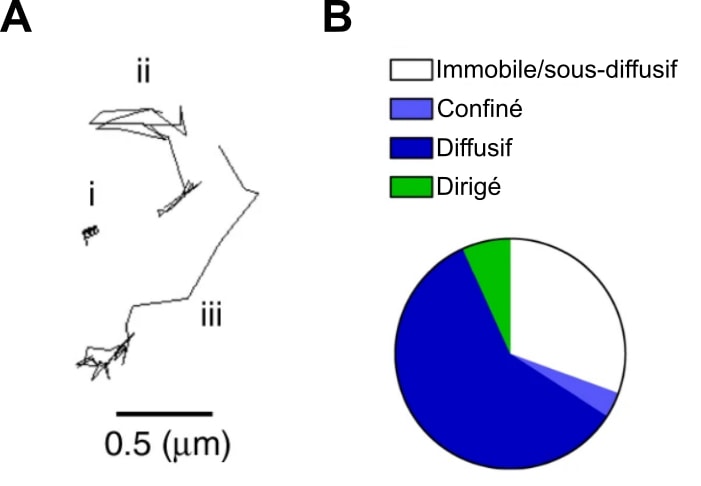
Les chercheurs ont montré qu’environ 75 % des clusters d’IP3R se déplacent, c’est-à-dire qu’elles n’ont pas une position fixe dans la cellule. À l’inverse, 25 % des clusters d’IP3R sont immobiles et confinées à une certaine position dans la cellule (Figure 8). Notez qu’il semble y avoir plusieurs processus à l’origine des déplacements des clusters d’IP3R : la majorité présentent une trajectoire aléatoire, caractéristique des déplacements par diffusion (mouvements Browniens), tandis que d’autres se déplacent de manière directionnelle, c’est-à-dire par des mouvements non aléatoires résultant de l’activité de molécules appelées moteurs moléculaires, présentes à la surface des microtubules [****]. Ces mouvements nécessitent un apport d’énergie (ATP). Les auteurs ont donc divisé les clusters d’IP3R en 4 catégories : immobiles, confinés (toujours aucun rapport avec la pandémie), diffusifs ou dont le déplacement est directionnel.
Confinés = qualifiés pour mieux communiquer ?
Imaginez ces pauvres petits IP3R confinés, qui aimeraient bien voir du pays mais qui sont coincés sur leur bout de membrane… Mais, au final, est-ce que le confinement des IP3R fonctionne comme le nôtre ? Eh bien, pas vraiment ! Thillaiappan et ses collègues ont montré que les clusters d’IP3R qui sont immobiles prennent du poids sont localisés dans des sites spécifiques de la cellule, au niveau de sites de contact entre la membrane de la cellule (membrane plasmique) et le RE. De plus, ils ont mis en évidence que ce sont ces IP3R, qui paraissent peu actifs, qui font le gros du boulot (les IP3R, les as du télétravail !). Comme expliqué dans l’introduction, les IP3R peuvent être activés en réponse à un signal extérieur. Ils vont alors s’ouvrir et générer un signal calcique qui permettra à la cellule de répondre au signal qu’elle a reçu.
Les chercheurs ont remarqué que les signaux calciques étaient toujours observés au même endroit dans la cellule. Il s’agit des sites de contact entre le RE et la membrane plasmique, à côté des IP3R immobiles (Figure 9) ! L’immobilité des IP3R leur donnerait donc un rôle central dans la cellule, permettant de produire des signaux à des localisations très précises au sein de la cellule [*****]. Le fait que les signaux soient déclenchés à des endroits précis dans la cellule permet d’activer des réponses elles-aussi localisées, permettant une réponse rapide au signal reçu. Bon, c’est très flou tout ça donc je vais vous donner un exemple concret ! Si on prend l’exemple des neurones, le fait que les canaux calciques et les vésicules contenant les neurotransmetteurs soient localisés au même endroit dans la cellule est nécessaire à la libération des neurotransmetteurs en réponse aux signaux calciques. Cela permet la libération rapide des neurotransmetteurs dans la synapse, où ils vont diffuser et se fixer à des récepteurs à la membrane du neurone dit post-synaptique. Si les signaux calciques étaient générés à un autre endroit dans la cellule, les neurotransmetteurs ne seraient pas libérés. La localisation des canaux calciques est donc un paramètre fondamental régissant la transmission des signaux.

Conclusion : IP3R confinés rime avec efficacité ?
Comme le calcium intervient dans de très nombreux processus cellulaires dont la mort cellulaire (!), le fait que certains IP3R semblent être homologués pour répondre aux signaux, et ce à des localisations bien précises dans la cellule, permet potentiellement d’éviter les interférences entre différents signaux. La cellule pourrait alors mener de front plusieurs « conversations » en même temps. La cellule, une vraie pro multi-tâche ! L’utilisation des techniques de microscopie à super-résolution comme celles présentées dans cet article est très récente. De fait, on commence à peine à caractériser les mouvements des molécules au sein de la cellule et à comprendre leurs rôles. Le confinement des molécules pourrait bien être la norme permettant aux cellules de gérer leur communication avec le monde extérieur de façon contrôlée et fiable. Finalement, dans les cellules, le confinement est source d’efficacité en termes de communication, de quoi nous inspirer en cette période de pandémie ;).
[*] Pour plus de détails, vous pouvez vous référer à cette page.
[**] L’IP3R est en fait composé de 4 sous-unités. Le modèle le plus couramment accepté est que chaque sous unité est caractérisée par 2 sites de fixation au calcium et un site de fixation à l’IP3. L’un des sites de fixation au calcium est activateur et le second est inhibiteur. L’IP3R s’ouvre lorsque les deux sites activateurs (Ca2+ et IP3) sont liés à leur ligand mais le site inhibiteur est libre. L’augmentation locale de la concentration en calcium à proximité des IP3R ouverts permet la fixation du calcium sur le site inhibiteur (dont l’affinité pour le calcium est inférieure à celle du site activateur). La concentration basale en Ca2+ est ensuite rétablie par l’activité des pompes à calcium sur la membrane du RE : les pompes SERCA. Pour plus de détails sur la structure des IP3R, je vous conseille la revue publiée par Ivanova et collègues [8]. Pour les curieux des différents modèles de l’IP3R proposés à ce jour, allez jeter un œil à la revue publiée par Siekmann et collègues [9].
[***] Les cellules HeLa sont une lignée de cellules cancéreuses qui proviennent d’un prélèvement de métastase sur une patiente atteinte du cancer du col de l’utérus en 1951 ! Ces cellules se divisent indéfiniment et sont de fait qualifiées d’immortelles. Comme vous pouvez le voir avec cet article, mais aussi dans bien d’autres études scientifiques, les chercheurs continuent de nos jours à utiliser les cellules HeLa en recherche pour mieux comprendre comment nos cellules fonctionnent.
[****] Dans cette étude, Thillaiappan et ses collègues montrent que les IP3R dont la trajectoire est non aléatoire sont co-localisés avec les microtubules, protéines du cytosquelette, et se déplacent le long de ces derniers.
[*****] Pour que cet article reste facile à mâcher, j’ai décidé de ne pas vous présenter tous les résultats de l’article de Thillaiappan et ses collègues. Notez que les auteurs ont de plus montré que lorsque la concentration en calcium dans le RE diminue à la suite d’un signal calcique, les protéines STIM (Stromal interaction molecule 1) sont relocalisées au niveau des sites de contact RE-membrane plasmique (MP) et co-localisent avec les IP3R immobiles. Le blocage des protéines STIM au niveau des sites ER-MP engendre son changement de conformation, activant le canal ORAI. Ceci engendre un flux calcique depuis le milieu extracellulaire et une restauration de la concentration en calcium au sein du RE. Ce phénomène se nomme SOCE (de l’anglais store-operated Ca2+ entry) et est un mécanisme partagé par de nombreuses cellules pour un rétablissement rapide de la concentration en calcium du RE. Ce phénomène est essentiel pour réguler la concentration basale en calcium dans la cellule, et donc la capacité de cette dernière à communiquer sous forme de signaux calciques. Le fait que les IP3R immobiles soient localisés au niveau de ces sites de SOCE renforce l’idée de l’existence d’îlots de communication cellulaire ultra-spécialisés, permettant une communication optimale en favorisant l’ouverture des IP3R et le remplissage du RE post-signal.
[#] Vidéo supplémentaire de l’article original disponible ici.
[1] Berridge M. J., The endoplasmic reticulum: a multifunctional signaling organelle. Cell Calcium, 2002. DOI : 10.1016/S0143416002001823. [Publication scientifique]
[2] Maklad A., et al., Calcium Signaling in Brain Cancers: Roles and Therapeutic Targeting. Cancers, 2019. DOI : 10.3390/cancers11020145. [Publication scientifique]
[3] Denizot A., Simulation de la signalisation calcique dans les prolongements fins astrocytaires. 2019. [Manuscrit de thèse de doctorat]
[4] Smith I. F., et al., Single-Molecule Tracking of Inositol Trisphosphate Receptors Reveals Different Motilities and Distributions. Biophysical Journal, 2014. DOI : 10.1016/j.bpj.2014.05.051. [Publication scientifique]
[5] Ferreri-Jacobia M., et al., Translational mobility of the type 3 inositol 1,4,5-trisphosphate receptor Ca2+ release channel in endoplasmic reticulum membrane. Journal of Biological Chemistry, 2005. DOI : 10.1074/jbc.M409462200. [Publication scientifique]
[6] Pantazaka E. & Taylor C. W., Differential Distribution, Clustering, and Lateral Diffusion of Subtypes of the Inositol 1,4,5-Trisphosphate Receptor. Journal of Biological Chemistry, 2011. DOI : 10.1074/jbc.M111.236372. [Publication scientifique]
[7] Smith I. F., et al., Localization of puff sites adjacent to the plasma membrane: Functional and spatial characterization of Ca2+ signaling in SH-SY5Y cells utilizing membrane-permeant caged IP3. Cell Calcium, 2009. DOI : 10.1016/j.ceca.2008.06.001. [Publication scientifique]
[8] Ivanova H., et al., Inositol 1,4,5-trisphosphate receptor-isoform diversity in cell death and survival. Biochimica et Biophysica Acta, 2014. DOI : 10.1016/j.bbamcr.2014.03.007. [Publication scientifique]
[9] Siekmann I., et al., Data-driven modelling of the inositol trisphosphate receptor (IPR) and its role in calcium induced calcium release (CICR). Computational Glioscience, 2019. DOI : 10.1007/978-3-030-00817-8_2. [Publication scientifique]