Cet article a été traduit depuis le site Softbites
Écriture (anglais) : Arthur Michaut
Traduction : Eléonore Pérès
Relecture scientifique : Arthur Michaut
Relecture de forme : Aurélien Schwob
Difficulté :
Temps de lecture : environ 6-7 minutes.
Thématiques : Biologie cellulaire (Biologie) ; Matière molle (Physique)
Publication originale : Grashoff C., et al., Measuring Mechanical Tension Across Vinculin Reveals Regulation of Focal Adhesion Dynamics. Nature, 2010. DOI : 10.1038/nature09198. Disponible sur EuropePMC
« UTILISE TES JAMBES ! » C’est ce qu’on aurait pu te crier la première fois que tu es allé faire de l’escalade. On est tellement habitué à marcher ou à courir qu’on ne pense même pas à la façon dont on le fait. Mais lorsque l’on rencontre un nouvel environnement, comme une pente abrupte par exemple, on réalise souvent qu’il n’est pas si facile de trouver la meilleure stratégie pour se déplacer dans l’espace.
Maintenant, imagine que tu ne mesures que quelques dizaines de microns, sans jambes ni bras, et que tu vis dans un fluide visqueux. Comment te déplacerais-tu ? C’est la question qui intéresse des biologistes spécialistes des mouvements des cellules. En les observant au microscope, ils ont constaté que selon leur type ou leur environnement, elles présentent une grande variété de stratégies pour se déplacer. Cependant, une chose ne change jamais : les cellules ont besoin d’exercer des forces sur leur environnement pour se déplacer. Pour cela, certains types de cellules forment des structures appelées adhérences focales. Elles sont constituées de plusieurs protéines assemblées à l’extérieur de la cellule. Comme de minuscules morceaux de scotch double face, elles permettent à la cellule de se coller à tout ce qui se trouve à proximité (voir Figure 1). Dans un langage un peu plus technique, les adhérences focales relient le squelette moléculaire de la cellule à un substrat (support).
Les cellules peuvent donc exercer des forces sur leur environnement par les adhérences focales. Bien qu’il soit possible de mesurer ces forces à l’extérieur de la cellule en créant un substrat sensible à la force [*], il est beaucoup plus difficile de comprendre ce qu’il se passe à l’intérieur de la cellule. L’accès à ces forces internes est le défi que C. Grasshoff et ses collègues ont relevé dans leur article de 2010.
Pour mesurer une force, la méthode la plus simple consiste à utiliser un ressort. C’est un objet extensible dont on peut, après calibration, déduire la force qui lui est appliquée en mesurant la longueur de son extension. Par conséquent, une force peut être mesurée par la longueur du ressort. Pour mesurer les forces que les adhérences focales exercent sur la cellule, les auteurs ont eu l’idée d’injecter de minuscules ressorts dans les cellules au niveau de ces adhérences focales.
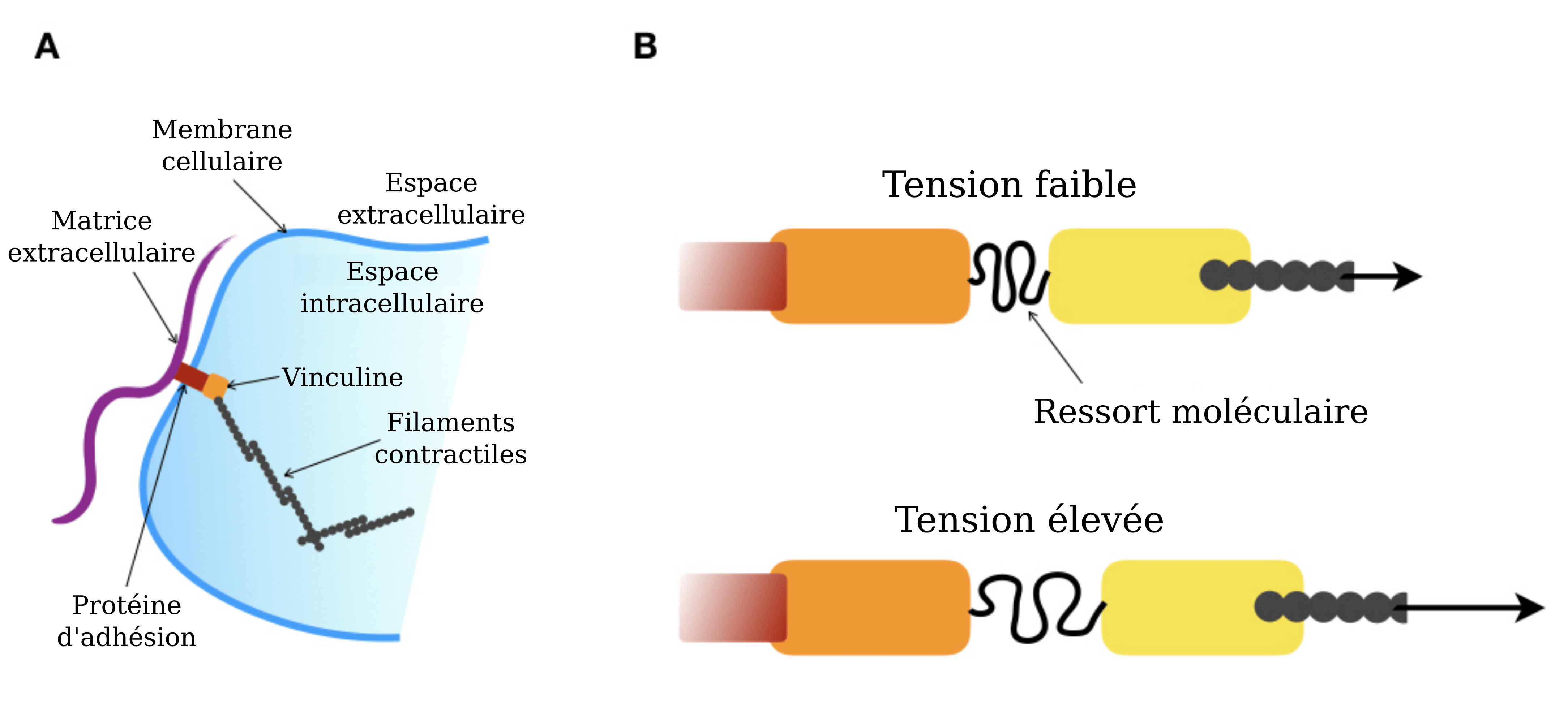
Ils ont ainsi profité d’une protéine de soie produite par une araignée, dont les propriétés sont littéralement celles d’un ressort moléculaire. Grâce à des outils génétiques, une partie du gène de cette protéine de soie peut être insérée dans un gène cellulaire. Les chercheurs ont choisi le gène codant pour la protéine vinculine, qui est une partie essentielle de la structure de l’adhérence focale. En effet, comme le montre la Figure 2A, la vinculine relie les filaments protéiques du squelette cellulaire à l’extérieur de la cellule (la matrice extracellulaire).
Aussi, après transcription du gène et traduction, un bout de la protéine de soie se retrouve au cœur de la protéine vinculine. Grâce à ce protocole, les chercheurs ont donc mis au point une variante artificielle de la vinculine qui comprend un ressort moléculaire dérivé de la protéine de soie, placé en plein milieu de la molécule (voir Figure 2B).
Après avoir vérifié que les cellules génétiquement modifiées pour intégrer le ressort moléculaire se comportent normalement, l’étape suivante a été de mesurer son extension. Cependant, mesurer les distances à l’échelle moléculaire n’est pas une mince affaire. Par exemple, l’extension typique d’un tel ressort est de 6 nanomètres, ce qui est bien inférieur à la résolution des meilleurs microscopes optiques [**]. Pour contourner cette limitation, C. Grasshoff et ses collègues ont profité de l’effet de Transfert d’Énergie de Résonance de Förster (FRET) pour mesurer la distance entre les deux domaines de la vinculine (orange et jaune sur la Figure 2B).
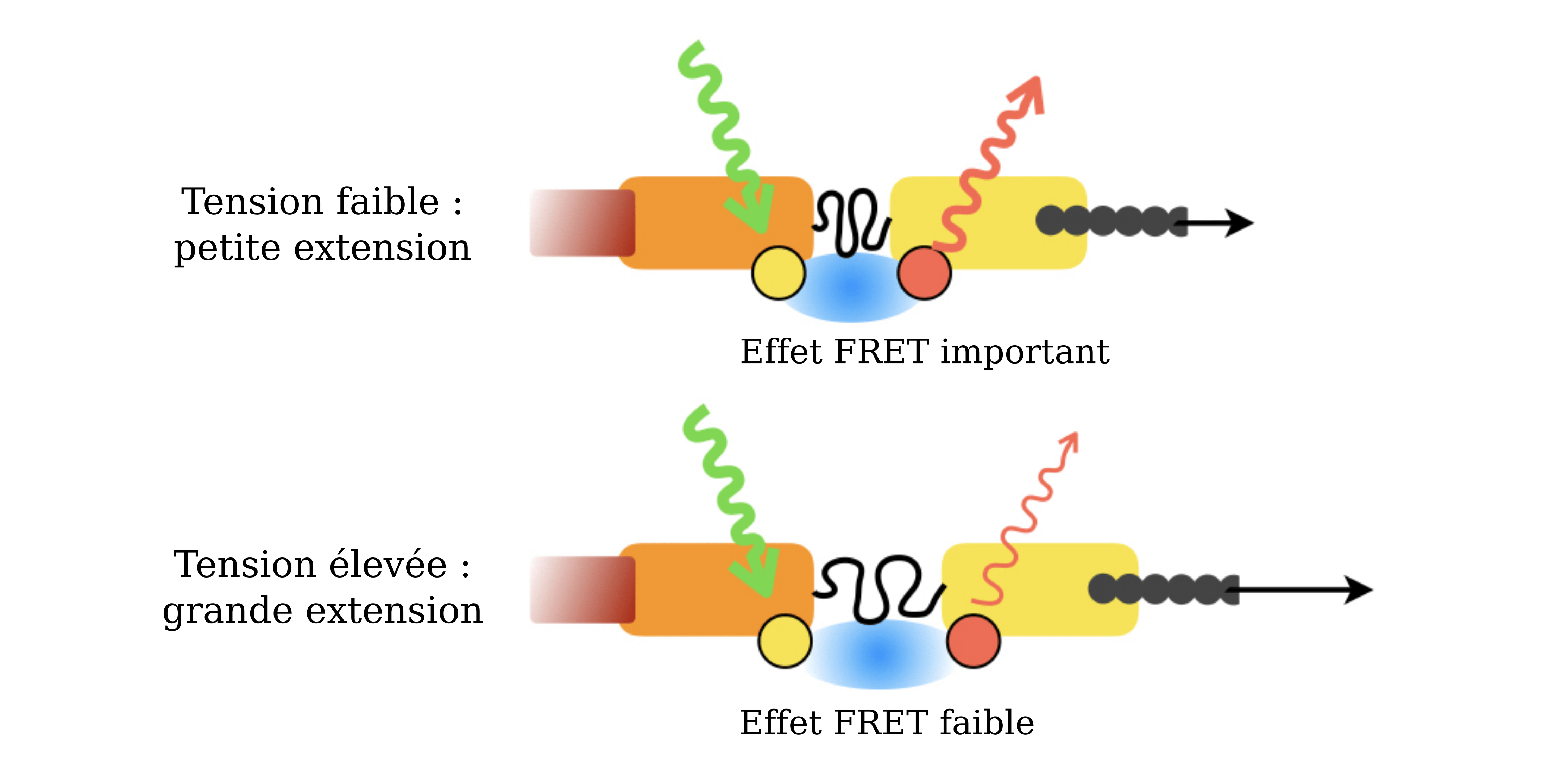
Qu’est-ce que l’effet FRET ? C’est un phénomène qui se produit entre deux molécules fluorescentes très proches dans l’espace. Une molécule fluorescente, lorsqu’elle est excitée par une lumière à une longueur d’onde précise, émet une lumière à une longueur d’onde plus grande. Mais si une deuxième molécule fluorescente est suffisamment proche d’elle, la première molécule (donneuse) peut transférer directement son énergie à la deuxième molécule (acceptrice). Alors, la molécule acceptrice émet de la lumière à son tour, dans une longueur d’onde distincte de la molécule donneuse. Par conséquent, l’intensité du FRET peut être calculée en mesurant les émissions relatives des molécules donneuse et acceptrice. De plus, et c’est important pour cette application, l’efficacité de ce procédé est très sensible à la distance entre le donneur et l’accepteur : plus les molécules sont proches, plus l’intensité d’émission de l’accepteur sera importante. Par conséquent, la distance entre les deux molécules peut être mesurée avec une grande précision (sub-nanométrique) en mesurant l’intensité de l’effet FRET. Les auteurs ont donc choisi de concevoir la protéine vinculine en plaçant le ressort moléculaire entre deux molécules fluorescentes liées aux domaines de la vinculine (Figure 3, cercles jaunes et rouges). Ces molécules fluorescentes sont capables de subir l’effet FRET, permettant de mesurer la distance d’extension du ressort moléculaire.
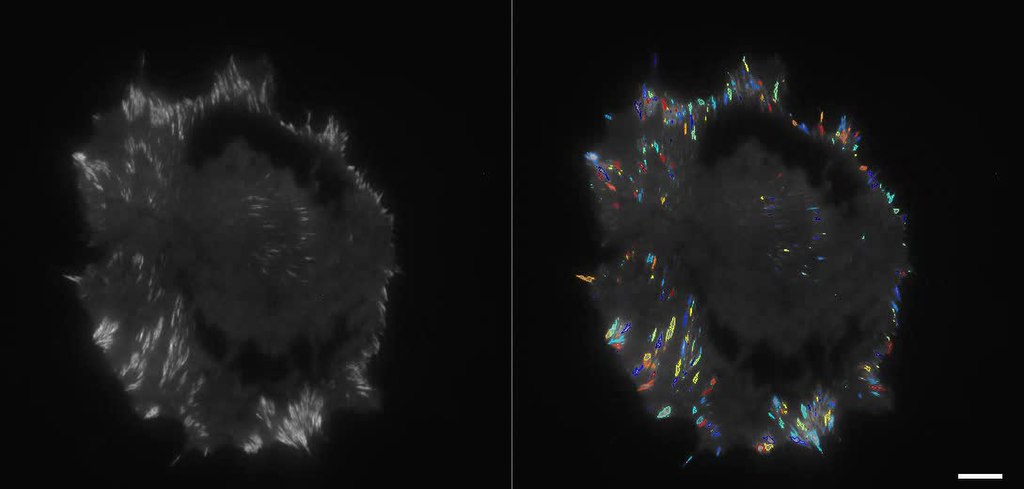
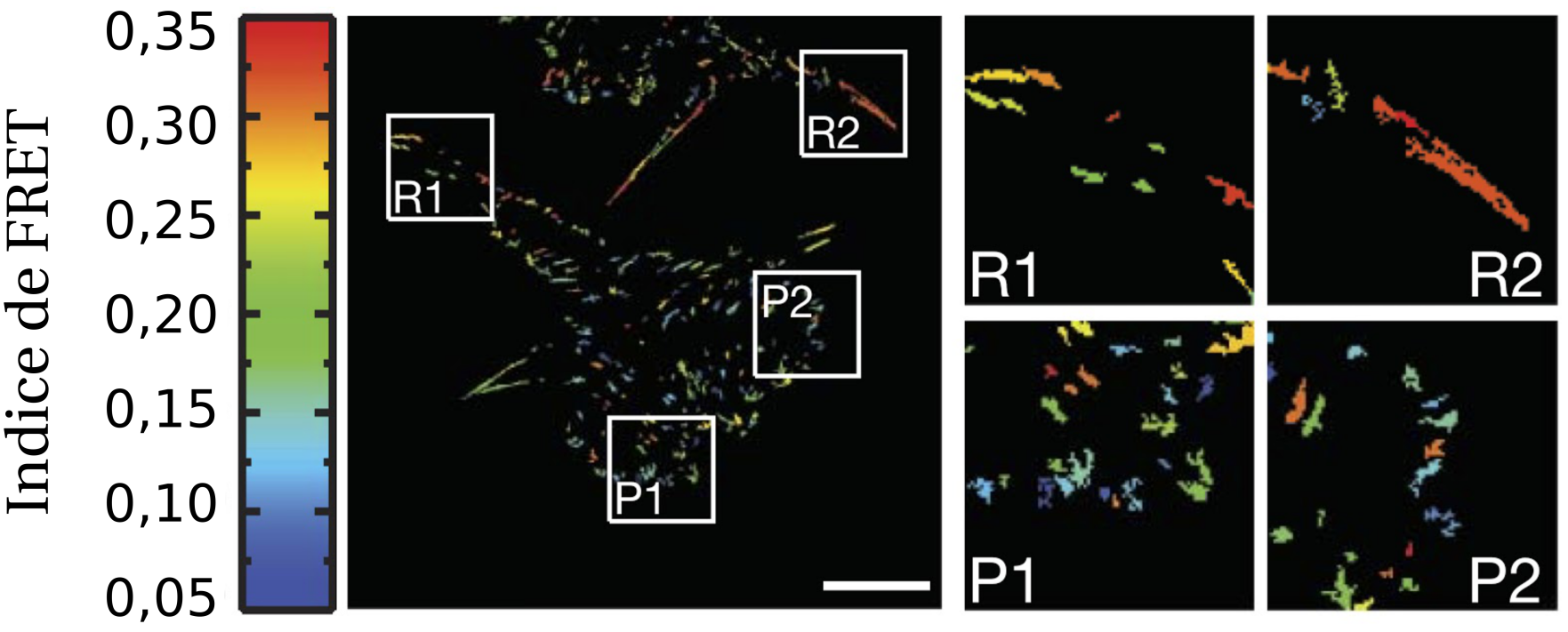
À ce stade, les auteurs disposaient donc d’une méthode pour mesurer l’intensité de la tension entre les molécules de vinculine simplement en examinant l’intensité du FRET. L’idée était de cartographier les tensions à travers les contacts de la cellule sur son environnement. Ils ont observé que soumettre une adhérence focale à une tension élevée entraîne une augmentation de son extension et donc de sa taille, ce qui la soulage de cette tension. De façon peut-être surprenante, ils ont également montré que les régions où le contact de la cellule s’étend sur le support (zones saillantes) sont soumises à une tension supérieure à celle des régions où le contact se rétracte (zones rétractées), comme le montre la Figure 4.
Dans cet article, les auteurs ont donc mis au point une nouvelle technique pour mesurer les forces à l’intérieur des cellules. En réalisant des expériences sur une molécule unique, ils ont même pu calibrer leur ressort moléculaire et relier l’intensité du FRET aux valeurs absolues des forces (de l’ordre de quelques piconewtons [***]). Ils ont ouvert la voie à toute une classe de nouveaux capteurs de force basés sur le FRET avec différentes rigidités, qui peuvent maintenant être utilisés dans les autres structures internes des cellules.
Tout a commencé par l’ajout d’un gène de soie d’araignée dans une cellule. Devenue mutante, elle a aujourd’hui le pouvoir d’éclairer les scientifiques sur les forces existant à l’intérieur des cellules. Mais, comme un autre mutant araignée le sait bien, « un grand pouvoir implique de grandes responsabilités » !
[*] Ces techniques sont appelées Microscopie à Force de Traction (TFM). La déformation d’un substrat calibré (gel ou micropilier) est mesurée pour calculer les forces exercées par la cellule.
[**] Les microscopes optiques classiques ont une résolution typique d’environ 200 nm. Les nouvelles techniques de microscopie optique de haute-résolution atteignent une résolution de quelques dizaines de nanomètres.
[***] Pour vous donner une idée de cet ordre de grandeur : lorsque vous tenez un stylo, disons d’environ 10 g, vous appliquez une force de 0,1 N (newton). Au niveau cellulaire, les cellules exercent sur leur environnement des forces de l’ordre de quelques dizaines de nanonewtons (selon cette étude). Au niveau moléculaire, l’ADN a été manipulé en appliquant des forces dans le même ordre de grandeur que la tension de la vinculine : 1-100 pN (selon cette étude). 1 nN = 10-9 N ; 1 pN = 10-12 N.
Publié le 24/11/2019
Tous droits réservés © 2019 Arthur Michaut/Softbites/Eléonore Pérès/Papier-Mâché
Texte et images, à l’exception des images soumises à droits d’auteurs différents : voir au cas par cas en légende.