Cet article a été traduit depuis le site Softbites
Écriture (anglais) : Karen Kwon
Traduction : Jérémy Ferrand
Relecture scientifique : Léa Lachaud
Relecture de forme : Arthur Michaut
Difficulté :
Temps de lecture : environ 8 minutes.
Thématique : Matière molle (Physique)
Publication originale : Ingebrigtsen T.S. & Tanaka H., Structural predictor for nonlinear sheared dynamics in simple glass-forming liquids. Proceedings of the National Academy of Sciences, 2018. DOI : 10.1073/pnas.1711655115
Vous avez forcément déjà vécu cette expérience : vous tentez de verser du ketchup sur vos frites, mais rien ne sort de la bouteille. Vous tapotez alors le fond à plusieurs reprises plus ou moins énergiquement et… d’un coup, le ketchup en jaillit en recouvrant votre assiette ! Pourquoi un tel désastre ?
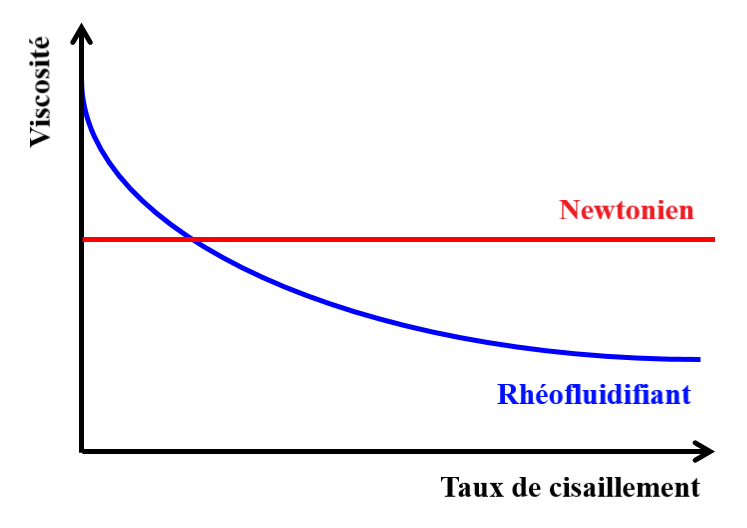
Ce phénomène est appelé rhéofluidification et ne s’observe qu’avec certains fluides qui présentent des propriétés de viscosité particulières. Pour les fluides simples tels que l’eau et l’alcool (aussi appelés fluides newtoniens), la viscosité dépend principalement de la température. Par conséquent, si la température ne change pas, la viscosité demeure la même en toutes circonstances (Figure 1, courbe rouge). Cependant, pour les fluides dits non-newtoniens comme le ketchup, la viscosité peut dépendre des contraintes mécaniques qui s’appliquent sur le fluide.
La contrainte de cisaillement, par exemple, désigne la force surfacique ressentie par un matériau lorsqu’il subit une déformation parallèle à sa surface : c’est-à-dire qui peut être causée par un étirement ou un glissement. Dans les fluides rhéofluidifiants, qui sont un type de fluides non-newtoniens, la viscosité diminue lorsque le taux de cisaillement augmente (Figure 1, courbe bleue). Le ketchup, ainsi que d’autres liquides composés de particules en suspension, comme le sang ou le vernis à ongles, fait partie de cette catégorie de fluides. En tapotant sur la bouteille, vous appliquez à son contenu une contrainte de cisaillement qui fait chuter la viscosité du ketchup, facilitant ainsi son écoulement. Cependant, bien que la rhéofluidification soit un phénomène depuis longtemps observé par les scientifiques, son mécanisme microscopique, pour certains fluides, demeure encore incompris.
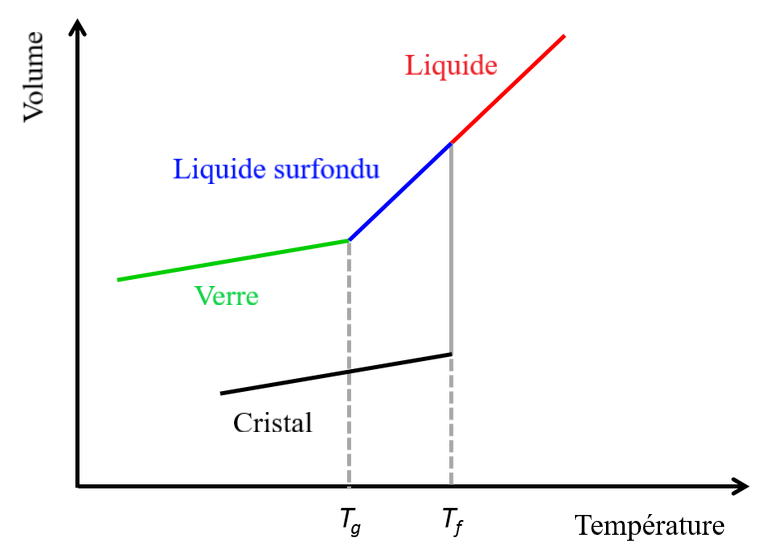
Une autre catégorie de fluides présente un comportement rhéofluidifiant : celle des liquides dits surfondus. Comme illustré sur la Figure 2, lorsque l’on refroidit rapidement un liquide — n’importe lequel — jusqu’à atteindre une température inférieure à son point de congélation, au lieu de se solidifier peu à peu comme le fait l’eau dans un bac à glaçons, il se transforme en un fluide très visqueux, appelé liquide surfondu. Si l’on abaisse encore davantage la température, il arrive un moment où la viscosité devient trop grande pour que le fluide s’écoule sur des temps raisonnables et le liquide surfondu se durcit en une phase solide désordonnée dite vitreuse, car elle s’apparente à du verre [*]. C’est pourquoi les liquides surfondus sont également appelés liquides vitreux.
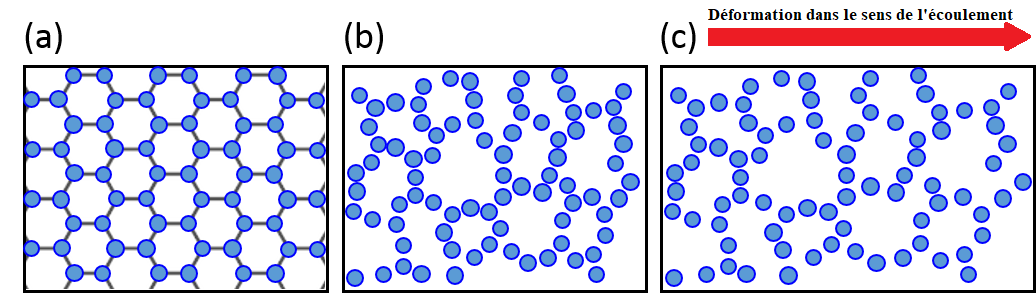
Trond Ingebrigtsen et Hajime Tanaka, chercheurs à l’Institut des Sciences Industrielles de l’Université de Tokyo, ont effectué des simulations de dynamique moléculaire afin de mieux comprendre l’écoulement de liquides surfondus qui sont un type de fluides rhéofluidifiants. Il s’agit d’une méthode de calcul numérique permettant d’étudier les interactions des molécules entre elles. Grâce à ces simulations, Ingebrigtsen et Tanaka ont pu confirmer ce que d’autres scientifiques soupçonnaient déjà auparavant : la rhéofluidification est liée à l’augmentation du désordre dans les liquides, c’est-à-dire aux irrégularités de structure dans la disposition des molécules. En particulier, elle est due au désordre structurel dans la direction de l’écoulement.
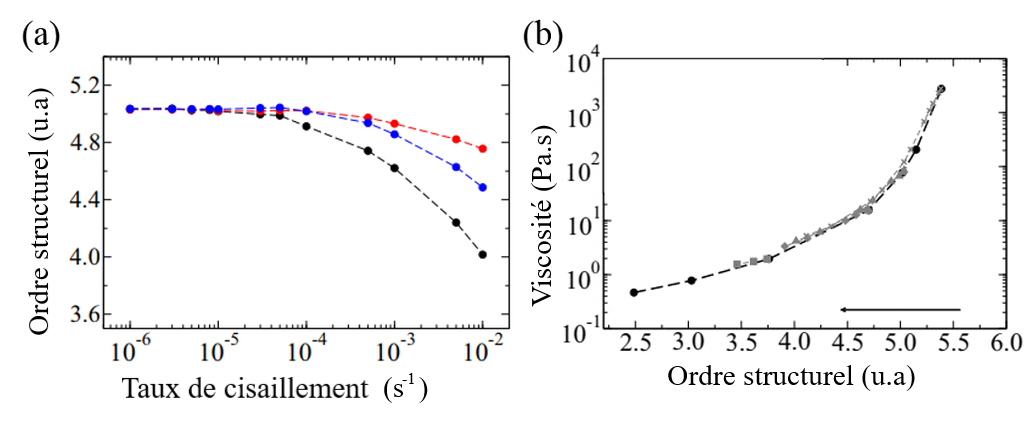
Afin de modéliser les liquides surfondus, les auteurs ont choisi de simuler un système colloïdal où des molécules en suspension interagissent de manière similaire aux molécules des fluides réels. Après avoir vérifié que le système simulé se comporte comme un liquide surfondu (par exemple, que sa viscosité diminue bien avec l’augmentation du taux de cisaillement), ils ont étudié l’origine microscopique de la rhéofluidification dans ce modèle. La simulation a révélé que plus le taux de cisaillement dans le liquide augmente, plus la structure moléculaire devient désordonnée. C’est ce qui est illustré schématiquement sur les Figures 3a et 3b, et quantitativement sur la Figure 4a où l’on voit l’ordre structurel décroître avec le taux de cisaillement.

C’est ce désordre structurel dans la disposition des molécules qui est à l’origine du comportement rhéofluidifiant des liquides surfondus. En effet, comme le montre la Figure 4b, lorsque la structure moléculaire devient plus désordonnée, la viscosité du liquide diminue. Pour comprendre ce résultat, il faut regarder de plus près la Figure 4a. En comparant la courbe noire aux courbes rouge et bleue, on voit que le cisaillement cause un trouble structurel plus important dans la direction de l’écoulement que dans les autres directions transverses. Si on imagine ce qui arrive aux molécules du fluide lorsque l’on applique un cisaillement, on peut interpréter la diminution de viscosité grâce à ce désordre longitudinal. Comme le montre la Figure 3c, le cisaillement appliqué libère de l’espace entre les molécules dans la direction de l’écoulement, laissant à celles-ci la possibilité de se réarranger à mesure que le fluide se répand, ce qui facilite l’écoulement du fluide.
Cette étude met en lumière le mécanisme jusqu’alors méconnu de la rhéofluidification pour des liquides surfondus. Toutefois, Ingebrigtsen et Tanaka précisent que le fondement microscopique de leur observation doit être étudié plus en détails afin d’expliquer de manière plus complète la rhéofluidification. Alors la prochaine fois qu’un désastre se produit sur vos frites, détendez-vous et pensez que vous êtes en train de réaliser une expérience non newtonienne super cool !
[*] Rigoureusement, le verre n’est pas une phase, bien que ce mot soit utilisé pour simplifier l’explication. Le verre est un solide amorphe dont la structure moléculaire est désordonnée ; contrairement à la glace, dont la structure cristalline est régulière. Voir la Figure 3b pour la visualisation d’une structure moléculaire désordonnée.
Publié le 25/02/2020
Tous droits réservés © 2020 Karen Kwon/Softbites/Jérémy Ferrand/Papier-Mâché
Texte et images, à l’exception des images soumises à droits d’auteurs différents : voir au cas par cas en légende.
« la viscosité ne dépend que de la température »-> elle peut dépendre de la pression.
« Cependant, bien que la rhéofluidification soit un phénomène depuis longtemps observé par les scientifiques, son mécanisme microscopique demeure encore largement incompris. »-> ce n’est pas vrai de tous les fluides non newtoniens, pour certains, c’est très largement compris.
« Une autre catégorie de fluides présente un comportement rhéofluidifiant : celle des liquides dits surfondus. Comme illustré sur la Figure 2, lorsque l’on refroidit rapidement un liquide — n’importe lequel — jusqu’à atteindre une température inférieure à son point de congélation, au lieu de se solidifier peu à peu comme le fait l’eau dans un bac à glaçons, il se transforme en un fluide très visqueux, appelé liquide surfondu. Si l’on abaisse encore davantage la température, il se produit une seconde transformation au cours de laquelle le liquide surfondu se durcit en une phase solide désordonnée dite vitreuse, car elle s’apparente à du verre [1]. C’est pourquoi les liquides surfondus sont également appelés liquides vitreux »-> c’est assez étonnament écrit. En fait, du point de vue de la viscosité, il ne se passe rien à la Tg contrairement au coefficient de dilatation thermique.
« Trond Ingebrigtsen et Hajime Tanaka, chercheurs à l’Institut des Sciences Industrielles de l’Université de Tokyo, ont effectué des simulations de dynamique moléculaire afin de mieux comprendre l’écoulement de liquides surfondus, du ketchup et d’autres liquides rhéofluidifiants. « ->Non uniquement des liquides surfondus.
En conclusion, cet article ne dit strictement rien des fluides comme le ketchup. Moralité, je propose de reformuler très largement cet article de vulgarisation.
Merci pour votre commentaire. Nous allons prendre en compte vos remarques, apporter au besoin des précisions à l’article et vous répondre plus en détails bientôt.
Des modifications ont été effectuées sur les points que vous avez soulevés, permettant d’être plus précis sur certains aspects. Nous avons également transmis vos remarques à l’autrice de la version anglaise sur Softbites pour qu’elle puisse également les prendre en considération.