Cet article a été traduit depuis le site Softbites
Écriture (anglais) : Danny Seara
Traduction : Jérémy Ferrand
Relecture scientifique : Léa Lachaud
Relecture de forme : Arthur Michaut
Difficulté :
Temps de lecture : environ 10-12 minutes.
Thématiques : Évolution (Biologie) ; Matière molle (Physique)
Publication originale : Zwicker D., et al., Growth and Division of Active Droplets Provides a Model for Protocells. Nature Physics, 2017. DOI : 10.1038/nphys3984.
Version libre disponible ici (antérieure à la version publiée revue par les pairs)
Au début, il y avait… quoi, exactement ? Si la découverte des origines de la vie représente un enjeu majeur, il s’agit surtout d’un problème difficile. En effet, quand un chercheur regarde une cellule aujourd’hui, il y voit le produit de millénaires d’évolution, mais ne peut accéder aux étapes de l’ingénierie biologique qui ont permis d’aboutir à un tel résultat. Les cellules vivantes se comportent différemment du reste de la matière, alors qu’elles sont pourtant constituées des mêmes éléments chimiques. Une différence majeure, c’est que contrairement à la matière inerte qui est stable, les cellules vivantes évoluent en permanence : on dit qu’elles fonctionnent constamment hors-équilibre.
Pour mieux comprendre ce qu’est l’équilibre d’un système, considérons un verre d’eau glacée, placé dans une pièce chaude. Initialement hors-équilibre, le verre se met aussitôt à échanger de l’énergie thermique avec l’air de la pièce jusqu’à ce que la glace fonde et que toute l’eau se réchauffe à la température de la pièce autour de lui. À ce stade, on dit que l’eau a atteint un état d’équilibre avec son environnement. Les cellules vivantes au contraire, bien qu’elles soient majoritairement constituées d’eau, ne s’équilibrent jamais avec leur environnement. Au lieu de cela, elles consomment et dépensent sans cesse de l’énergie au cours de processus cycliques qui les maintiennent en vie. Comme il est courant de le dire, « l’équilibre, c’est la mort » [*] : l’arrêt de la consommation d’énergie peut être considérée comme une définition de la mort. Ainsi, la façon dont la matière vivante hors-équilibre a pu émerger spontanément d’un environnement non vivant à l’équilibre, constitue un mystère qui a laissé perplexes les scientifiques et les philosophes pendant la majeure partie de l’histoire humaine [**].
Il est impératif pour une jeune cellule en développement de séparer spatialement son fonctionnement interne de son environnement. Cela permet aux réactions spécifiques nécessaires à la vie telles que la réplication du matériel génétique, de se produire en lieu sûr à l’abri de toute perturbation extérieure. Aujourd’hui, les cellules possèdent une membrane sophistiquée qui assure leur protection mais aussi la régulation de ce qui entre et sort à travers elle. Une théorie propose qu’aux prémices de la vie, cette membrane complexe n’ait pas été formée immédiatement mais plutôt que des gouttelettes seraient d’abord apparues au sein d’une soupe primordiale, constituée des espèces chimiques présentes sur la Terre primitive. Ces gouttelettes, susceptibles de croître et de se diviser, auraient servi de premiers contenants à la formation des éléments constitutifs de la vie. Cette idée a été proposée indépendamment par le biochimiste soviétique A. Oparin en 1924 et le scientifique britannique J.B.S. Haldane en 1929 [1]. Oparin a fait valoir que ces gouttelettes auraient été un moyen simple pour les premières cellules de s’isoler de leur environnement, écartant ainsi le scénario où la membrane se forme en premier.
Dans l’article proposé ici, David Zwicker, Rabea Seyboldt et leurs collègues construisent un modèle théorique remarquable et relativement simple sur la façon dont les gouttelettes peuvent imiter le comportement des cellules vivantes. Ils considèrent un fluide à quatre constituants, chacun de nature différente : A, B, C et C’, comme le montre la Figure 1. Les fluides A et B constituent la majeure partie du système, et ne peuvent pas se mélanger l’un à l’autre ; on dit qu’ils sont non miscibles. Ils forment deux phases séparées, de sorte qu’une gouttelette composée principalement de B existe au sein d’un bain composé principalement de A. Ce type de système, de même que des gouttelettes d’huile dans de l’eau, est appelé une émulsion. La plupart du temps, une gouttelette dans une émulsion vit une vie très ennuyeuse : elle peut grossir en fusionnant avec les autres gouttelettes jusqu’à ce que toutes les gouttelettes soient rassemblées, ou bien s’évaporer avec elles jusqu’à ce qu’elles aient toutes disparu. Pourtant ici, en introduisant des réactions chimiques entre les fluides, l’équipe de recherche a pu construire un modèle qui confère aux gouttelettes un comportement bien plus surprenant.
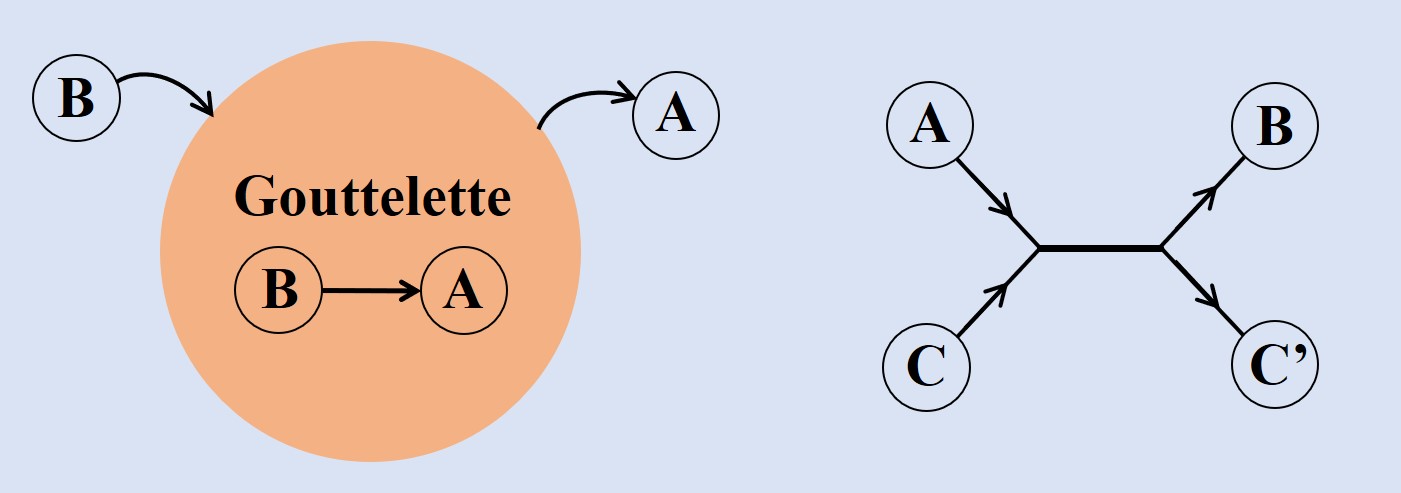
Les réactions chimiques du modèle sont assez simples (voir Figure 1). Le fluide B est susceptible de se dégrader spontanément en fluide A, réduisant la taille de la gouttelette. Alors que le fluide A ne peut pas spontanément se transformer en fluide B (puisque la dégradation spontanée implique de passer d’un état de haute énergie à un état de basse énergie), le fluide C peut réagir avec A pour créer les fluides B et C’. Ainsi cette réaction permet d’alimenter la gouttelette en fluide B.
B → A et A+C → B+C’
Si un mécanisme réapprovisionne (respectivement appauvrit) constamment le milieu en C (respectivement C’), alors C et C’ peuvent être maintenus à des concentrations fixes. Sans C et C’, la goutte entière disparaîtrait en se dégradant dans le fluide A, menant à un état d’équilibre. Mais ici, C et C’ agissent comme un carburant qui éloigne constamment le système de l’équilibre, créant ce que les auteures et auteurs appellent une émulsion active. Les systèmes de matière active comme celui-ci sont adaptés à la description des êtres vivants puisque, comme toute matière vivante, ils présentent la particularité d’être hors d’équilibre en permanence.
Devant la complexité des équations qui décrivent comment les concentrations des fluides A et B évoluent dans le temps, les auteurs ont utilisé une simulation numérique afin de résoudre leur modèle. Cela les a conduits à une observation notable : les gouttelettes qui ne réagissent pas chimiquement avec le fluide environnant ne cessent jamais de croître tant qu’il reste d’autres gouttelettes à avaler à proximité, pourvu qu’elles soient de même nature. Ce processus est appelé mûrissement d’Ostwald [***]. En revanche, les auteurs ont montré que dans un système d’émulsion active, la matière change sans arrêt de nature sous l’effet des réactions chimiques, ce qui supprime le mûrissement d’Ostwald et permet à la gouttelette de maintenir une taille stable.
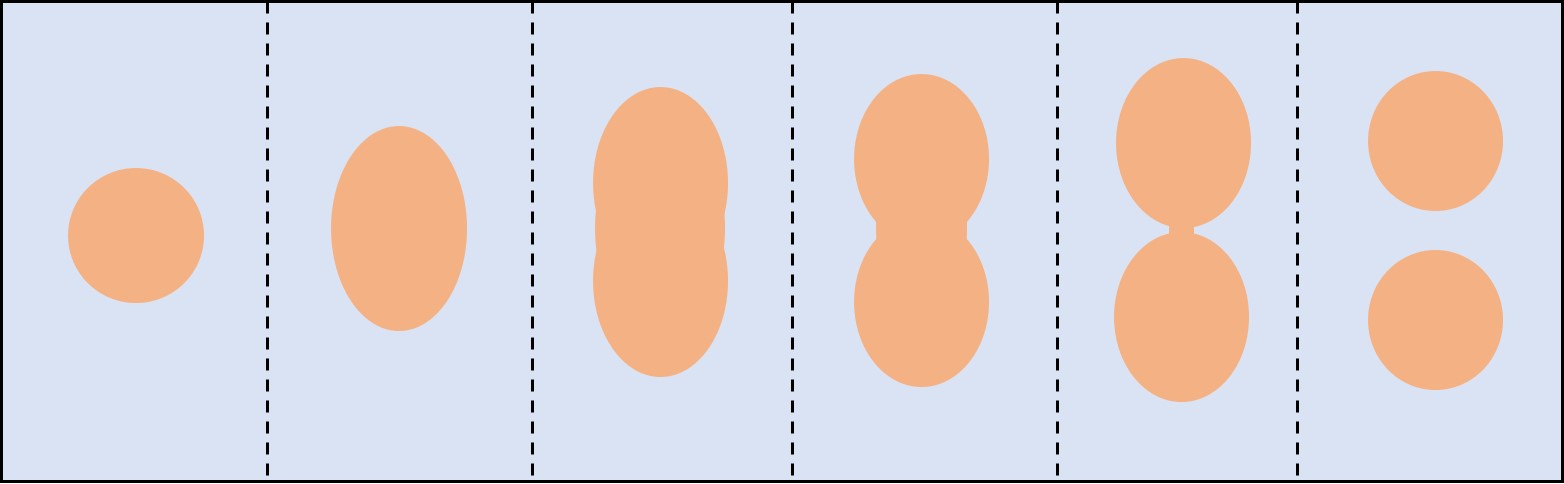
En plus de cette limitation de croissance, les auteur·e·s constatent que les gouttelettes subissent une instabilité de forme qui entraîne leur division spontanée (voir l’illustration de la Figure 2). Ceci est dû à l’alimentation constante en carburant C et C’, qui entretient les réactions chimiques et crée un gradient de concentration au voisinage de la gouttelette. En effet, juste à l’extérieur de celle-ci, la réaction de dégradation B → A provoque un appauvrissement du milieu en B et une abondance de A. En revanche, loin de la gouttelette, la réaction A+C → B+C’ consomme le fluide A et produit le fluide B. Les fluides C et C’ étant maintenus à des concentrations constantes, les fluides A et B atteignent une concentration d’équilibre régie par le taux de réaction de A avec C. On appelle le surplus de B à l’équilibre, loin du voisinage de la gouttelette, sursaturation. Le milieu présente ainsi un excès de B loin de la gouttelette et un défaut de B proche de celle-ci : on a un gradient de concentration, qui engendre un flux de particules du fluide B allant vers la gouttelette. À ce flux convergeant s’oppose un flux divergeant qui résulte de la diffusion de B hors de la gouttelette, de même qu’une pulvérisation de parfum projetée dans un coin d’une pièce diffuse peu à peu à toute la pièce au bout d’un certain temps. Finalement, l’évolution de la taille de la gouttelette dépend du résultat de la compétition entre les flux de particules B entrant et sortant de la gouttelette.

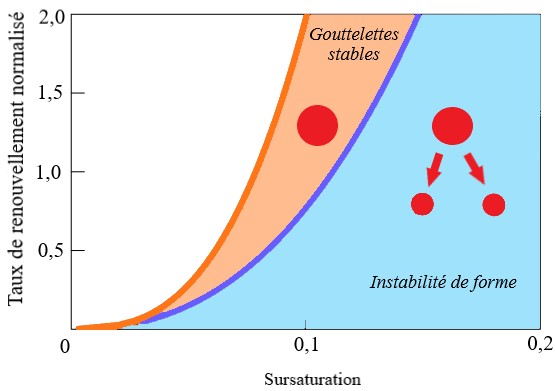
Lorsque les flux entrant et sortant cessent de changer dans le temps, la sursaturation atteint une valeur constante, ainsi que le taux de dégradation B → A. Pour une sursaturation et un taux de dégradation donnés, les auteurs ont calculé l’évolution de la taille de la gouttelette, et ont trouvé trois régimes possibles. 1) Dans un régime où le taux de dégradation est supérieur à la sursaturation, la gouttelette se dissout dans A et finit par disparaître. 2) Dans un deuxième régime, la gouttelette croît jusqu’à une taille limitée puis reste stable, car la sursaturation et la dégradation se compensent exactement. 3) Le troisième régime, le plus intéressant car il suggère celui des cellules vivantes, a lieu lorsque la sursaturation est telle que la gouttelette est davantage alimentée en B qu’elle ne se dégrade en A. Elle se met à grossir jusqu’à ce que sa forme sphérique devienne instable, et qu’une toute petite perturbation suffit à provoquer son étirement puis sa division en deux gouttelettes filles (voir Figure 2). La Figure 3 représente les différents régimes au sein d’un même graphique, localisés dans trois zones différentes selon les valeurs du taux de dégradation et de la sursaturation.
Et c’est tout ! Si vous disposez de deux fluides non miscibles et d’une source de carburant pour convertir l’un en l’autre, la croissance et la division contrôlée des gouttelettes suivront naturellement. Bien que ces gouttelettes soient plus sophistiquées que les gouttelettes d’émulsion ordinaires (sans réaction chimique), elles sont encore loin des microorganismes les plus simples que nous observons aujourd’hui. Il n’y a pas notamment d’information génétique qui se réplique et se propage, et il n’y a pas non plus de structure interne aux gouttelettes. Comme nous l’avons vu plus haut, les gouttelettes n’ont pas les membranes que les cellules modernes possèdent, et qui les protège de leur environnement. Une question qui demeure ouverte est de trouver un système synthétique qui permette de tester le modèle proposé par les auteurs. Néanmoins, ces émulsions actives fournissent un mécanisme possible permettant de déterminer comment les processus à la base de la vie ont pu avoir lieu sans l’infrastructure complexe des cellules modernes.
Bien que de nombreuses questions subsistent, Zwicker et ses collègues ont contribué à une théorie importante, simple et réalisable sur l’émergence de la vie : tout a pu commencer avec une seule goutte.
[*] Ce n’est pas tout à fait vrai. Certains organismes font de l’anhydrobiose : ils sont déshydratés ou réhydratés en fonction de l’environnement, ce qui a pour conséquence d’arrêter ou de démarrer (respectivement) leur propre métabolisme. De plus, certaines bactéries ont un métabolisme ralenti, qui leur permet d’éviter ainsi l’ingestion accidentelle d’antibiotiques. C’est une sorte de stratégie de minimisation des risques.
[**] Par exemple, d’anciens philosophes grecs tels que Démocrite et Aristote croyaient en la théorie de la génération spontanée, réfutée par Louis Pasteur au XIXe siècle.
[***] Le mûrissement d’Ostwald est un phénomène observé dans les émulsions (comme les gouttelettes d’huile dans l’eau, ou la mayonnaise) et même dans les cristaux (comme la glace) qui décrit comment les inhomogénéités du système changent avec le temps. Dans le cas des émulsions, il décrit comment les gouttelettes plus petites se fusionnent en faveur des gouttelettes plus grosses.
[1] Oparin, A. I. « L’origine de la vie ». Moscou : Moscow Worker publisher, 1924 (en russe) ; Haldane, J. B. S. « The origin of life ». Rationalist Annual 148, 3-10 (1929). [Livre de science]
Publié le 01/02/2020
Tous droits réservés © 2020 Danny Seara/Softbites/Jérémy Ferrand/Papier-Mâché
Texte et images.