Chargement de l'article...
Écriture : Élodie Billard
Relecture scientifique : Marion Kennel
Relecture de forme : Flora Gaudillière et Delphine Montagne
Temps de lecture : environ 8 minutes.
Thématiques : Microbiologie et Évolution (Biologie)
Publication originale : Al-Shayeb B., et al., Clades of huge phages from across Earth’s ecosystems. Nature, 2020. DOI : 10.1038/s41586-020-2007-4

Les bactériophages — littéralement mangeurs de bactéries — sont des virus qui infectent les bactéries et sont connus pour avoir généralement des génomes de petite taille. Toutefois, une étude récente vient de découvrir un grand nombre de bactériophages avec des génomes de taille bien supérieure à ceux connus jusqu’alors et que l’on peut trouver dans une dizaine d’écosystèmes sur Terre. L’étude de l’ADN de ces phages a réservé bien des surprises, notamment la présence de certains mécanismes que l’on avait, jusqu’à présent, observé uniquement chez les bactéries. Certains ont même la capacité de détourner les systèmes de défense de leur hôte, ce qui leur permet d’éliminer les phages concurrents.
Une très brève histoire des bactériophages
Les bactériophages, aussi appelés phages, sont des virus qui infectent les bactéries. Ils ont été découverts en 1915 par le bactériologiste britannique Frederick Twort. Ce dernier identifie des colonies de bactéries qui ont un aspect anormal (vitreux). D’autres colonies, mises en contact avec celles-ci, prennent elles aussi ce même aspect vitreux. Deux ans plus tard, en 1917, le franco-canadien Félix d’Herelle va faire la même observation dans des excréments de personnes malades. Il va alors isoler pour la première fois des phages et inventer le terme de bactériophage. Il faudra attendre les années 1940 pour obtenir la première observation de bactériophages au microscope électronique. En 1969, trois chercheurs obtiennent le prix Nobel de physiologie pour leurs travaux sur l’utilisation des phages dans le domaine de la biologie moléculaire. Depuis, les bactériophages sont des outils essentiels pour la recherche et ils ont permis de faire de nombreuses découvertes, comme le séquençage de l’ADN par Frederick Sanger ou encore l’expérience de Crick, Brenner & al.
Des tailles de génome au-delà de celles connues
On classe les bactériophages, et plus généralement les virus, dans le « non vivant » ; le « vivant » étant constitué des Procaryotes (Bactéries et Archées) et des Eucaryotes (organismes constitués de cellules où le matériel génétique se trouve dans un noyau — groupe où se trouvent les humains). Cette distinction vivant / non vivant est un débat toujours en cours entre les scientifiques. Pour se reproduire, les virus et les bactériophages doivent infecter un hôte : ils ne sont pas capables de se multiplier par eux-mêmes. C’est cette caractéristique qui les classe, pour l’heure, dans le monde du « non vivant ». Pour se multiplier, les bactériophages doivent transférer leur matériel génétique (l’ADN le plus souvent) dans leur cellule hôte. Les phages n’infectent qu’une seule sorte de bactérie : ils sont spécifiques.
La grande majorité des bactériophages (environ 95 %) possède un génome ayant une taille de quelques dizaines de kilobases (Kb) [*] (à noter qu’1 base = 1 nucléotide). Le matériel génétique des bactériophages est donc généralement de petite taille (< 200 Kb, soit 200 000 bases). De récentes études ont montré qu’il existait des phages ayant des génomes de taille plus importante, tels les Jumbophages (> 200 Kb, [1]) et les Mégaphages (> 500 Kb, [2]). La question posée par l’étude qui nous intéresse est de savoir si ces phages de grandes tailles sont plus répandus que ce que l’on imagine. Existe-t-il d’autres grands phages ? Qu’infectent-ils ? Où vivent-ils ? Comment fonctionnent-ils ?
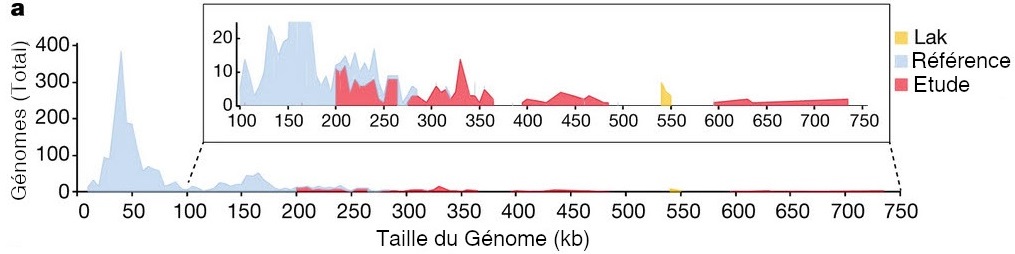
Pour répondre à ces questions, les auteurs de la publication ont travaillé à partir des séquences d’ADN récoltées lors de précédentes études. Ils ont fait un travail minutieux pour les trier, les sélectionner et les valider afin de créer un panorama de bactériophages ayant des tailles de génomes supérieures à 200 Kb. Au final, ils ont obtenu 351 séquences d’ADN de phages de grandes tailles, comprises entre 200 et 735 Kb (Figure 1), qu’ils ont appelés huge phages c’est à dire « énormes phages ». Parmi ces résultats, quatre génomes entiers compris entre 630 et 735 Kb ont été identifiés, soit les plus grands génomes de bactériophages découverts jusqu’à présent. Ces quatre génomes sont entre 12 et 15 fois plus grands que la moyenne habituelle (environ 50 kB, Figure 1). Cette découverte signifie aussi que ces phages ont un génome plus grand que celui de certaines bactéries.
Écosystèmes et bactéries hôtes des huges phages
Les chercheurs se sont ensuite intéressés aux hôtes et aux milieux de vie de ces bactériophages. Pour cela, ils ont classé les phages identifiés en fonction de leurs écosystèmes d’origine. Les scientifiques ont montré la présence des huge phages dans 13 écosystèmes différents (sols, rivières, lacs, océans, ainsi que des échantillons humains, excréments d’animaux, etc.). Ils ont aussi identifié 6 grands groupes bactériens hôtes de ces énormes phages. Parmi ces 6 groupes, 2 sont prédominants :
- le 1er groupe (Firmicutes) a été retrouvé uniquement dans les échantillons humains et animaux (3 écosystèmes sur 13) ;
- le 2e groupe (Protéobactéries) est présent dans quasiment tous les écosystèmes étudiés (12 écosystèmes sur 13).
Les chercheurs ont aussi montré qu’il existerait un lien, une spécificité entre les groupes de phages et leurs hôtes : un groupe de phages infecte un groupe de bactéries spécifique, c’est le lien hôte-virus. De plus, ces énormes phages sont présents dans de nombreux écosystèmes, démontrant ainsi la diversité des écosystèmes colonisés.
Les bactériophages ne sont donc pas la particularité d’un seul écosystème, ni d’un seul hôte. De plus, ceci tend à montrer qu’avoir un génome de grande taille est une caractéristique relativement stable au cours de l’évolution des virus.
Après avoir découvert autant de huge phages, dans autant d’écosystèmes différents, les chercheurs ont donc dû classer et nommer ces nouveaux bactériophages. Ce ne sont pas moins de 10 nouveaux groupes (clades) distincts qui ont été créés. Pour les nommer, les scientifiques ont utilisé un mot signifiant énorme dans les différentes langues maternelles des co-auteurs : Kabirphage, Mahaphage, Biggiephage, Dakhmphage, Kyodaiphage, Kaempephage, Jabbarphage, Enormephage, Judaphage et Whopperphage.
Des virus au métabolisme innovant
À ce stade, les scientifiques avaient déjà fait d’incroyables découvertes : un très grand nombre de phages jamais identifiés auparavant, la taille impressionnante de leur génome, mais aussi la diversité de leurs hôtes et de leurs milieux de vie. Mais les chercheurs sont allés plus loin en tentant d’identifier les gènes présents dans le génome de ces bactériophages. En effet, si leur génome est plus grand, c’est peut-être qu’ils possèdent des gènes que n’ont pas les autres bactériophages. La question est donc de savoir quels sont ces gènes !
La première découverte est la présence étonnante de gènes appartenant au système de défense des bactéries (CRISPR-Cas) ! Cet outil, aussi appelé ciseau génétique, permet aux bactéries de détecter et de couper de l’ADN étranger (notamment celui des virus) intégré dans leur propre ADN, pour l’éliminer. Certains bactériophages décrits dans cette étude portent dans leur génome des gènes permettant de produire les fameux ciseaux génétiques des bactéries. L’hypothèse avancée par les chercheurs est que les bactériophages utiliseraient ce système de défense pour éliminer d’autres bactériophages concurrents qui seraient présents dans le même hôte. Il y aurait donc une réorientation du système de défense des bactéries au bénéfice du virus et qui permettrait de limiter la compétition avec d’autres bactériophages.
La seconde découverte est la présence de gènes impliqués dans le mécanisme de traduction. Habituellement, la petite taille des génomes viraux restreint l’information génétique qu’ils contiennent. Ainsi, ils utilisent principalement la machinerie cellulaire de leur hôte pour la traduction de leur génome. Mais dans le génome des huge phages, des gènes intervenants dans plusieurs étapes de la traduction ont été identifiés. Les huge phages peuvent donc favoriser la traduction de leurs propres protéines au détriment des protéines de leur hôte. Ils ont donc acquis des gènes fondamentaux impliqués dans la traduction et qui sont essentiels aux organismes vivants.
À la frontière du vivant et du non vivant
C’est ce point particulier qui relance le débat sur la frontière entre le vivant et le non vivant. Pour l’instant, les virus sont toujours considérés comme « non vivants » car, sans hôte, ils ne sont pas capables de se multiplier, contrairement aux organismes dits « vivants ». Mais la présence dans le génome des huges phages de gènes impliqués dans la traduction et la similitude de ces gènes viraux avec ceux que l’on peut retrouver chez certaines bactéries montre clairement que la limite entre vivant et non vivant n’est pas si nette.
Les auteurs de l’étude évoquent le terme « d’hybrides » pour qualifier ces huge phages. En effet pour Jillian Banfield (co-autrice de l’étude) « il semble y avoir des stratégies de vie efficaces qui sont hybrides entre ce que nous considérons comme des virus traditionnels et des organismes vivants classiques » [3]. Reste à savoir si c’est une stratégie ancienne, apparue en même temps que les cellules vivantes et que nous n’avions pas encore identifiée, ou récente, en lien avec un épisode d’augmentation de la taille des génomes des bactériophages.
Cette question est encore plus essentielle au regard de la présence de ces phages partout où vivent leurs hôtes, y compris dans le microbiote intestinal humain. Ces phages pourraient avoir une influence sur notre santé en transportant des gènes qui seraient nuisibles aux bactéries de notre microbiote intestinal. Ils pourraient aussi déclencher des maladies et/ou des résistances aux antibiotiques et ce, d’autant plus que d’après Jillian Banfield « plus le génome est grand, […] plus la probabilité de transmission de gènes indésirables aux bactéries des microbiotes humains est élevée » [3].
[*] À titre de comparaison, le génome de l’être humain est de 3,9 milliards de bases (3,9 Gb) et celui de la bactérie E. coli de 4,6 millions de bases (4,6 Mb).
[**] Les génomes de référence représentent l’ensemble des gènes identifiés chez les bactériophages.
[1] Yuan, Y. & Gao, M., Jumbo bacteriophages: an overview. Front. Microbiol., 2017. DOI : 10.3389/fmicb.2017.00403. [Publication scientifique]
[2] Devoto, A. E., et al., Megaphages infect Prevotella and variants are widespread in gut microbiomes. Nat. Microbiol., 2019. DOI : 10.1038/s41564-018-0338-9. [Publication scientifique]
[3] Citations de Jillian Banfield (en anglais).
Écriture : Élodie Billard
Relecture scientifique : Marion Kennel
Relecture de forme : Flora Gaudillière
Temps de lecture : environ 10 minutes.
Thématiques : Microbiologie et Évolution (Biologie)
Publication originale : Al-Shayeb B., et al., Clades of huge phages from across Earth’s ecosystems. Nature, 2020. DOI : 10.1038/s41586-020-2007-4

Les bactériophages — littéralement mangeurs de bactéries — sont des virus qui infectent les bactéries et sont connus pour avoir généralement des génomes de petite taille. Toutefois, une étude récente vient de découvrir un grand nombre de bactériophages avec des génomes de taille bien supérieure à ceux connus jusqu’alors et que l’on peut trouver dans une dizaine d’écosystèmes sur Terre. L’étude de l’ADN de ces phages a réservé bien des surprises, notamment la présence de certains mécanismes que l’on avait, jusqu’à présent, observé uniquement chez les bactéries. Certains ont même la capacité de détourner les systèmes de défense de leur hôte, ce qui leur permet d’éliminer les phages concurrents.
Une très brève histoire des bactériophages
Avant de rentrer dans le vif du sujet, faisons un petit rappel historique sur les bactériophages. Les bactériophages, aussi appelés phages, sont des virus qui infectent les bactéries. Peut-être n’avez-vous jamais entendu parler d’eux. Pourtant leur découverte par le britannique Frederick Twort remonte à plus d’un siècle. En 1915, le bactériologiste observe que certaines colonies bactériennes ont parfois un aspect vitreux, lequel est en lien avec la destruction des cellules bactériennes. Il remarque aussi que cette caractéristique est transmissible à d’autres colonies par simple contact.
En 1917, une seconde observation de bactériophages est faite dans des selles de malades par le franco-canadien Félix D’Herelle. Il va alors isoler les premiers phages et inventer le terme de bactériophage. Il sera aussi à l’origine des premières applications médicales des phages : c’est la naissance de la phagothérapie, c’est à dire l’utilisation des bactériophages pour le traitement de certaines maladies infectieuses d’origine bactérienne. Il faudra attendre les années 1940 pour observer pour la première fois des bactériophages au microscope électronique. En 1969, Max Delbrück, Alfred Hershey et Salvador Luria obtiennent le prix Nobel de physiologie pour des travaux conduits dans les années 60 portant sur l’utilisation des phages comme vecteurs de clonage.
Depuis, les bactériophages sont devenus des outils essentiels pour la recherche et ils ont permis de faire de nombreuses découvertes notamment dans le domaine de la biologie moléculaire. Par exemple, l’utilisation du phage T4 a permis de démontrer que l’information génétique est codée sous forme d’un triplet de nucléotides non chevauchants : les codons (expérience de Crick, Brenner, et al.). Enfin, le britannique Frederick Sanger a reçu le prix Nobel pour avoir séquencé l’ADN d’un phage : c’était le premier génome séquencé !
Des tailles de génome au-delà de celles connues…
Les phages n’ayant pas la possibilité de se reproduire par eux-mêmes, ils doivent infecter un hôte pour se multiplier : ils sont donc dépendants de leur hôte. Cette caractéristique fait que l’on classe généralement les virus (et donc les phages) à part, et non dans le monde vivant constitué des Bactéries, des Archées et des Eucaryotes. Cette distinction vivant / non-vivant est un débat toujours en cours. Mais les récents travaux des chercheurs de l’Université de Berkeley (Californie) viennent brouiller un peu plus cette limite et relancer le débat.
L’une des caractéristiques des phages connus jusqu’alors était qu’ils avaient de petits génomes (< 200 kilobases (Kb) [*], à noter qu’1 base = 1 nucléotide). En effet, la grande majorité des bactériophages (environ 95 %) possède un génome ayant une taille de quelques dizaines de Kb. De récentes études avaient cependant déjà révélé la présence de phages ayant des génomes de taille plus importante, tels que les Jumbophages (> 200 Kb, [1]) et les Mégaphages (> 500 Kb, [2]).
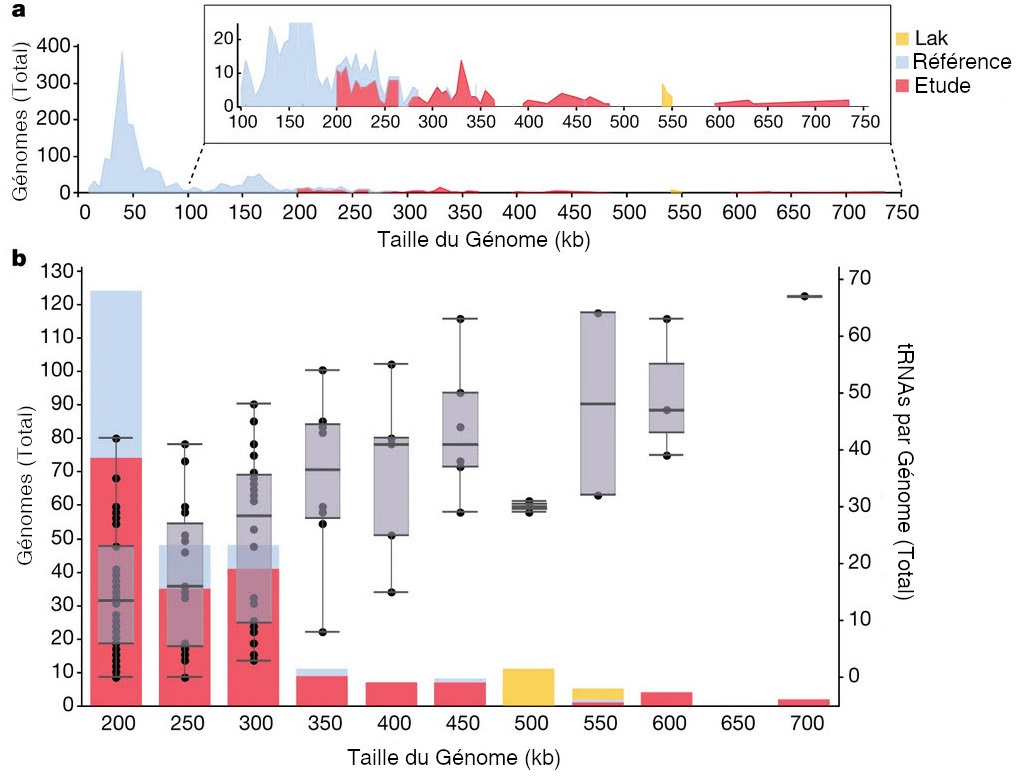
Dans cette étude, les chercheurs sont partis de données de séquençage issues de précédentes recherches faites sur une grande variété d’écosystèmes. Les séquences ont été triées, sélectionnées et analysées afin de recréer un jeu de données de phages ayant des génomes d’une taille supérieure à 200 Kb. Ce travail a permis aux chercheurs de reconstruire 351 séquences de phages d’une taille au moins 4 fois supérieure à la taille moyenne des génomes de phages connus jusqu’alors (génomes de référence — environ 50 kB) (Figure 1a). Parmi ceux-ci, 4 génomes entiers de 634, 636, 642 et 735 Kb ont été identifiés, soit les plus grands génomes de bactériophages identifiés jusqu’à présent, c’est-à-dire des génomes non seulement 15 fois plus grand que la moyenne, mais aussi plus grand que ceux de certaines bactéries. On connaissait déjà des génomes viraux plus grands que ceux de bactéries [3], mais ceux-ci infectent des eucaryotes — par exemple les amibes — et non des bactéries.
Écosystèmes et bactéries hôtes des huge phages
Cette étude a donc également cherché à identifier les hôtes de ces énormes bactériophages et 6 phylums bactériens ont été prédits comme hôtes : les Firmicutes, les Bacteroidetes, les Protéobactéries, les Actinobactéries, les Spirochètes, les Cyanobactéries et les Chlamydias (Figure 2). Parmi eux, 2 phylums sont prédominants, les Firmicutes et les Protéobactéries. La très grande majorité des phages qui infecteraient les Firmicutes ont été identifiés dans les échantillons prélevés dans les intestins humains et animaux, contrairement aux phages qui infecteraient les Protéobactéries que l’on retrouve dans tous les écosystèmes étudiés. En revanche, les 5 génomes ayant les plus grandes tailles dans cette étude n’infecteraient pas ces 2 phylums mais le phylum des Bacteroidetes. Dans l’ensemble, les phages proches phylogénétiquement (d’un même clade) infecteraient, dans la plupart des cas, des bactéries appartenant au même phylum. Il existerait donc un lien, une spécificité entre les clades des phages et les clades de leurs hôtes.
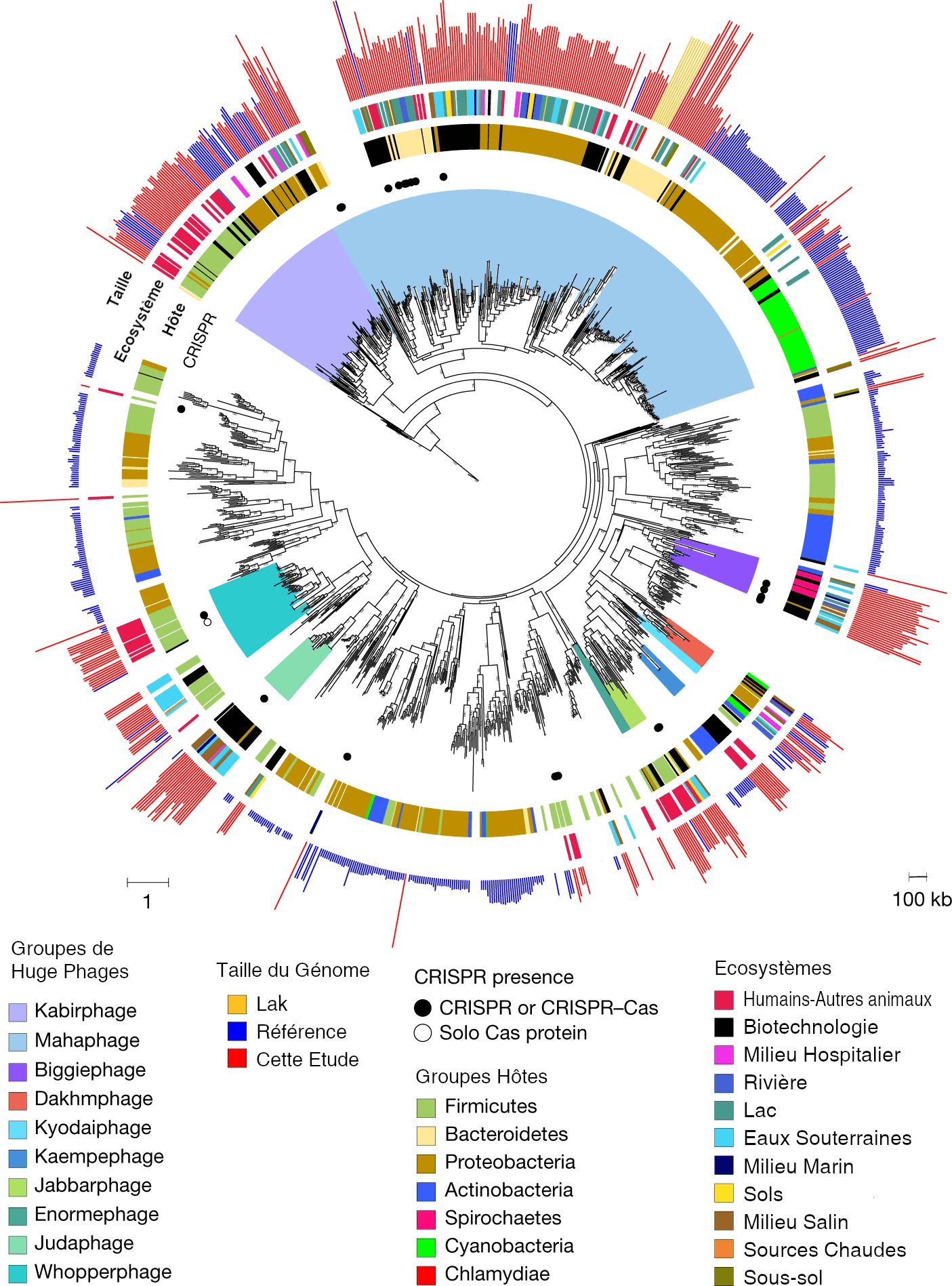
Des virus au métabolisme innovant
Bien que la taille du génome de ces bactériophages soit déjà en soi une découverte importante, la complexité de leurs génomes l’est encore plus. La petite taille des génomes viraux restreint l’information qu’ils contiennent, ainsi ils utilisent principalement la machinerie cellulaire de leur hôte pour la transcription et la traduction de leur génome. Mais ces huge phages ont dans leur génome un nombre important d’ARNt (Acide RiboNucléique de transfert) et d’ARNt synthétases. Par exemple, le génome du plus grand des phages décrit dans cette étude compte jusqu’à 67 ARNt (Figure 1b) alors que d’autres n’en possèdent aucun. De plus, il y a une corrélation entre la taille du génome et le nombre d’ARNt : plus le génome est grand, plus le nombre de d’ARNt augmente (Figure 1b). Les phages peuvent ainsi charger leur propres ARNt avec les acides aminés de leur hôte au cours de la traduction de leur matériel génétique.
À ceci s’ajoute la présence dans leur génome de gènes impliqués dans le détournement de la traduction de leur hôte. En effet, les chercheurs ont identifié la présence de plusieurs molécules qui interviennent à différentes étapes de la traduction (par exemple des facteurs d’initiation, d’élongation, de terminaison et de libération des protéines). Ainsi les phages peuvent favoriser la traduction de leurs protéines au détriment des protéines de leur hôte. Ces huge phages ont donc acquis des gènes fondamentaux intervenant dans la traduction et qui sont essentiels aux organismes vivants.
Enfin, cette étude a aussi permis d’identifier plusieurs systèmes CRISPR-Cas dans ces phages. Ce système est normalement un outil de défense des bactéries et des archées contre les virus. Aussi appelé ciseau génétique, ce système permet aux organismes de détecter et de couper l’ADN étranger intégré à leur génome pour l’éliminer. Certains des bactériophages décrits dans cette étude portent dans leur génome des gènes codant pour des variantes des protéines Cas identifiées chez les bactéries. L’un de ces bactériophages, par exemple, est capable de fabriquer une protéine analogue à la protéine Cas9 (protéine utilisée pour l’édition génétique CRISPR-Cas9), nommé Cas Φ (Phi, notation traditionnellement utilisée pour désigner les bactériophages). L’hypothèse avancée par les chercheurs est que les bactériophages injecteraient leur propre séquence de CRISPR-Cas dans leur hôte, que celui-ci va multiplier, ce qui leur permettrait d’éliminer les virus concurrents qui auraient le même hôte. Il y aurait donc une réorientation du système de défense des bactéries au bénéfice du virus et une limitation de la compétition avec d’autres bactériophages. La présence de ces variants est aussi une bonne nouvelle car elle ouvre la voie à de potentiels nouveaux outils pour l’étude des génomes, en particulier pour les modifications génétique ciblées sur l’ADN. Et ce d’autant plus que les auteurs soulignent que de nombreux gènes présents dans le génome de ces bactériophages n’ont pas encore été identifiés.
À la frontière du vivant et du non vivant
Ces récentes découvertes viennent relancer aujourd’hui le débat sur la frontière entre le vivant et le non vivant. Pour l’instant, les virus ne sont pas considérés comme des êtres vivants car, sans hôte, ils ne peuvent pas se multiplier, contrairement aux bactéries et aux archées. Mais la présence de séquences codant pour des protéines ribosomales et des facteurs de transcription ainsi que la similitude de ces gènes avec ceux que l’on peut retrouver chez certaines bactéries symbiotiques montrent que la limite entre vivant et non vivant n’est pas si nette.
Les auteurs de l’étude évoquent le terme d’hybrides pour qualifier ces huge phages. En effet, pour Jillian Banfield (co-autrice de l’étude) « il semble y avoir des stratégies d’existence efficaces qui sont hybrides entre ce que nous considérons comme des virus traditionnels et des organismes vivants classiques » [4]. Reste à savoir si cette stratégie est issue de lignées anciennes apparues en même temps que les cellules vivantes que nous n’avions pas encore identifiées ou de lignées récentes en lien avec un épisode d’augmentation de la taille des génomes.
Cette question est encore plus essentielle au regard de la présence de ces phages partout où vivent leurs hôtes, y compris dans le microbiote intestinal humain. Ceux-ci pourraient influencer notre microbiote, notamment par le transport de gènes (transfert horizontaux) qui pourraient être nuisibles aux bactéries qui le constituent ou participer au développement de maladies et/ou de résistances aux antibiotiques. Ceci est d’autant plus probable que d’après Jillian Banfield « plus le génome est grand, […] plus la probabilité de transmission de gènes indésirables aux bactéries des microbiotes humains est élevée » [4].
[*] À titre de comparaison, le génome de l’être humain est de 3,9 milliards de bases (3,9 Gb) et celui de la bactérie E. coli de 4,6 millions de bases (4,6 Mb).
[1] Yuan, Y. & Gao, M., Jumbo bacteriophages: an overview. Front. Microbiol., 2017. DOI : 10.3389/fmicb.2017.00403. [Publication scientifique]
[2] Devoto, A. E., et al., Megaphages infect Prevotella and variants are widespread in gut microbiomes. Nat. Microbiol., 2019. DOI : 10.1038/s41564-018-0338-9. [Publication scientifique]
[3] Pérez-Brocal, V et al. A small microbial genome : the end of a long symbiotic relationship? Science, 2006. DOI : 10.1126/science.1130441. [Publication scientifique]
[4] Citations de Jillian Banfield (en anglais).