Écriture : Moïra Courseaux
Relecture scientifique : Clément Fabre et Siham de Goeyse
Relecture de forme : Estelle Nakul et Lucile Rey
Temps de lecture : environ 13 minutes.
Thématiques : Biologie végétale (Biologie), Écologie
Publication originale : Grasset C., et al., The Transformation of Macrophyte-Derived Organic Matter to Methane Relates to Plant Water and Nutrient Contents: Transformation of Macrophyte OC to Methane. Limnology and Oceanography, 2019. DOI : 10.1002/lno.11148

Si vous deviez citer les plus importantes sources de méthane, que répondriez-vous ? La première chose qui nous vient en tête est bien souvent les vaches. Mais saviez-vous que près de 40 % des émissions proviennent des lacs, marais et rivières ? La putréfaction des plantes dans ces milieux participe grandement à la production de ce puissant gaz à effet de serre. C’est d’ailleurs comme cela que le méthane a été découvert ! La production aquatique de méthane a de nombreux secrets à révéler, découvrez-en quelques-uns grâce à cet article.
La production aquatique du méthane
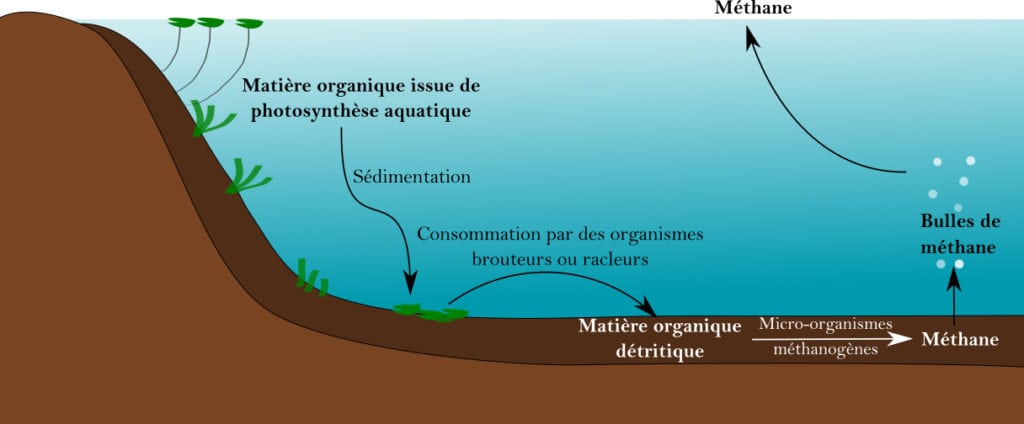
On entend souvent parler du méthane (CH4) en mal : c’est un puissant gaz à effet de serre. Il est produit lors de la digestion du bétail, mais ce que vous ne savez peut-être pas, c’est qu’il peut être produit à partir de plantes. C’est même ce mode de production qui est à l’origine de sa découverte en 1776 par Alessandro Volta ! Ce chimiste et physicien vivait proche de zones humides, dont un gaz issu de la putréfaction des plantes s’échappe. Après un prélèvement de ce « gaz des marais », Alessandro Volta isola sa fraction inflammable qui est aujourd’hui appelée méthane. En effet, au niveau des lacs et des cours d’eau se trouvent des macrophytes (plantes macroscopiques d’eau douce). Les macrophytes vivent en surface comme la fougère aquatique Azolla, ou bien en partie dans et hors de l’eau comme le lotus. Ces plantes sont décomposées en matière organique lorsqu’elles meurent. En conditions anoxiques, c’est-à-dire en absence d’oxygène, cette matière organique peut être transformée en méthane (Figure 1). Cette dégradation est réalisée dans les sols par des microorganismes particuliers appelés méthanogènes. Elle se fait plus ou moins facilement en fonction de la composition des tissus des plantes. Par exemple, si vous vous baladez régulièrement en forêt, vous avez peut-être remarqué que les feuilles des arbres sont décomposées plus vite que des aiguilles de pins. On ne comprend pas encore très bien comment ce processus de méthanogenèse à partir de végétaux fonctionne et de nombreuses questions subsistent : Comment la composition des plantes influence-t-elle la méthanogenèse ? Quel est l’effet du sédiment sur cette production ? La compréhension de cette production de méthane est essentielle pour estimer les émissions de ce gaz à effet de serre par l’ensemble des écosystèmes. Nous pourrions par exemple prédire comment ces émissions évoluent avec le changement climatique. En effet, même si la majorité des émissions de méthane est due aux activités humaines, les milieux aquatiques participent à près de 40 % des émissions globales [1].
Dans la publication présentée ici, C. Grasset et ses collègues nous renseignent sur deux éléments importants :
- les caractéristiques chimiques des macrophytes ont un effet sur la production de méthane ;
- la présence de sédiment favorise la transformation de la matière organique dérivée des macrophytes en méthane.
Reproduire un lac en laboratoire
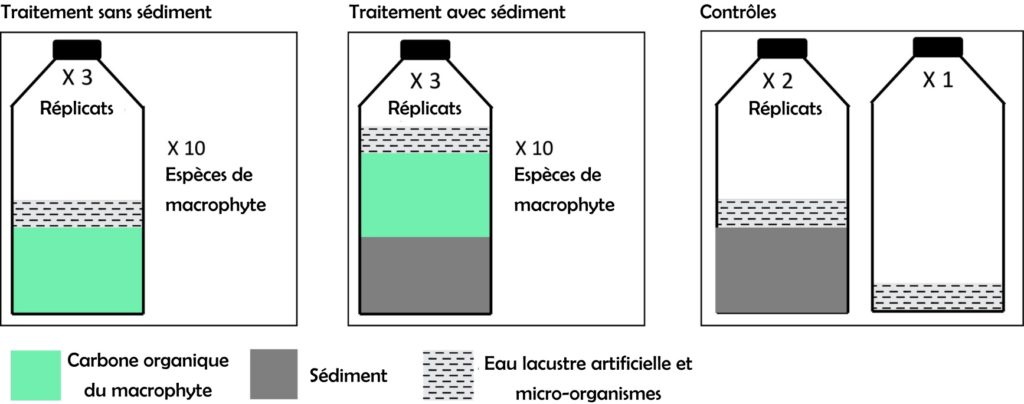
Pour comprendre comment la matière organique issue de la décomposition des plantes est transformée en méthane, les scientifiques se placent dans des conditions similaires à l’environnement naturel. Afin de pouvoir tester spécifiquement l’effet d’un paramètre sur un processus, comme l’effet de la présence de sédiment sur la production de méthane, tous les chercheurs procèdent de la même manière. Ils contrôlent les variables de l’environnement de telle sorte que seul le paramètre d’intérêt diffère entre les différentes conditions de l’expérience. Cela n’étant pas ou peu possible dans un environnement naturel, une solution est d’imiter les conditions naturelles en laboratoire. Dans la publication, les chercheurs ont ainsi fabriqué des mini-lacs très simplifiés dans des bouteilles en verre. Ces microcosmes contiennent chacun : des tissus de plantes aquatiques lacustres (qui vivent dans ou auprès d’un lac), des microorganismes et de l’eau artificielle de lac [**]. Pour répondre aux questions qu’ils se posent, C. Grasset et ses collègues ont mis au point différentes conditions. Pour tester l’effet du sédiment sur la production de méthane, certaines bouteilles contiennent du sédiment et d’autres pas. Pour comprendre l’effet des caractéristiques chimiques des plantes sur leur décomposition et leur transformation en méthane, les auteurs ont comparé dix espèces différentes de macrophytes.
Dans cette étude, pour la condition avec sédiment et la condition sans sédiment, trois réplicats par espèce sont réalisés ainsi qu’un contrôle sans matière organique. Il y a donc pour chacune des dix espèces de macrophytes, trois bouteilles sans sédiment et trois bouteilles avec sédiment (Figure 2).
Grandeurs mesurées et utilisation des données générées
Efficacité de transformation de la plante en méthane
C. Grasset et ses collaborateurs se sont d’abord intéressés à la proportion de carbone de la plante transformée en méthane par rapport à celle transformée en dioxyde de carbone (CO2) [***]. Le carbone issu du méthane et du CO2 n’est plus présent dans les tissus de la plante, ainsi la quantité de méthane et de CO2 mesurée est appelée quantité (de carbone) perdue. Pour calculer l’efficacité de ces transformations, la quantité de carbone organique total de la plante et les concentrations en CO2 et en méthane contenues dans l’air entre l’eau et le bouchon de la bouteille sont mesurées. Savez-vous comment on peut mesurer des concentrations de gaz ? Ici les scientifiques ont utilisé une seringue en plastique (les mêmes que celles utilisées à l’hôpital !) avec laquelle ils aspirent l’air situé en haut de la bouteille. Le contenu de la seringue est ensuite injecté dans un appareil appelé Ultra-Portable Gas Analyzer qui analyse ces gaz à partir de leurs spectres d’absorption, c’est-à-dire à partir des longueurs d’onde de la lumière qu’ils absorbent.
Évolution temporelle de la concentration en méthane
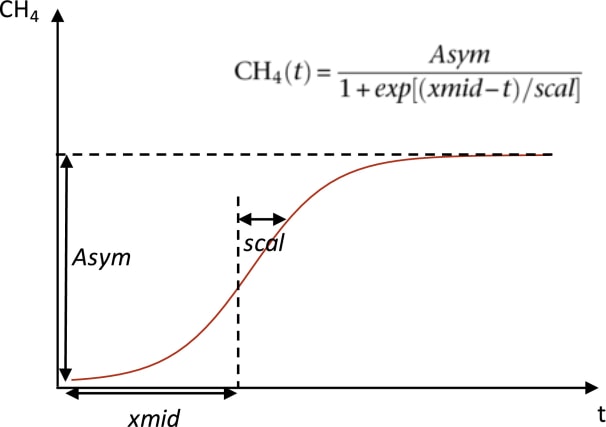
La concentration en méthane est mesurée au cours du temps, ce qui permet de comparer les vitesses de production de méthane dans les différentes conditions de l’expérience. La concentration de méthane en fonction du temps se modélise en théorie par une courbe logistique [****]. Concrètement, les données de concentration permettent d’obtenir une courbe expérimentale par milieu. Il faut ensuite tester si chaque courbe peut être modélisée mathématiquement par une fonction logistique. Une fonction logistique peut s’écrire sous forme d’équation dans laquelle interviennent différents paramètres. Ces paramètres décrivent sa forme, jusqu’où elle monte, à quelle vitesse, à partir de quand il y a un plateau, etc. Le modèle utilisé dans la publication est présenté dans la Figure 3. Il fait intervenir trois paramètres : la production totale de méthane ou hauteur du plateau (Asym), le temps pour lequel la moitié de méthane total a été produit (xmid) et la vitesse à laquelle la production de méthane atteint la production totale, autrement dit la pente à xmid (décrites par scal). Ces paramètres sont calculés (par des logiciels de statistiques) pour chacune des conditions expérimentales, afin de pouvoir les comparer. Cette comparaison permet de mettre en évidence (ou non) les différences de comportements des macrophytes.
Composition des plantes
Pour répondre à leur dernière question, à savoir déterminer l’influence de la composition des plantes sur la méthanogenèse, les auteurs se sont concentrés sur des éléments spécifiques. Ils ont mesuré les concentrations en carbone, azote et phosphore, ainsi que le contenu en eau des tissus des macrophytes avant le début de l’expérience dans les bouteilles. Il est connu que les quantités relatives de nutriments spécifiques — appelé stœchiométrie des nutriments — ont un effet sur la dégradation microbienne des tissus [2]. Le contenu en eau d’un tissu est le pourcentage de la masse du tissu frais qui correspond à de l’eau. Pour le déterminer, il suffit de peser l’échantillon avant et après séchage, puis de calculer à quelle part de masse fraîche correspond la différence entre les masses fraîche et sèche.
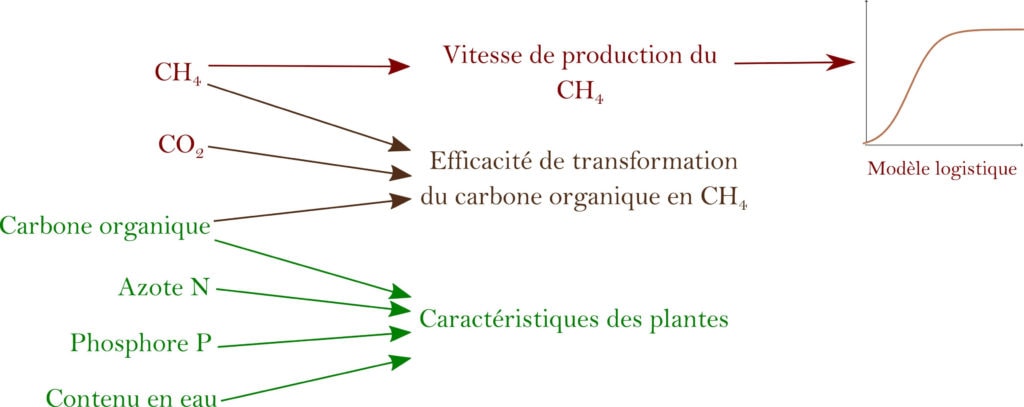
Toutes ces mesures, résumées dans la Figure 4, fournissent des données qui peuvent être comparées entre elles et apportent différentes informations quant à la production de méthane à partir des macrophytes. Les bouteilles de contrôle permettent de connaître la quantité de gaz mesurée qui n’est pas liée à la dégradation des plantes. Par exemple, un problème d’étanchéité du dispositif expérimental permettrait à du CO2 présent à l’extérieur de la bouteille d’y rentrer.
Le sédiment affecterait la production de méthane totale et sa cinétique
C. Grasset et ses collègues ont montré que la présence de sédiment affecte l’efficacité de transformation des plantes en méthane. Pour cela, ils ont exprimé la quantité de carbone organique perdue (transformée en gaz) en pourcentage de la quantité totale de carbone organique de la plante. Sur l’ensemble des milieux, la perte varie entre 1,28 % et 32,7 %, ce qui représente un intervalle relativement grand. Au sein de cet intervalle, les milieux avec sédiment présentent une perte qui varie d’environ 6,11 % à 32,7 %, alors que la perte pour les milieux sans sédiment varie entre 1,28 % et 22,78 %. Suite à des analyses statistiques, les chercheurs concluent que la présence de sédiment favorise la transformation de la matière organique des plantes en méthane. Autrement dit, la production de méthane est plus élevée en présence de sédiment.
Pour expliquer ces résultats, les chercheurs proposent deux hypothèses principales. La première est la mise en place de conditions physico-chimiques favorables à la production de méthane en termes de pH et de potentiel d’oxydo-réduction. La présence de sédiment a pour effet le maintien d’un pH neutre et d’un potentiel d’oxydo-réduction bas, ce qui constitue des conditions favorables à la méthanogenèse. La deuxième hypothèse implique la formation de biofilms de microorganismes. Au sein d’un biofilm, les microorganismes interagissent entre eux et cela pourrait stimuler la méthanogenèse.
La présence de sédiment n’affecte pas seulement la production totale de méthane et de CO2, mais aussi son évolution au cours du temps. Pour le vérifier, les auteurs ont comparé les paramètres des courbes logistiques dont je vous ai parlé. Ces paramètres ainsi que la forme des courbes logistiques leur a permis de mettre en évidence que l’effet de la présence de sédiment sur la vitesse de production de méthane et de CO2 varie entre les espèces de macrophytes. Cela peut être directement lié aux différences de composition des plantes. D’après les auteurs, la présence de sédiment favoriserait la décomposition de certains constituants des macrophytes par rapport à d’autres. La matière organique issue de tissus végétaux de compositions variées ne serait ainsi pas transformée en méthane avec la même cinétique.
Inégalités de production entre les espèces de plantes : habitat et stœchiométrie des nutriments
Les chercheurs ont distingué trois types d’espèces parmi celles étudiées, en fonction de l’habitat de la plante au sein du lac. Les macrophytes sont soit submergés comme les algues, flottants telles que les lentilles d’eau, ou bien émergés comme les roseaux (Figure 5). Ils ont ainsi montré que ce sont les espèces submergées qui présentent la transformation la plus efficace. Ce résultat est cohérent avec une autre étude qui compare les algues à des feuilles terrestres tombées dans l’eau [3]. Les molécules organiques des algues, comparées aux molécules des plantes terrestres, sont dégradées plus facilement en raison de la plus faible présence de tissus structuraux tels que la lignine et la cellulose.

C. Grasset et collaborateurs ont montré que la production de méthane est plus élevée quand la quantité relative de carbone et d’azote (C/N) est faible, c’est-à-dire quand la part d’azote augmente par rapport à celle de carbone. Ce résultat est cohérent avec d’autres études [3, 4]. En effet, si la quantité relative de carbone est élevée, cela signifie que la structure de la matière organique de la plante est plus complexe, et donc… plus difficile à dégrader ! De même, plus la quantité relative d’azote est faible, plus la part des végétaux décomposée et transformée en méthane sera importante. Donc si le ratio C/N est élevé, les microorganismes dégraderaient mieux les tissus et produiraient ainsi moins de méthane. L’étude montre aussi que la production de méthane est plus élevée quand le contenu en eau des plantes est plus important. Cela est cohérent avec les résultats précédents car le contenu en eau des tissus est inversement proportionnel à la quantité de composés structuraux, riches en carbone. Ces composés, tels que la lignine et la cellulose, sont relativement difficiles à dégrader, ce qui limite la méthanogenèse.
Vers une modélisation des émissions aquatiques globales de méthane
Grâce à cette étude, on commence à comprendre quels types de plantes produisent plus de méthane et comment les conditions du milieu favorisent sa production. Cependant, il reste encore beaucoup de travail pour arriver à modéliser les émissions aquatiques de méthane. En effet, les résultats de l’étude ne sont valables que pour les lacs tropicaux. D’autres recherches sont nécessaires avant de pouvoir les généraliser à d’autres types de lacs. En plus de cela, beaucoup de questions ne sont pas encore résolues : quel est l’effet de la composition du sédiment sur la production de méthane ? Quel est le rôle des différentes espèces de microorganismes méthanogènes ? Comment se déroule le transport du méthane du fond des lacs à l’atmosphère ? En effet, il ne faut pas oublier que le méthane est produit dans un milieu sans oxygène, dans le sédiment. Pour qu’il parvienne à l’atmosphère, il doit sortir du sédiment et traverser l’eau du lac. L’hypothèse la plus vraisemblable est un transport par bulles (Figure 1) mais cela requiert une production de méthane importante afin que les bulles puissent se former.
Pour aller encore plus loin, on pourrait envisager l’effet du changement climatique induit par les activités humaines sur la production de méthane. L’article présenté ici montre que le sédiment et la composition des tissus des plantes ont un effet sur la production de méthane. Cependant, de nombreux autres facteurs jouent sur cette production, tels que le pH et les communautés microbiennes [5]. Ces facteurs sont affectés par le changement climatique, tout comme la composition des communautés végétales. Le CO2 est en effet absorbé par les milieux aquatiques et s’y dissout progressivement, produisant de l’acide carbonique qui contribue à diminuer le pH de l’eau. Le changement climatique modifie ainsi des facteurs qui régulent la production de méthane, mais on ne sait pas dans quelle mesure cela impacterait les émissions de méthane globales. Il faudrait faire des études à une plus grande échelle afin de répondre à cette question.
[*] Les organismes brouteurs (comme certains poissons) consomment les algues et les biofilms à la surface du substrat, tandis que les organismes racleurs (comme certains mollusques) raclent de manière homogène la surface du substrat.
[**] Eau (stérile) enrichie en azote, potassium et phosphore imitant la composition d’une eau de lac naturelle, mais sans les micro- et nano-organismes.
[***] Le CO2 est le second gaz contenant du carbone produit lors de la décomposition des tissus [4].
[****] Représentation graphique d’une fonction logistique, qui est elle-même une fonction mathématique. Une courbe logistique est une courbe en forme de S telle que celle de la Figure 3.
[1] Houghton J.T., et al. IPCC, 2001., « Climate Change 2001: The Scientific Basis. Contribution of Working Group I to the Third Assessment Report of the Intergovernmental Panel on Climate Change ». Cambridge University Press. [Livre de science]
[2] Enriquez S., et al., Patterns in decomposition rates among photosynthetic organisms: the importance of detritus C:N:P content. Oecologia, 1993. DOI : 10.1007/bf00566960. [Publication scientifique]
[3] West W. E., et al., Effects of algal and terrestrial carbon on methane production rates and methanogen community structure in a temperate lake sediment. Freshwater Biology, 2012. DOI : 10.1111/j.1365-2427.2012.02755.x. [Publication scientifique]
[4] Acharya C. N., Studies on the anaerobic decomposition of plant materials: The decomposition of plant substances of varying composition. The Biochemical journal, 1935. DOI : 10.1042/bj0291459. [Publication scientifique]
[5] Valentine D. W., et al., Ecosystem and physiological controls over methane production in northern wetlands. Journal of Geophysical Research, 1994. DOI : 10.1029/93JD00391. [Publication scientifique]
Chargement de l'article...
Écriture : Moïra Courseaux
Relecture scientifique : Clément Fabre et Siham de Goeyse
Relecture de forme : Estelle Nakul et Lucile Rey
Temps de lecture : environ 9 minutes.
Thématiques : Biologie végétale (Biologie), Écologie
Publication originale : Grasset C., et al., The Transformation of Macrophyte-Derived Organic Matter to Methane Relates to Plant Water and Nutrient Contents: Transformation of Macrophyte OC to Methane. Limnology and Oceanography, 2019. DOI : 10.1002/lno.11148

Si vous deviez citer les plus importantes sources de méthane, que répondriez-vous ? La première chose qui nous vient en tête est bien souvent les vaches. Mais saviez-vous que près de 40 % des émissions proviennent des lacs, marais et rivières ? La putréfaction des plantes dans ces milieux participe grandement à la production de ce puissant gaz à effet de serre. C’est d’ailleurs comme cela que le méthane a été découvert ! La production aquatique de méthane a de nombreux secrets à révéler, découvrez-en quelques-uns grâce à cet article.
Une découverte (d)étonnante
Alessandro Volta, chimiste et physicien, vivait proche de marais desquels s’échappe un gaz appelé gaz des marais. En 1776, Volta préleva des échantillons de ce gaz dans une zone marécageuse d’une île du lac Majeur en Italie, puis en isola la fraction inflammable qu’il nomma air inflammable. Le terme méthane est proposé près d’un siècle après l’isolation de ce gaz, en 1866, par August Wilhem von Hofmann. Vous en avez peut-être déjà fait l’expérience, une bougie ou une allumette allumée en présence de méthane entraîne son embrasement comme illustré par la Figure 1. Bien entendu, ne tentez pas de reproduire l’expérience chez vous. À noter qu’il n’y a pas que du méthane qui s’échappe des marais, le gaz des marais contient aussi du sulfure d’hydrogène et du dioxyde de carbone (CO2). Mais au fait, d’où viennent ces gaz ?

Production aquatique de méthane
On entend souvent parler du méthane en mal : c’est un puissant gaz à effet de serre. Il est produit lors de la digestion du bétail, mais ce que vous ne savez peut-être pas, c’est qu’il peut aussi être produit à partir de plantes. En effet, dans les lacs et les cours d’eau se trouvent des plantes appelées macrophytes. Ce nom signifie que ces plantes (phytes) sont visibles à l’œil nu (macro). Elles vivent en surface comme la fougère aquatique Azolla, ou bien en partie dans et hors de l’eau comme le lotus. Ces plantes sont décomposées en matière organique lorsqu’elles meurent. En absence d’oxygène, cette matière organique peut être transformée en méthane (Figure 2). Cette dégradation est réalisée dans les sols par des microorganismes particuliers appelés méthanogènes.
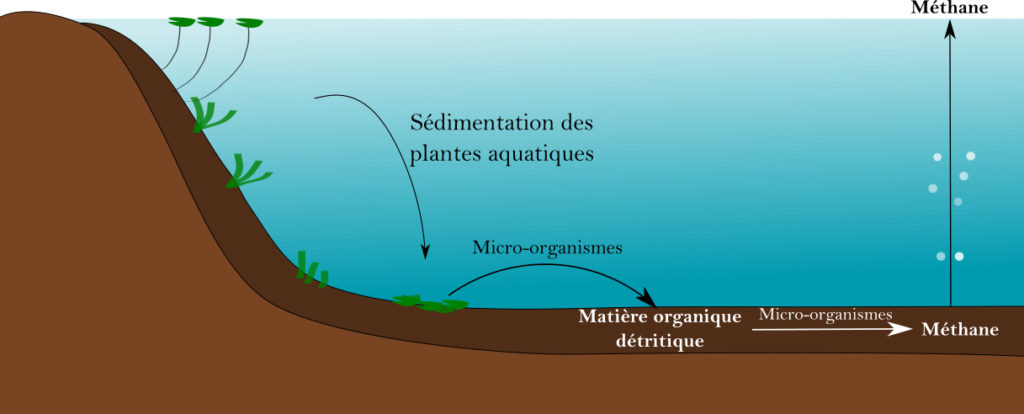
En quête de la compréhension de la méthanogenèse aquatique
Dit comme ça, on a l’impression qu’on comprend comment ça fonctionne, mais il reste beaucoup d’éléments inconnus ! Toutes les plantes peuvent-elles être transformées en gaz ? Comment la composition des plantes influence-t-elle la production de méthane ? Quel est l’effet du sédiment, de la température, du pH (unité de mesure de l’acidité) sur cette production ? Comment le méthane est-il transporté des sols à l’atmosphère ? Dans la publication présentée ici, C. Grasset et ses collègues apportent des éléments de réponse en montrant que la composition des plantes a un effet sur la quantité de méthane produite.
Reproduire un lac en laboratoire
Pour comprendre comment la matière organique issue de la décomposition des plantes est transformée en méthane, les scientifiques se placent dans des conditions similaires à l’environnement naturel (le lac). Afin de tester spécifiquement l’effet d’un paramètre (ici l’espèce de plante) sur un processus (ici la méthanogenèse), tous les chercheurs procèdent de la même manière. Ils contrôlent l’environnement de telle sorte que seul le paramètre d’intérêt diffère entre les différentes conditions de l’expérience. Cela n’étant pas ou peu possible dans un environnement naturel, une solution est d’imiter ces conditions naturelles en laboratoire.
Dans l’article présenté ici, les chercheurs ont ainsi concocté des mini-lacs très simplifiés dans des bouteilles en verre. En voici les ingrédients : du sédiment, des plantes vivant dans ou près de lacs, de l’eau artificielle de lac [*] et des microorganismes (Figure 3). Pour comprendre l’effet des caractéristiques des plantes sur leur décomposition et leur transformation en méthane, les auteurs ont comparé dix espèces différentes de plantes aquatiques. Ils ont étudié différentes caractéristiques des tissus de ces plantes : les concentrations de carbone, d’azote et de phosphore.
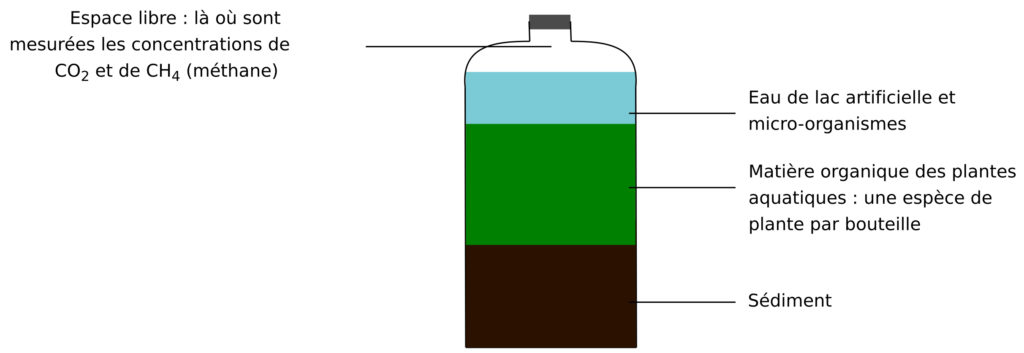
Comment mesurer et comparer la méthanogenèse des différentes plantes ?
Lors de sa décomposition, les atomes de carbone (C) de la plante peuvent se retrouver dans des molécules de méthane (CH4) ou bien de dioxyde de carbone (CO2). Après avoir mesuré la production de méthane et de dioxyde de carbone, C. Grasset et ses collègues ont calculé l’efficacité de transformation de la plante en méthane, c’est-à-dire la proportion de la plante transformée en méthane, par rapport à celle transformée en CO2. Cette grandeur est ensuite utilisée pour faire des comparaisons entre les différentes espèces de plantes.
Inégalités de production : habitat et composition de la plante
Les plantes vivant au bord ou dans les lacs sont classées en plusieurs types. Celles qui sont submergées (sous l’eau) comme les algues ; flottantes comme les lentilles d’eau ou les nymphéas ; ou bien émergées, avec une partie hors de l’eau comme les roseaux (Figure 4). En utilisant cette classification et les données d’efficacité de transformation obtenues grâce à différentes mesures faites dans les lacs artificiels, les chercheurs ont montré qu’une proportion plus importante des plantes submergées est transformée en méthane par rapport à celle des plantes flottantes et émergées. La transformation en méthane des espèces submergées est donc la plus efficace. Comment expliquer ce résultat ?
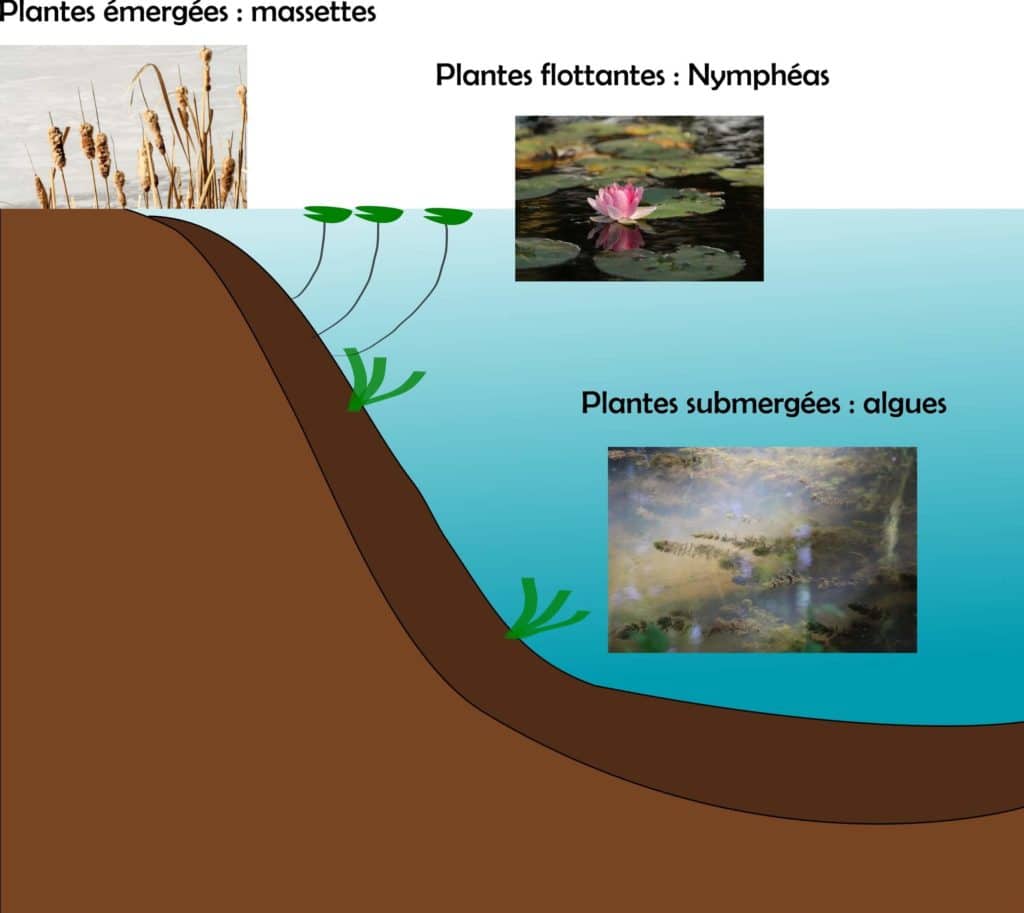
Une autre découverte permet de donner un début d’explication. Une équipe de recherche différente avait déjà montré que les proportions de carbone et d’azote ont un effet sur la dégradation microbienne des plantes [1]. C’est un peu comme avec les gâteaux, si on change les proportions on se retrouve avec un résultat différent de celui attendu (mettre une pincée de sucre et 100 g de sel dans un brownie ne satisfera pas vos convives). Ici, C. Grasset et ses collaborateurs se sont également intéressés au lien entre les caractéristiques chimiques des plantes et leur efficacité de transformation en méthane. La question était alors de savoir si la production de méthane était également impactée par la composition chimique des plantes. À partir des mesures des concentrations en divers éléments des tissus et des valeurs d’efficacité de transformation en méthane, les scientifiques ont montré que la production de méthane est plus élevée quand la concentration en azote de la plante est élevée par rapport à celle du carbone.
Ces deux résultats peuvent alors être mis en relation autour du fait suivant : les plantes ont des compositions différentes selon qu’elles vivent dans l’air ou dans l’eau, et ce pour des causes propres à chacun de ces milieux.
En effet, les plantes qui vivent sous l’eau ont besoin de moins de maintien car l’eau est un milieu qui porte plus que l’air. À la piscine ou à la mer, si vous vous allongez sans rien faire, vous flottez, alors que dans l’air, ça n’est pas vraiment possible. Ainsi, les plantes vivant hors de l’eau présentent plus de tissus de maintien, tels que la lignine, par rapport aux plantes vivant sous l’eau. Cela leur permet de se tenir droites. Ces tissus de maintien ont une composition différente des autres tissus. Ils contiennent plus de composés dits structuraux, qui sont eux-mêmes composés d’une quantité de carbone plus élevée par rapport à celle d’azote. Les tissus ont ainsi une structure plus complexe, et donc… plus difficile à dégrader ! En suivant ce raisonnement, les plantes submergées ont moins de tissus de maintien, c’est-à-dire moins de carbone par rapport à la quantité d’azote, et sont donc plus faciles à dégrader. Ceci résulterait en une production plus importante de méthane, ce qui coïncide avec les résultats expérimentaux !
La quête n’est pas terminée !
Grâce à l’étude présentée ici, les scientifiques lèvent le voile sur la production aquatique de méthane. Comprendre cette production permettrait d’estimer avec plus de précision la quantité de méthane émis par les différents milieux aquatiques. Pour en arriver là, il reste encore beaucoup de chemin à parcourir. En effet, les résultats de l’étude ne sont valables que pour les lacs tropicaux. D’autres recherches sont nécessaires avant de pouvoir les généraliser à d’autres types de lacs. En plus de cela, beaucoup de questions ne sont pas encore résolues : quel est l’effet de la composition du sédiment sur la production de méthane ? Quel est le rôle des différentes espèces de microorganismes méthanogènes ? Comment se déroule le transport du méthane du fond des lacs à l’atmosphère ? En effet, il ne faut pas oublier que le méthane est produit dans un milieu sans oxygène, dans le sédiment. Pour qu’il parvienne à l’atmosphère, il doit sortir du sédiment et traverser l’eau du lac. L’hypothèse la plus vraisemblable est un transport par bulles (Figure 1) mais cela requiert une production de méthane importante afin que les bulles puissent se former.
De plus, les chercheurs pourraient envisager de prédire l’effet du changement climatique induit par les activités humaines sur la production de méthane. Le changement climatique impacte des éléments qui régulent la production de méthane, de la même manière que la température d’un four impacte la cuisson d’un gâteau. Dans quelle mesure la production de méthane aquatique va-t-elle être affectée par le changement climatique ? Répondre à cette question nécessite de continuer d’étudier ce phénomène connu depuis des siècles, afin de comprendre quels paramètres physico-chimiques et quels organismes contrôlent la production de méthane. Les recherches continuent sur ce sujet, une étude récente démontre que des espèces particulières de bactéries, les cyanobactéries, produisent elles aussi du méthane [2]. Par ailleurs, le méthane est un gaz à effet de serre, il contribue donc au réchauffement climatique. Ainsi, plus il y a de méthane dans l’atmosphère, plus il y a de réchauffement. Plus il y a de réchauffement, plus il y a de méthane libéré des sols. Mais y a t-il aussi plus de méthane produit par les milieux aquatiques ? La nature est loin de nous avoir dévoilé ses secrets, la liste des ingrédients de la recette n’est pas complète.
[*] Eau (stérile) enrichie en azote, potassium et phosphore imitant la composition d’une eau de lac naturelle, mais sans les micro et nano-organismes.
[1] Enriquez S., et al., Patterns in decomposition rates among photosynthetic organisms: the importance of detritus C:N:P content. Oecologia, 1993. DOI : 10.1007/bf00566960. [Publication scientifique]
[2] Bižić M., et al., Aquatic and terrestrial cyanobacteria produce methane. Science Advances, 2020. DOI : 10.1126/sciadv.aax5343. [Publication scientifique]

Bonjour,
Je trouve cet article intéressant. Je l’ai lu attentivement et j’ai apprécié.