Chargement de l'article...
Écriture : Eléa Héberlé
Relecture scientifique : Aude Grézy
Relecture de forme : Yann Méheust et Emmanuelle Lebeau
Temps de lecture : environ 12 minutes.
Thématiques : Génétique & Épigénétique (Biologie)
Publication originale : Wu T. P., et al., DNA methylation on N6-adenine in mammalian embryonic stem cells. Nature, 2016. DOI : 10.1038/nature17640
Version libre disponible ici.
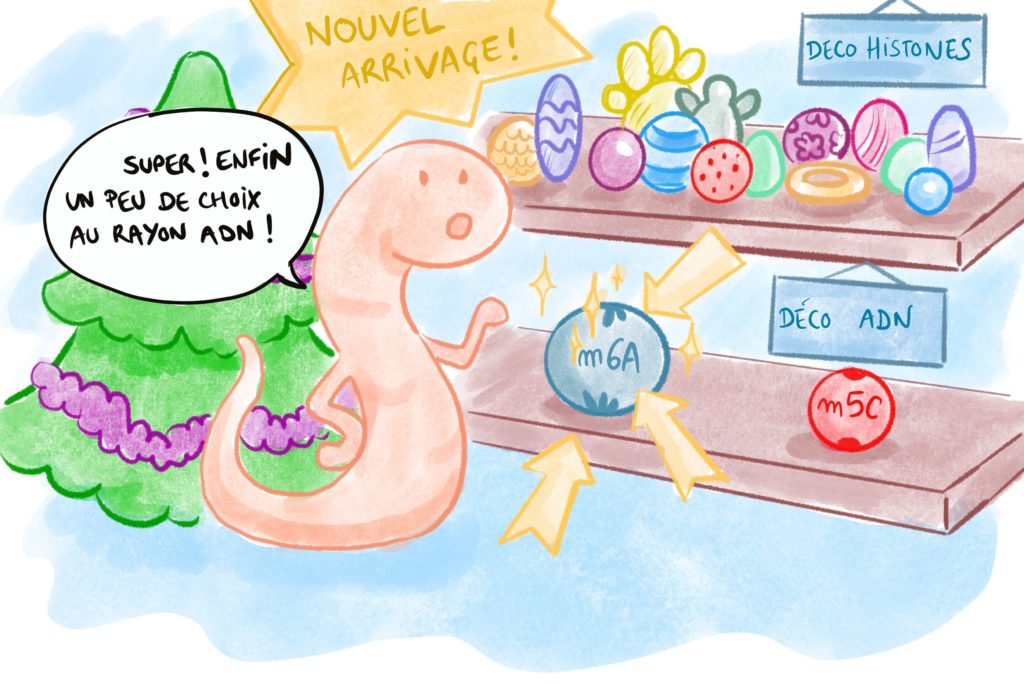
Les scientifiques ont découvert une nouvelle façon de réguler l’expression des gènes. Grâce à une nouvelle décoration dans les cellules de souris, la 6-méthyladénine, on peut éteindre des gènes et empêcher des éléments génétiques de sauter partout et de mettre la pagaille ! Car en biologie, il y a l’étude des gènes — la génétique — et l’étude de leur régulation : l’épigénétique où il s’agit plus ou moins de comprendre de quelle façon le génome est décoré, comme des boules sur un sapin de Noël. De quoi réjouir la communauté scientifique, car ce n’est pas tous les jours qu’on trouve une nouvelle boule à mettre sur le sapin !
Par delà le génome, l’épigénome
Au cœur de chacune de nos cellules se trouve la molécule d’ADN ou acide désoxyribonucléique. Mais oui, vous savez, cette molécule que l’on cherche pour résoudre un crime dans les enquêtes policières parce que c’est la « signature » de chaque personne ! Les quatre briques avec lesquelles sont construites cette molécule, A (Adénine), T (Thymine), C (Cytosine), G (Guanine) se succèdent invariablement, formant parfois des gènes. Chaque gène porte l’information permettant de créer des protéines ou des enzymes, qui sont autant de petites machines qui font fonctionner les cellules de tous les êtres vivants.
Or, si chaque cellule d’un organisme contient exactement la même information, sous la forme de l’ADN, comment expliquer que certaines cellules deviennent des neurones dans le cerveau, et que d’autres deviennent des cellules d’intestin ? Comment se fait-il que des cellules fonctionnent bien, et que d’autres tombent malade et deviennent des cancers ?
Tout cela s’explique par le fait que la cellule ne fait pas que lire bêtement tous les gènes au même moment. Elle est aussi capable de les réguler, grâce à des mécanismes que l’on appelle épigénétiques. Épigénétique, cela vient de la fusion du préfixe « epi », « au-dessus de » en grec et « génétique », la science relative aux gènes et à l’hérédité.
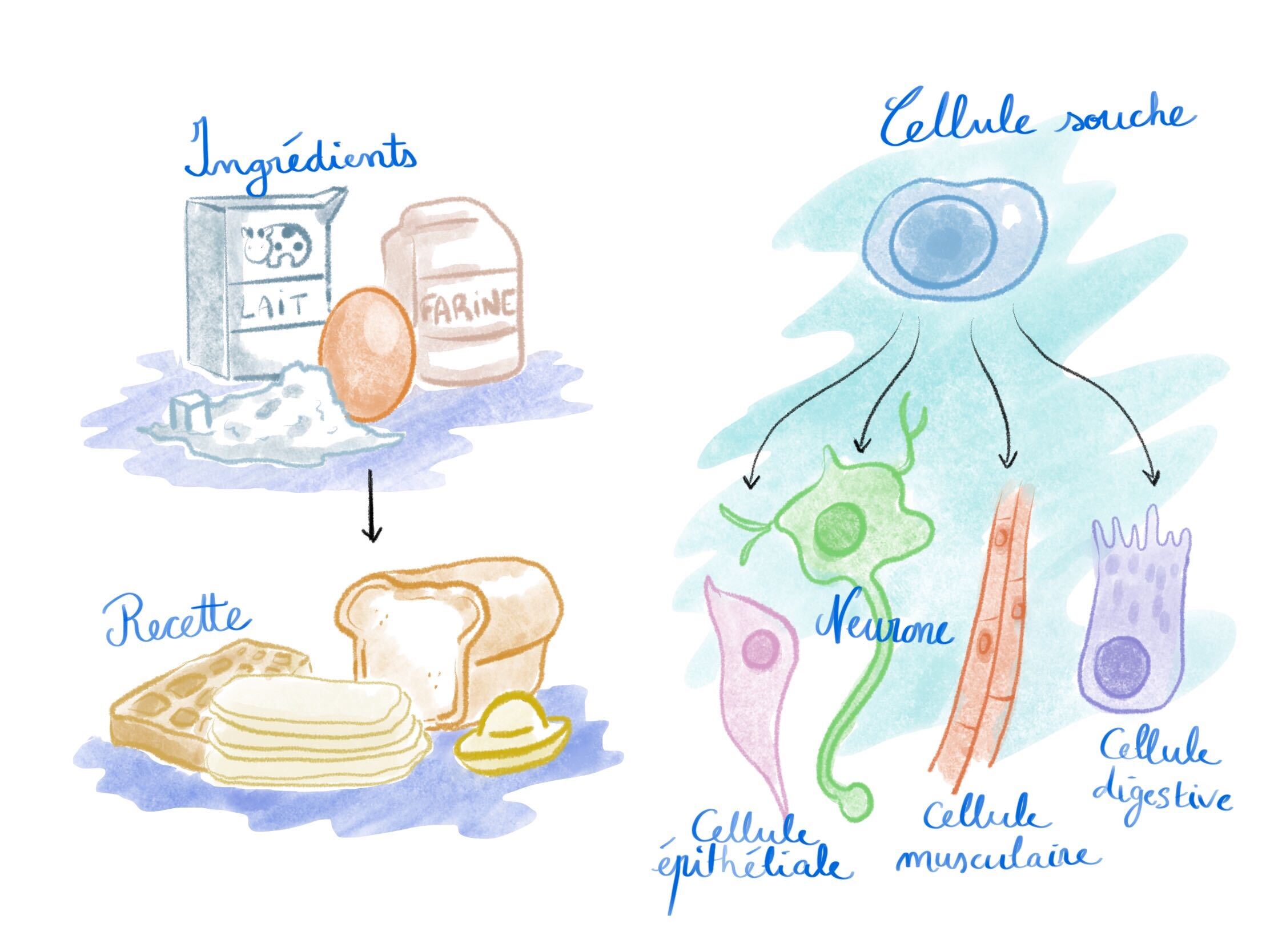
Si nos gènes étaient des ingrédients (des œufs, du lait, du sucre et de la farine), l’épigénétique serait en quelque sorte la recette qui permettrait de les combiner aux bons moments et dans les bonnes proportions pour obtenir des crêpes, des gaufres, des madeleines ou de la brioche (Figure 1). Mais trêve de métaphore culinaire, ou vous risquez de mourir de faim avant d’avoir fini cet article !
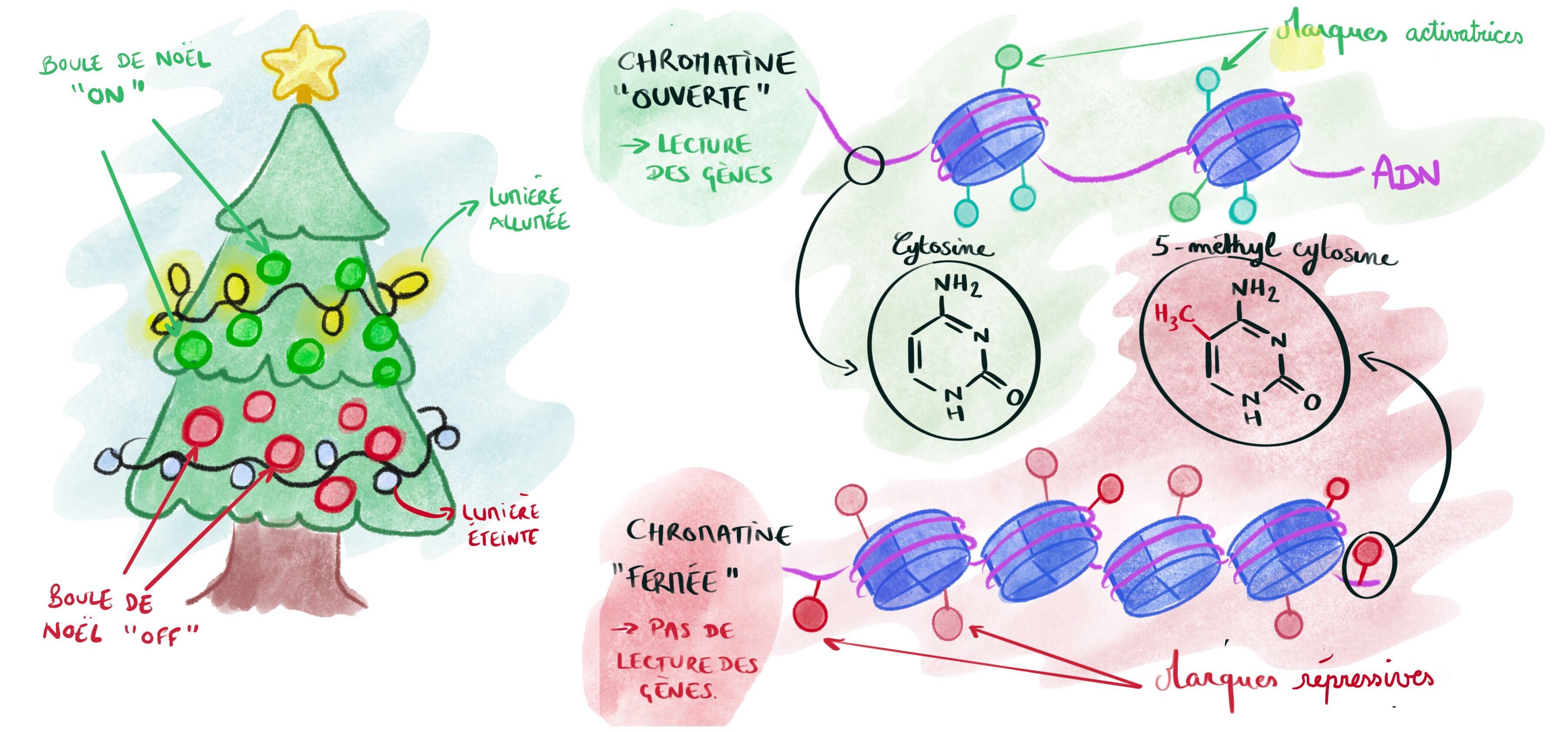
Comme un véritable arbre de Noël, l’ADN est décoré de toutes sortes de marques chimiques, qui sont autant de boules de Noël qui peuvent être posées et retirées à l’infini. Ces marques chimiques changent en permanence la manière dont l’information sera décryptée. Si l’ensemble de nos gènes est désigné par le terme génome (le sapin de Noël), l’ensemble des décorations de ce génome est appelé l’épigénome. Facile, n’est ce pas ?
Qui a la plus jolie boule ?
Dans une cellule, la régulation des gènes passe par la décoration de deux choses. Soit la molécule d’ADN elle-même, soit les petites pelotes de protéines autour desquelles cet ADN est enroulé, appelées histones. On estime qu’il y a plus de 70 décorations différentes sur ces histones [1] ! Sur celles-ci, certaines marques sont activatrices et vont permettre de lire le gène, d’autres sont dites répressives et permettent de mettre le gène en veille. Les scientifiques se sont rapidement demandés si l’ensemble de ces modifications ne correspondaient pas à un code crypté, qui, une fois décrypté, permettrait de mieux comprendre comment s’expriment les gènes (Figure 2).
Du côté de l’ADN en revanche, le sapin est moins garni. Pendant longtemps, on ne connaissait qu’une seule modification chimique : la méthylation de la cytosine. Une formule compliquée pour dire que l’une des briques de l’ADN porte un atome de carbone et 3 atomes d’hydrogène (-CH3) en plus que d’habitude. La méthylation de la cytosine est observée chez de nombreux êtres vivants, pour lesquels elle a des rôles très différents. Alors que chez les bactéries elle protège le matériel génétique de la dégradation par des enzymes, chez les autres êtres vivants elle a généralement pour conséquence d’empêcher les gènes de s’exprimer n’importe comment, et d’éviter que certains fragments d’ADN (que l’on appelle les rétrotransposons) « sautent » un peu partout pour aller se promener dans le génome.
Vous l’aurez compris, les chercheurs en épigénétique sont donc plus ou moins à la recherche de la plus belle boule de Noël et des règles de décoration du sapin. Une fois trouvées, ils les étudient et tentent de comprendre leur rôle et leur fonctionnement !
N6-méthyladénine : une nouvelle boule en rayon !
Dans cette étude, les chercheurs expliquent la découverte d’une nouvelle décoration de l’ADN dans des cellules embryonnaires de souris : la méthylation de l’adénine.
Pour comprendre ce qu’il se passe dans une cellule, les chercheurs ont actuellement des outils merveilleux : des canne à pêche à décorations, et des ciseaux moléculaires ! Grâce à une technique appelée immunoprécipitation de la chromatine, les auteurs de la publication ont réussi à pêcher spécifiquement une nouvelle modification chimique : la N6-méthyladénine (Figure 3). Cette décoration n’est pas présente partout sur le génome des embryons de souris étudiés, mais dans des endroits spécifiques : plutôt sur le chromosome X et notamment sur les rétrotransposons. Et cela pose la question suivante : à quoi cela peut-il servir de mettre une boule précise sur une branche de notre sapin, et pas sur une autre ?
Après quelques recherches, les scientifiques ont également pu prédire l’enzyme qui était capable de retirer cette boule de Noël dans la cellule. Son petit nom : ALKBH1. Pour bien comprendre ce que fait une enzyme dans une cellule, l’expérience la plus simple à mettre en œuvre est de la supprimer, et d’observer ce qu’il se passe en son absence. De nos jours, les chercheurs disposent d’un outil formidable pour ça : CRISPR-Cas9.
Cet outil fonctionne comme un ciseau qui coupe un endroit précis de l’ADN. Grâce à cela, on peut enlever la protéine de notre choix dans n’importe quelle cellule vivante (ou presque). En enlevant ALKBH1, les chercheurs constatent en effet que la quantité de N6-méthyladénine augmente, et toujours dans des régions où il y a des éléments génétiques sauteurs. Cette observation démontre bien le rôle de cette protéine, à savoir le retrait de cette nouvelle boule de Noël. En mesurant l’expression des gènes dans des populations de cellules qui ne disposent pas d’ALKBH1, et en le comparant à des cellules normales sans modification (c’est à dire dans les cellules où l’on n’a pas retiré ALKBH1), les auteurs se sont aussi rendus compte que l’expression de certains gènes était modifiée, notamment sur le chromosome X.
La nouvelle décoration de sapin identifiée peut donc contribuer à la régulation de ces gènes sur le chromosome X et sur l’expression des éléments sauteurs, les rétrotransposons. Ces éléments non codants ont la capacité de « sauter » dans le génome, ce qui peut avoir des conséquences délétères dans le cas où ils s’insèrent dans un gène, pouvant déréguler leur expression et être à l’origine de pathologies comme les cancers. Les auteurs suggèrent même qu’en régulant les rétrotransposons, la m6A pourrait indirectement réguler l’expression des gènes du chromosome X lors du développement des embryons. Notre nouvelle boule de Noël aurait donc un rôle très important dans le début de la vie de la souris !
Une nouvelle boule c’est bien, mais faut-il croire au père Noël ?
D’autres chercheurs soutiennent que cette boule n’existe pas vraiment et que les observations publiées dans cet article ne sont que des artefacts, des erreurs expérimentales. La N6-méthyladénine est-elle donc comme le père Noël ? Un concept auquel beaucoup de gens croient sans jamais l’avoir vraiment vu ?
Il est vrai que ces boules de Noël sont plutôt rares, et quand on travaille sur l’ADN, tout est si petit que l’on doit constamment utiliser des méthodes indirectes pour tirer des observations de nos expériences. C’est pour cela que les scientifiques, comme ce qui a été fait ici, publient bien souvent voire systématiquement le résultat de plusieurs expériences consécutives pour tester la même hypothèse, avant de réellement conclure. De plus, une seule étude est rarement suffisante, et la connaissance avance grâce à des faisceaux de résultats du monde entier que l’on assemble comme un puzzle pour mieux comprendre le monde dans lequel on vit. La recherche fonctionne pas à pas, et prend parfois du temps… ce n’est jamais inutile de le rappeler par les temps qui courent !
Pour finir, cet article, convaincant s’il en faut, nous montre qu’en biologie tout n’est jamais tout noir ou tout blanc. Tout l’enjeu de la recherche est de compiler des observations, souvent contradictoires, pour en tirer l’explication la plus cohérente et réajuster les hypothèses.
Si ces observations sont renouvelées et confirmées dans d’autres organismes et dans d’autres circonstances, il ne fait aucun doute que cette découverte permettra d’ouvrir de nouvelles possibilités et de nouveaux angles de recherche pour la compréhension de la régulation des gènes. Si des maladies humaines sont liées à ces erreurs de décoration, progressivement nous pourrions même envisager leur correction de façon à ce que les cellules fonctionnent à nouveau normalement ! Une chose est sûre : la chasse aux nouvelles boules de Noël ne fait que commencer !
[1] Tan M., et al., Identification of 67 histone marks and histone lysine crotonylation as a new type of histone modification. Cell, 2011. DOI : 10.1016/j.cell.2011.08.008. [Publication scientifique]
Écriture : Eléa Héberlé
Relecture scientifique : Aude Grézy
Relecture de forme : Yann Méheust
Temps de lecture : environ 14 minutes.
Thématiques : Génétique & Épigénétique (Biologie)
Publication originale : Wu T. P., et al., DNA methylation on N6-adenine in mammalian embryonic stem cells. Nature, 2016. DOI : 10.1038/nature17640
Version libre disponible ici.

Les scientifiques ont découvert une nouvelle façon de réguler l’expression des gènes. Grâce à une nouvelle décoration dans les cellules de souris, la 6-méthyladénine, on peut éteindre des gènes et empêcher des éléments génétiques de sauter partout et de mettre la pagaille ! Car en biologie, il y a l’étude des gènes — la génétique — et l’étude de leur régulation : l’épigénétique où il s’agit plus ou moins de comprendre de quelle façon le génome est décoré, comme des boules sur un sapin de Noël. De quoi réjouir la communauté scientifique, car ce n’est pas tous les jours qu’on trouve une nouvelle boule à mettre sur le sapin !
Plus fort que le génome, l’épigénome
On nous le répète assez en cours de biologie : l’ADN porte l’information génétique sous la forme de portions codantes appelés gènes. Pendant très longtemps, le dogme fondateur de la biologie moléculaire suggérait que chacun de nos gènes codait pour une protéine, et que l’ensemble de ces protéines déterminait le phénotype de chaque individu. Or, si chaque cellule d’un organisme contient exactement la même information, comment expliquer que nous ayons autant de types cellulaires différents ? Comment expliquer que certaines cellules dévient de leur route, pour passer d’un état de cellule souche pluripotente à un neurone, une cellule musculaire, ou une cellule digestive ? Comment expliquer qu’à partir de la même information, une cellule puisse devenir cancéreuse ?
Une nouvelle discipline a émergé, l’épigénétique, permettant d’étudier tous les phénomènes cellulaires contribuant à la régulation fine de l’expression des gènes, dans le temps et l’espace. Parmi ces phénomènes, certaines modifications chimiques apposées soit sur les molécules de compaction du brin d’ADN, les histones, soit apposées directement sur les acides nucléiques, permettent de moduler la compaction de l’information et l’accessibilité des gènes aux facteurs de transcription permettant leur lecture.
Comme un véritable arbre de Noël, l’ADN est décoré de toutes sortes de marques chimiques, qui sont autant de boules de Noël qui peuvent être posées et retirées à l’infini. Celles-ci changent en permanence la manière dont l’information sera décryptée. Si l’ensemble de nos gènes est désigné par le terme génome (le sapin de Noël), l’ensemble des décorations de ce génome est appelé l’épigénome. Facile, n’est ce pas ?
Qui a la plus jolie boule ?
Parmi ces ornementations, on retrouve la méthylation (ajout d’un groupement méthyl, CH3), l’acétylation, (ajout d’un groupement acétyl), la phosphorylation (ajout d’un groupement phosphate), l’ubiquitination (ajout d’un groupement ubiquitine), etc. Sur les histones, plus de 70 marques différentes ont été identifiées (des boules de Noël, il y en a plein en magasin !), permettant de changer la compaction de l’ADN et l’expression des gènes à proximité [1]. Certaines marques sont dites activatrices de l’expression, d’autres sont dites répressives, au point que très tôt, les scientifiques ont proposé l’hypothèse qu’un code des marques d’histones existait, et qu’il suffisait d’étudier leur combinatoire pour comprendre le jeu de l’expression des gènes. Malheureusement, en biologie moléculaire plus encore que partout ailleurs, tout est une histoire de contexte, et le code histone est encore loin d’avoir été craqué.
Du côté de l’ADN, la modification la plus connue est la méthylation de la cytosine sur son carbone numéro 5 (m5C) (Figure 1). La preuve formelle de l’existence de cette base modifiée a été apportée en 1948, par Rollin Douglas Hotchkiss [2]. La méthylation de la cytosine est observée chez de nombreux êtres vivants, pour lesquels elle a des rôles très différents. Alors que chez les bactéries elle protège le matériel génétique de la dégradation par des enzymes, chez les eucaryotes elle a généralement pour conséquence la répression de l’expression des gènes. D’autres éléments du génome sont aussi régulés par la 5mC, comme les transposons. Ces éléments non codants ont la capacité de « sauter » dans le génome, ce qui peut avoir des conséquences délétères dans le cas où ils s’insèrent dans un gène, pouvant déréguler l’expression des gènes et être à l’origine de pathologies comme les cancers. La méthylation de la cytosine est très étudiée, car la quantité de cette marque varie souvent dans les cellules cancéreuses. Plusieurs pistes de traitement visent d’ailleurs spécifiquement sa régulation.

Vous l’aurez peut-être compris, tous les biologistes du domaine de l’épigénétique sont donc plus ou moins à la recherche de la plus belle boule de Noël et des règles de décoration du sapin. Et l’étude décortiquée ici s’inscrit complètement dans ce contexte.
N6-méthyladénine : une nouvelle modification chimique de l’ADN
Chez les bactéries, une autre modification chimique de l’ADN est connue : la méthylation de l’adénine sur l’azote numéro 6, ou N6-méthyladénine (m6A) (Figure 2). Cette marque épigénétique est présente sur l’ARN messager de certains virus, mais a aussi été mise en évidence chez quelques eucaryotes comme la drosophile (Drosophila melanogaster), le nématode (Caenorhabditis elegans) et des algues vertes (Chlamydomonas reinhardtii). Alors que le consensus jusqu’alors voulait que la m5C soit la seule modification de l’ADN chez les mammifères, l’article sur lequel on se penche ici révèle l’existence de m6A dans des cellules souches embryonnaires de souris, dites cellules ES. Chez les eucaryotes, on considère que la m5C est une marque qui a plutôt un rôle de répression de l’expression des gènes, tandis que les premiers articles décrivant la m6A montraient que cette dernière avait un rôle opposé, favorisant l’expression des gènes.

Avec l’apparition de la génomique — l’étude de génomes dans leur intégralité — permise par de nouvelles méthodes comme le séquençage à haut débit, les chercheurs ont désormais accès à toute la séquence génomique de n’importe quel organisme. Grâce au développement de nouveaux outils, comme des anticorps permettant de rechercher ces marques épigénétiques (les boules de Noël), il est possible d’en identifier et de les localiser dans les génomes.
C’est exactement ce que les auteurs ont réalisé avec la m6A. En utilisant une méthode de séquençage très précise appelée SMRT (Single molecule real-time sequencing), ils se proposent de mettre en évidence la répartition de m6A dans le génome (Figure 3). La méthode étant très coûteuse, ils ne peuvent se permettre de choisir qu’une petite portion du génome à analyser, et décident donc de procéder au séquençage après avoir pêché des régions d’ADN associées à un variant d’histone appelé H2A.X, par immunoprécipitation de la chromatine (ChIP). Ils ont choisi H2A.X car, d’après les données disponibles, cette protéine est associée à des régions génomiques importantes dans la différenciation cellulaire.
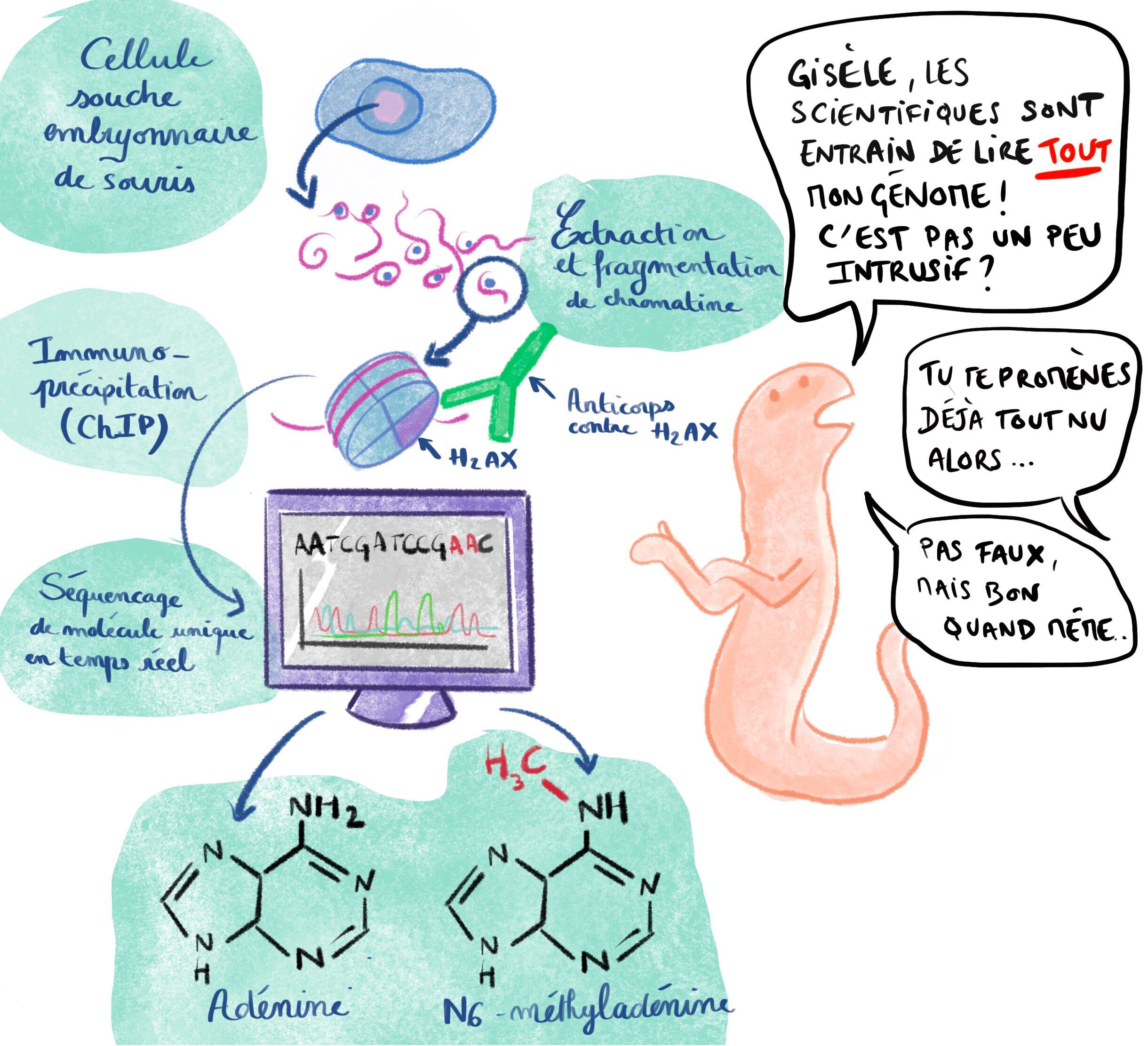
Après séquençage, ils se rendent compte que la m6A semble plus abondante dans les régions intergéniques (= entre les gènes), qui ne sont pas directement codantes. Leur estimation de l’abondance des m6A est de 25 à 30 par million d’adénines présentes, ce qui n’est pas énorme ! Est-il toutefois possible que ces quelques bases modifiées puissent avoir un impact biologique ? C’est précisément ce qu’ils essayent de comprendre dans la suite de l’article.
À la recherche du meilleur ciseau pour la méthylation de l’adénine
Pour comprendre la stratégie suivante des auteurs, il faut comprendre deux choses. Premièrement, en biologie, qui dit modification chimique dit enzyme capable d’ajouter et de retirer cette décoration. Les enzymes qui ajoutent de la méthylation sont généralement nommées méthyl-transférases, tandis que celles qui retirent la méthylation sont des déméthylases. Deuxièmement, lorsque l’on fait de la génétique, la méthode la plus simple pour connaître la fonction d’un gène est de le retirer de l’organisme étudié et d’observer les conséquences de cette perte de fonction.
Les auteurs ont donc naturellement choisi de trouver la déméthylase capable de retirer la m6A. S’inspirant de travaux sur d’autres organismes, ils jettent leur dévolu sur le gène Alkbh1. Prenant en compte la similitude de Alkbh1 avec le gène d’une déméthylase équivalente présente chez la bactérie, ils décident de générer des lignées de cellules ES dont la protéine correspondante, ALKBH1, serait absente. Pour cela, ils utilisent la technique d’édition génétique CRISPR-Cas9 en ciblant l’exon 3 du gène Alkbh1. L’efficacité de coupure n’étant pas de 100 %, toutes les cellules dans lesquelles les ARN guides spécifiques de Alkbh1 sont exprimés ne subissent pas de modifications, et ces cellules non modifiées peuvent ensuite servir de contrôle dans les expériences. Pour distinguer entre une cellule modifiée et non modifiée, les scientifiques peuvent identifier très tôt sur des populations dérivant de cellules uniques (que l’on appelle des clones) si oui ou non l’édition génique a fonctionné.
Dans les cellules dépourvues d’ALKBH1, le niveau de m6A semble bel et bien augmenter, ce qui confirme leur hypothèse selon laquelle ALKBH1 serait la déméthylase de m6A. En parallèle, ils parviennent à purifier l’enzyme ALKBH1 et démontrent qu’in vitro, hors des cellules, celle-ci est bien capable de retirer la méthylation de petits brins d’ADN synthétiques dont les adénines sont méthylées.
Super, mais à quoi ça sert ?
Pour mieux comprendre quel serait l’effet d’une accumulation de m6A dans ces cellules embryonnaires de souris générées précédemment, les auteurs se sont tournés vers d’autres expériences.
Grâce à une technique de séquençage de l’ARN, ils parviennent à montrer qu’une portion de gènes exprimés d’ordinaire dans des cellules embryonnaires sont réprimés dans leur lignée dépourvue d’ALKBH1. Les gènes dont l’expression varient semblent être portés principalement sur le chromosome X et sur le chromosome 13, et impliqués dans l’identité cellulaire.
Par ailleurs, la m6A semble localisée principalement au niveau d’une catégorie de transposons que les auteurs définissent comme jeunes… c’est à dire apparus dans le génome il y a moins d’1,5 millions d’années. On est d’accord, ce n’est pas si jeune que ça, mais ils sont encore capables de se déplacer dans le génome, contrairement à des éléments plus vieux qui ont perdu des bouts de séquence leur permettant de « sauter ». On appelle ces éléments encore capables de sauter longs éléments nucléaires espacés-1 (LINE-1 en anglais) (quelques détails sur les LINE en [*]).
En comparant le niveau d’autres modifications comme la méthylation de l’histone H3, ou la quantité d’H2A.X, qui sont d’ordinaire présentes aux abords de ces éléments transposables, les chercheurs ne constatent aucune différence notable entre les cellules normales et les cellules dépourvues d’ALKBH1. La m6A pourrait alors à elle seule être responsable de l’inactivation des éléments transposables à certains moments du développement embryonnaire, les empêchant de « sauter » intempestivement, ce qui pourrait provoquer des erreurs de développement.
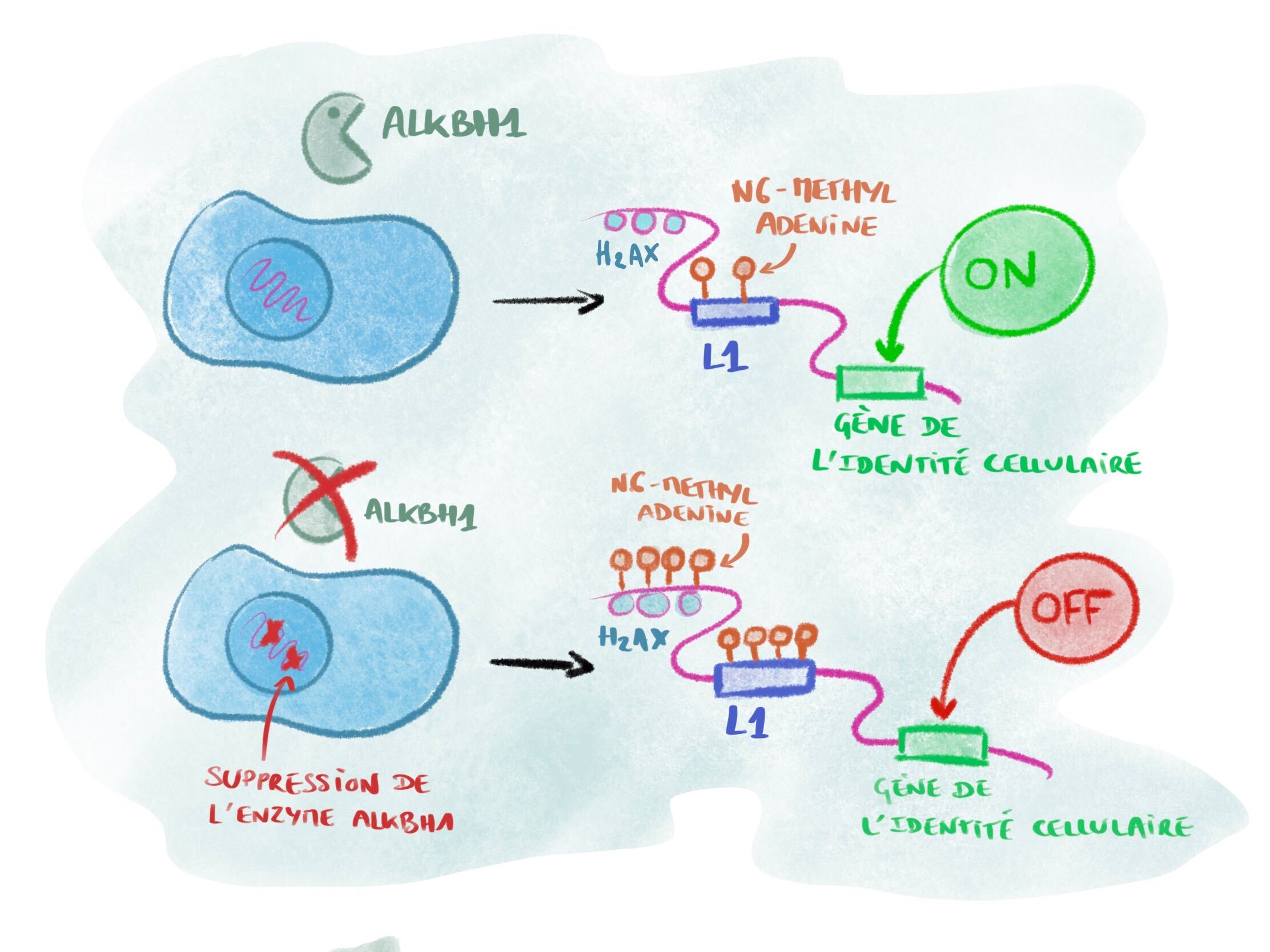
Grâce à tous ces éléments expérimentaux, les auteurs pensent donc avoir identifié une nouvelle marque épigénétique qui serait impliquée à la fois dans la régulation des gènes du chromosome 13 et du chromosome X et dans le contrôle des éléments génétiques mobiles actifs et récents répartis sur le génome. L’une des hypothèses mentionnée dans l’article est que la m6A pourrait jouer un rôle dans le contrôle des LINE, ce qui aurait ensuite des conséquences indirectes dans le phénomène d’inactivation du chromosome X (Figure 4). Ce phénomène génétique permet l’expression des gènes d’une seule des deux copies du chromosome X chez les femelles de mammifères, dont le sexe est déterminé par les chromosomes sexuels XX ou XY.
Chasse aux boules : laquelle sera la bonne ?
L’article, publié dans la très prestigieuse revue Nature, a eu un certain retentissement. Encore une nouvelle boule de Noël à prendre en compte dans la grande guirlande du langage ADN !
Le répertoire de modifications de l’ADN semble constamment s’étendre, mais certains auteurs ont émis des doutes quant aux résultats de l’étude, et les conclusions portent à controverse. Alors que certaines équipes mettent en évidence la même modification dans d’autres tissus de souris, ou dans des cellules embryonnaires, d’autres auteurs sont catégoriques : la m6A chez les mammifères est un artefact expérimental [3]. Une autre étude très récente prouve d’ailleurs que les méthodes de détection de la m6A sont toutes sévèrement biaisées, et met en garde contre les conclusions hâtives dans le domaine des modifications chimiques de l’ADN [4].
S’il est vrai que les quantités de m6A détectées sont très faibles, et donc à la limite même des seuils de détection des méthodes utilisées, comment expliquer les effets biologiques de la suppression de l’enzyme ALKBH1 chez la souris ? Cette protéine aurait-elle d’autres rôles lors du développement ?
Et s’il s’agissait bel et bien d’un artefact ? Qu’à cela ne tienne, de nombreuses autres modifications de l’adénine et de la cytosine ont été mises en évidence, et ce domaine de recherche a encore de beaux jours devant lui [3]. Retirer la méthylation de la cytosine résulte par exemple en la formation de toutes sortes de sous produits chimiques, qui pourraient eux aussi avoir un rôle dans la régulation des gènes. En attendant la réponses, la m6A n’a donc pas fini de faire parler d’elle… mais quelque part, heureusement que les scientifiques ont encore des questions à se poser n’est ce pas ?!
Pour finir, cet article, convaincant s’il en faut, nous montre qu’en biologie tout n’est jamais tout noir ou tout blanc. Tout l’enjeu de la recherche est de compiler des observations, souvent contradictoires, pour en tirer l’explication la plus cohérente et réajuster les hypothèses.
Dans le domaine de l’épigénétique, une meilleure compréhension de tous les mécanismes en jeu permettra sans aucun doute de mieux comprendre l’apparition de pathologies et d’y remédier à l’avenir. La chasse aux boules de Noël a encore de beaux jours devant elle !
[*] Les éléments transposables sont des petites portions d’ADN capables de se propager de façon autonome dans le génome. Il en existe plusieurs catégories, ceux qui se « copient-collent », comme les rétrotransposons, dont font partie les LINE et ceux qui se « coupent-collent ». Les transposons LINE-1 mentionnés dans l’article représentent une part non négligeable du génome (environ 15 % du génome humain), et sont d’ordinaires réprimés, à part pendant le développement embryonnaire, et dans des contextes cancéreux. Ils ont un rôle important dans la régulation de l’expression de gènes, dont le détail est encore mal compris. D’autres types de ces éléments, apparus il y plus longtemps au cours de l’évolution ne semblent pas montrer cette modification chimique. Ayant perdu les fragments leur permettant de se déplacer, il est possible qu’ils n’aient plus besoin d’être régulés par ce biais.
[1] Tan M., et al., Identification of 67 histone marks and histone lysine crotonylation as a new type of histone modification. Cell, 2011. DOI : 10.1016/j.cell.2011.08.008. [Publication scientifique]
[2] Hotchkiss R. D., The Quantitative Separation of Purines, Pyrimidines, and Nucleosides by Paper Chromatography. J. Biol. Chem., 1948. [Publication scientifique]
[3] Schiffers S., et al., Quantitative LC–MS Provides No Evidence for m6dA or m4dC in the Genome of Mouse Embryonic Stem Cells and Tissues. Angew. Chem. Int. Ed., 2017. DOI : 10.1002/anie.201700424. [Publication scientifique]
[4] Douvlataniotis K., et al., No evidence for DNA N6-methyladenine in mammals. Sci. Adv., 2020. DOI : 10.1126/sciadv.aay3335. [Publication scientifique]